Clear Sky Science · ar
يدعم PTBP1 تكوّن الحيوانات المنوية لدى الفئران من خلال تيسير تنظيم الهيكل الخلوي عبر مسار mTORC2–PKCα في خلايا سيرتولي
لماذا تهم هذه الدراسة الخصوبة الذكرية
غالبًا ما تبدو العقم لدى الذكور غامضًا، لكن جوهره يقوم على شراكة دقيقة بين الحيوانات المنوية النامية و"خلايا الممرضة" التي تدعمها. تبحث هذه الدراسة في أحد المساعدين الجزيئيين الخفيين داخل تلك الخلايا الممرضة وتبيّن كيف أن فشله يمكن أن يوقف إنتاج الحيوانات المنوية. فهم هذه الطبقة المخفية من الضبط قد يفتح الطريق نحو تشخيصات أو علاجات جديدة لبعض أشكال العقم الذكري.
خلايا الدعم التي تجعل تكوين الحيوانات المنوية ممكنًا
تتكوّن الحيوانات المنوية داخل أنابيب طويلة ملتفة في الخصية تُسمى الأنابيب المنوية. تبطن هذه الأنابيب خلايا سيرتولي، وهي نوع متخصّص من خلايا الدعم التي تحضن الخلايا الجرثومية النامية، تُغذيها، وتهيئها أثناء انقسامها ونضوجها إلى حيوانات منوية. تبني خلايا سيرتولي أيضًا جدارًا واقيًا يُعرف بحاجز الدم–الخصية، الذي يفصل الخلايا في المراحل المبكرة عن جهاز المناعة. لتنفيذ كل ذلك، تعتمد على هيكل داخلي من خيوط الأكتين والأنابيب المجهرية الذي يعيد تشكيل نفسه باستمرار بينما تتحرك موجات الخلايا الجرثومية عبر الأنابيب. إذا تعرض هذا الهيكل للاضطراب، يتسرب الحاجز وقد تنفصل الخلايا الجرثومية النامية أو تموت، مما يهدد الخصوبة.
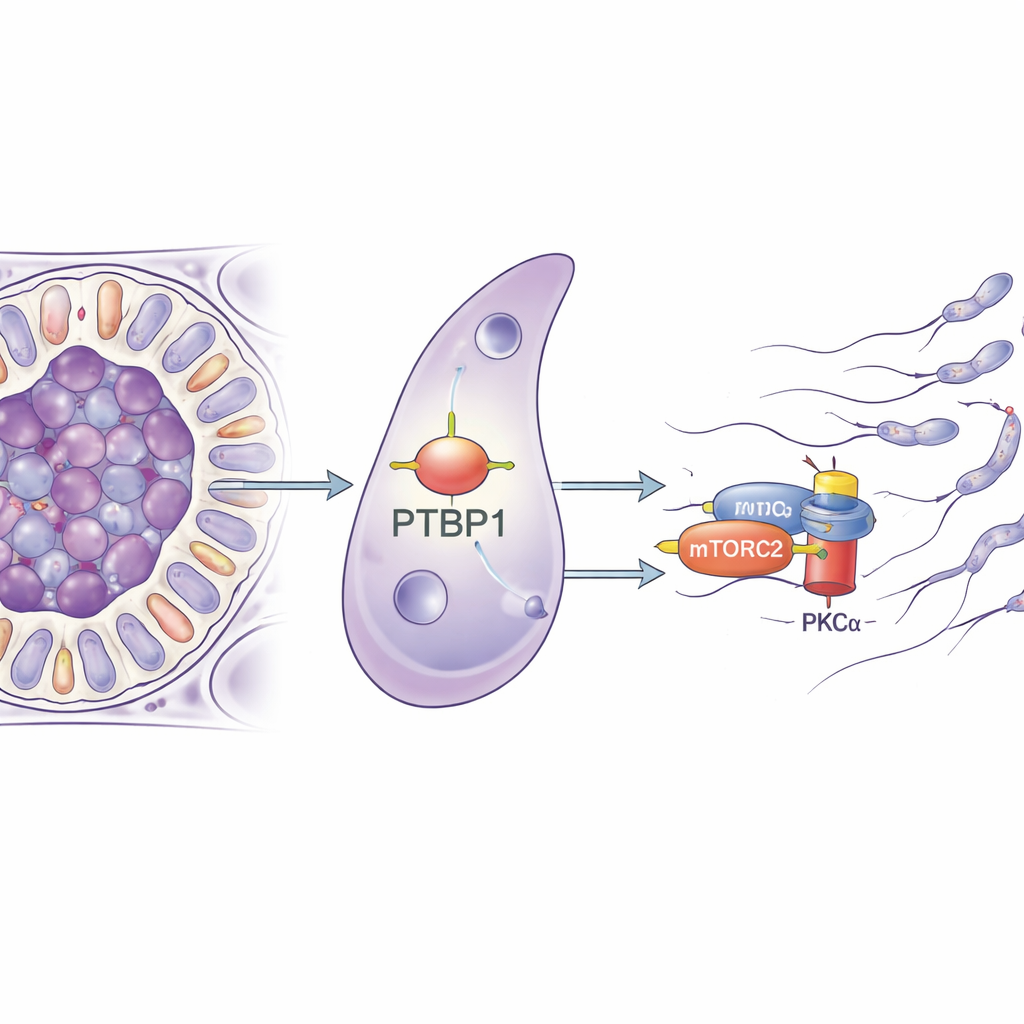
مدير RNA صغير ذو مهمة كبيرة
ركّز الباحثون على بروتين يدعى PTBP1، المعروف بدوره في إدارة جزيئات الحمض النووي الريبي داخل الخلايا—بتحكّمه في كيفية اقتطاع الجينات، وثبات رسائلها، ومدى كفاءتها في الترجمة إلى بروتين. يتواجد PTBP1 بكثرة في كل من الخلايا الجرثومية وخلايا سيرتولي، وأظهرت أعمال سابقة أن حذفه من الخلايا الجرثومية يعيق إنتاج الحيوانات المنوية. في هذه الدراسة، حذف الفريق PTBP1 فقط من خلايا سيرتولي لدى الفئران. بدا الفئران الصغيرة عادية للوهلة الأولى، لكن مع بلوغها النضج الجنسي انكمشت خصاها، وانخفض عدد الحيوانات المنوية في البربخ بشكل حاد، ولم يستطع أي من الذكور إنجاب ذرية، ما كشف عن فقدان كامل للخصوبة.
عندما ينهار الهيكل الخلوي
أظهر الفحص المجهري لخصاى هذه الفئران أن تكوّن الحيوانات المنوية توقف في منتصف الطريق. احتوت العديد من الأنابيب على فراغات، وتكتلات غير طبيعية من نوى الخلايا الجرثومية المندمجة، ونقصًا في الحيوانات المنوية المطولة بالكامل. غالبًا ما كانت نوى خلايا سيرتولي، التي عادة ما تلامس الجدار الخارجي للأنابيب، متزاحة نحو المركز، مما يوحِي بأن هذه الخلايا الممرضة فقدت تماسكها مع البنية المحيطة. أكد تلوين مكونات الوصلات والبروتينات الهيكلية الرئيسية أن حاجز الدم–الخصية مُضعف وأن حزم الأكتين الضيقة المعتادة استبدلت بشرائط فوضوية ومكثفة تمتد من القاعدة إلى مركز الأنبوب. تسربت جزيئة متتبعة كانت تبقى عادة على جانب "الدم" من الحاجز إلى أعماق الأنابيب، ما بيّن بشكل مباشر انهيار الحاجز.
تتبع الفشل إلى محور إشارات
لفهم كيف لبروتين رابط للـ RNA أن يؤدي إلى مثل هذه المشكلات الميكانيكية، نقّح الفريق خلايا سيرتولي وحلل أي الجينات تغيّرت نشاطها عندما غاب PTBP1. كانت العديد من الجينات المتأثرة متورطة في التحكم في هيكل الخلية وكيفية التصاق الخلايا ببعضها، مما يشير إلى عيب واسع في إعادة التشكيل. ثم استخرج الباحثون جزيئات الحمض النووي الريبي التي ترتبط فعليًا بـ PTBP1 ووجدوا أنه يتصل برسالة Rictor، وهو جزء أساسي من مركب إشارات يُسمى mTORC2. هذا المركب بدوره ينشط إنزيمًا يُدعى PKCα الذي يشكل خيوط الأكتين. في خلايا سيرتولي الخالية من PTBP1، انخفضت كمية بروتين RICTOR، وكان نشاط PKCα أقل بكثير، رغم أن مستوى الحمض النووي الريبي لِRictor تغيّر بالكاد. وهذا يوحي بقوة أن PTBP1 يساعد خلايا سيرتولي على إنتاج كمية كافية من بروتين RICTOR من رسالته الـ RNA، وبالتالي يحافظ على نشاط مسار mTORC2–PKCα.
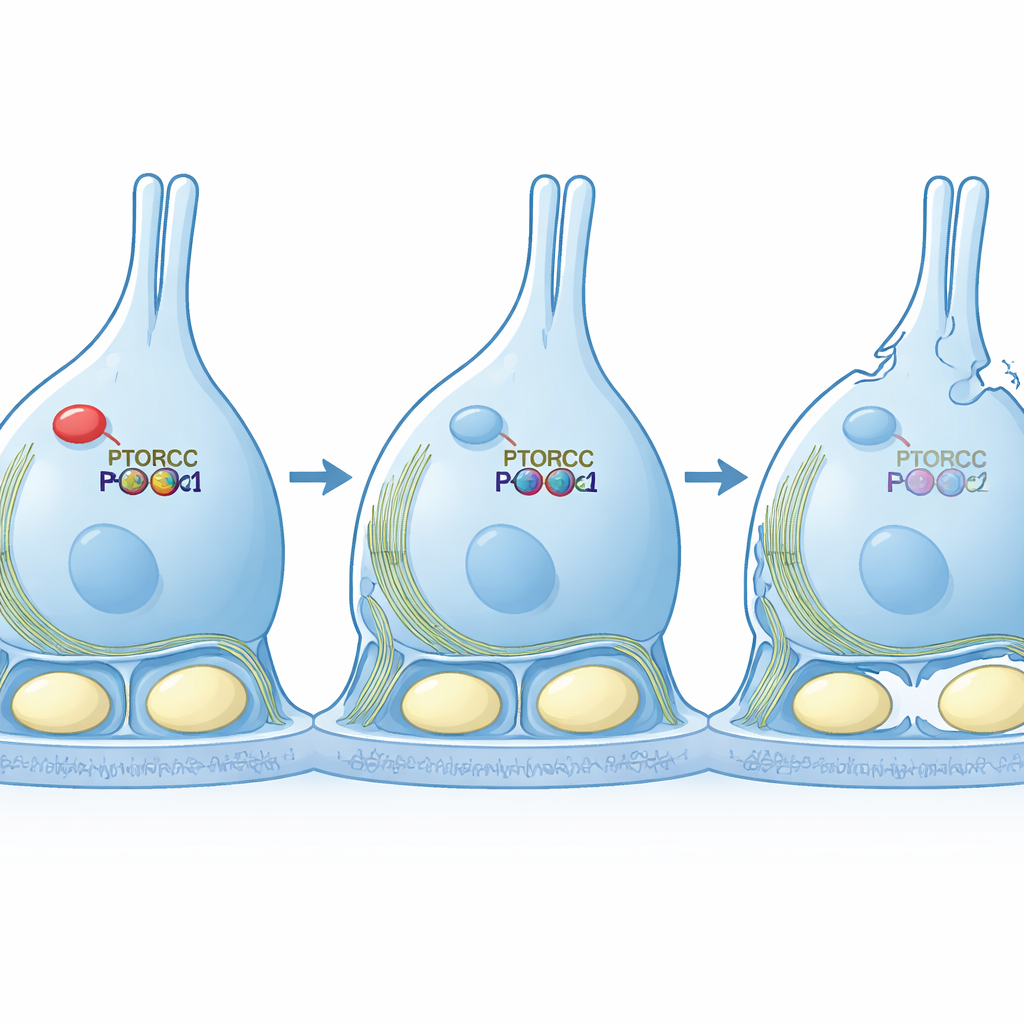
إنقاذ الهيكل عبر استعادة الإشارة
انتقل الفريق بعد ذلك إلى نماذج مزروعة لاختبار السببية. عندما قللوا PTBP1 في سطر خلوي يشبه خلايا سيرتولي، امتدت الخلايا إلى أشكال طويلة ونحيفة وأظهرت شبكة أكتين مشوشة—علامات على ضعف إشارة mTORC2. والأهم من ذلك، أنه عندما أجبروا هذه الخلايا على إنتاج نسخة فعّالة دائمة من PKCα، استعادت الخلايا شكلها المدمج الطبيعي وبنى أكتين أكثر انتظامًا، رغم أن مستوى RICTOR ظل منخفضًا. يوضح هذا التجربة الإنقاذية أن الوظيفة الأساسية لـ PTBP1 في هذا السياق هي الحفاظ على مسار mTORC2–PKCα قويًا بما يكفي لتنظيم الهيكل الداخلي للخلية.
ما الذي يعنيه هذا لفهم العقم
بعبارة بسيطة، تكشف هذه الدراسة سلسلة اعتماد داخل الخصية: يساعد PTBP1 خلايا سيرتولي على بناء محور إشارات رئيسي؛ هذا المحور ينظّم هيكلها الداخلي؛ والهيكل السليم يمكنها من الإمساك بالخلايا الجرثومية وحمايتها أثناء نموها. اكسر السلسلة عند PTBP1، فتفقد خلايا سيرتولي بنيتها، وينهار الحاجز الواقي، ويتوقف نمو الحيوانات المنوية، ما يؤدي إلى العقم الذكري. على الرغم من أن هذا البحث أُجري على الفئران، فإن الجزيئات نفسها موجودة في البشر، ما يثير احتمال أن عيوبًا طفيفة في ضبط الـ RNA داخل خلايا سيرتولي قد تكون السبب وراء بعض حالات العقم الذكري غير المفسرة، ويقدّم مجموعة جديدة من الأهداف الجزيئية للدراسات المستقبلية.
الاستشهاد: Ozawa, M., Taguchi, J., Mori, H. et al. PTBP1 supports mouse spermatogenesis by facilitating cytoskeletal organization through the mTORC2–PKCα pathway in Sertoli cells. Commun Biol 9, 341 (2026). https://doi.org/10.1038/s42003-026-09636-5
الكلمات المفتاحية: الخصوبة الذكرية, خلايا سيرتولي, تكوّن الحيوانات المنوية, الهيكل الخلوي, بروتينات رابطة للحمض النووي الريبي