Clear Sky Science · ar
نوتش3 ينظم اللدونة الظاهرية للخلايا الغمدية في سرطان القولون والمستقيم
لماذا تهم الأوعية الدموية المحيطة بالأورام
يعد سرطان القولون والمستقيم واحداً من أكثر السرطانات شيوعاً وفتكاً عالمياً، ومع ذلك تستهدف معظم العلاجات الخلايا الورمية مباشرة وغالباً ما تتجاهل نظام الدعم المحيط الذي يساعد الأورام على النمو. تركز هذه الورقة على مجموعة أقل شهرة من الخلايا الداعمة تُدعى الخلايا الغمدية، التي تحيط بالأوعية الدموية الدقيقة. من خلال كشف كيفية تغيير مفتاح إشارِي يُسمّى Notch3 لسلوك الخلايا الغمدية، يظهر الباحثون كيف يمكن دفع إمداد الدم للورم نحو أوعية أكثر تسرباً وفوضوية تفضّل السرطان، أو نحو أوعية أكثر طبيعية قد تُبطئ المرض وتحسّن فعالية العلاج. 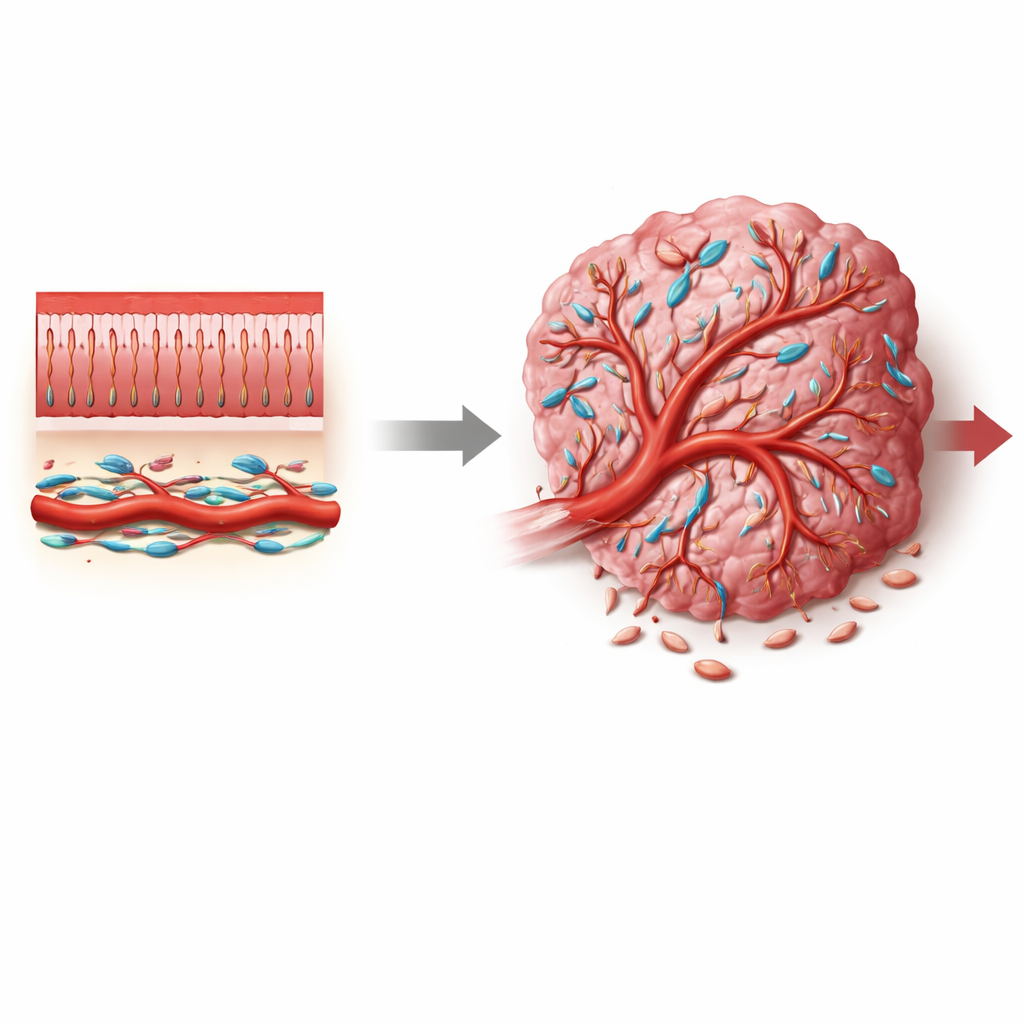
المعينون الخفيون حول أوعية الورم
الأوعية الدموية أكثر من أنابيب جوفاء فقط. في الأنسجة السليمة، تحيط بالخلايا الغمدية الأوعية الدقيقة بإحكام—وهي خلايا متخصصة تثبت جدران الأوعية، تتحكم بتدفق الدم، وتحد من التسرب. في الأورام، مع ذلك، تظهر هذه الخلايا الغمدية غالباً بمظهر وسلوك مختلفين: فقد تنفصل، تتكاثر، أو تغير هويتها، مما يساهم في الأوعية الشاذة والمتسربة النموذجية لدى السرطانات. في أورام القولون والمستقيم، حيث البيئة الدقيقة مليئة بالخلايا الليفية والخلايا المناعية وخلايا الأوعية، لم يكن واضحاً من أين تأتي الخلايا الغمدية المرتبطة بالورم، وما الحالات التي تتبناها، وأي الإشارات الجزيئية تدفعها نحو أدوار تساعد الورم.
تتبع الخلايا الغمدية أثناء تكوّن الأورام
لتتبع الخلايا الغمدية مع مرور الوقت، استخدم الباحثون نماذج فأرية لسرطان القولون والمستقيم المرتبط بالتهاب القولون حيث أمكنهم «وسم» أنواع خلوية معينة وراثياً ومراقبة مصيرها. أظهروا أن الخلايا الغمدية الموجودة في الأورام تنشأ إلى حد كبير من الخلايا الغمدية المقيمة طبيعياً في النسيج والتي تتوسع وتتكاثر مع تطور السرطان، بدلاً من قدومها من مصادر بعيدة مثل النخاع العظمي. باستخدام تسلسل RNA الخلوي المتقدم على مستوى خلية واحدة، صنّفوا عشرات الآلاف من الخلايا الداعمة من أورام الفئران والقولون الطبيعي ووجدوا أن الخلايا الغمدية مُعزَّزة بشكل ملحوظ في البيئة الدقيقة للورم. كما حددوا توسعاً مشابهاً للخلايا الغمدية في عدة مجموعات بيانات بشرية لسرطان القولون والمستقيم، مما يؤكد أن هذه الظاهرة ليست خاصة بالفئران فقط.
مفتاح جزيئي يغيّر سلوك الخلايا الغمدية
ثم سأل الفريق أي الإشارات تشكّل سلوك الخلايا الغمدية داخل الأورام فوجدوا أن Notch3—مستقبل يتيح للخلايا التواصل مع جيرانها—نشط بشكل خاص في الخلايا الغمدية الورمية. أشارت التحليلات الحسابية لتواصل الخلية–الخلايا إلى أن الخلايا الغمدية ترسل وتتلقّى إشارات مرتبطة بـNotch، خصوصاً عبر شركاء على خلايا الأوعية الدموية. عبر تفعيل Notch3 صناعياً في الخلايا الغمدية، لاحظ الباحثون أن هذه الخلايا تكثّرت أكثر لكن عبّرت عن بروتينات تقلصية أقل مرتبطة عادةً بسلوك تثبيت الأوعية. أصبحت أوعية الورم في هذه الفئران أكبر وأكثر تسرباً ومبطنة بمزيد من الخلايا البطانية المتكاثرة، مما يدل على أوعية أقل استقراراً. وعلى العكس، أدت إزالة Notch3 إلى تقليل تكاثر الخلايا البطانية، وتصغير حجم الأوعية، وخفض التسرب، مما يشير إلى تحول نحو أوعية دموية أكثر تطبيعاً دون تغيير كبير في عدد الأورام المبكرة أو حجمها. 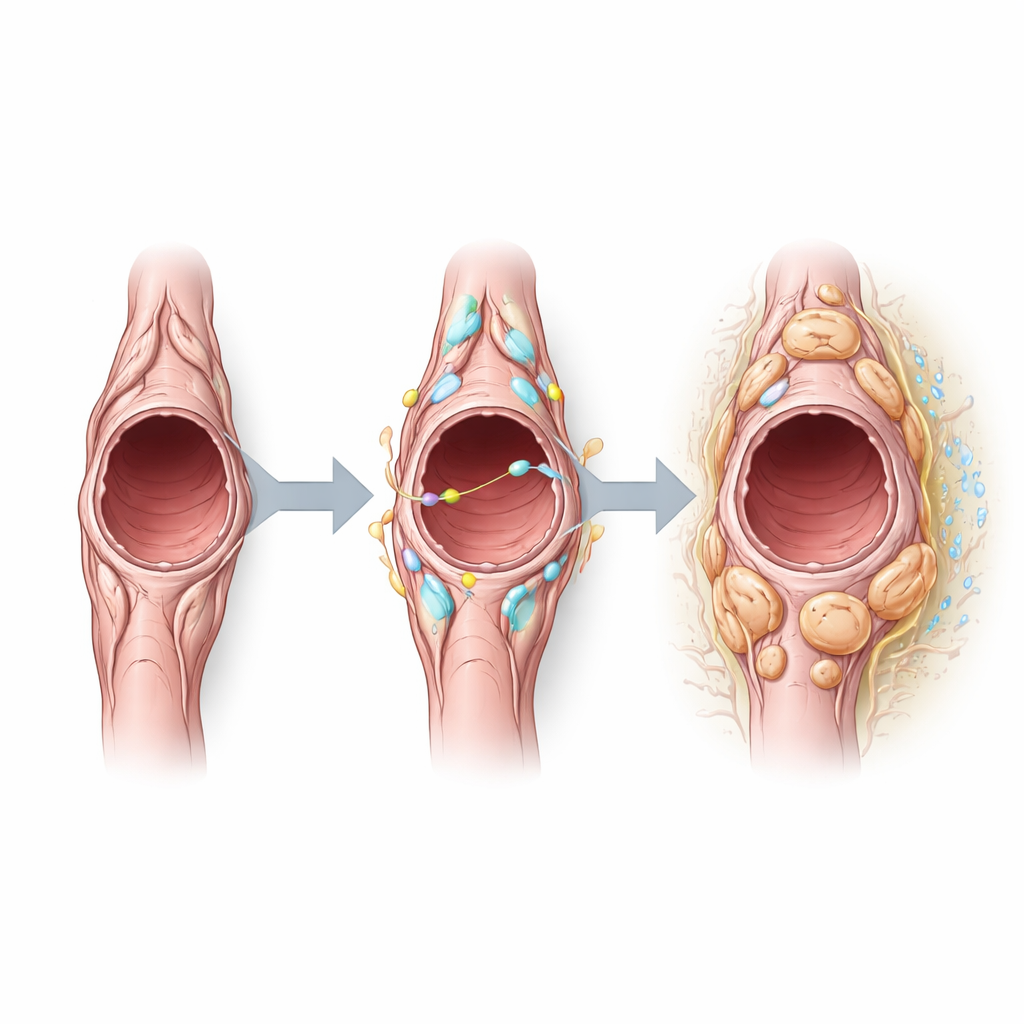
وجوه متعددة للخلايا الغمدية داخل الأورام
بعيداً عن التغيرات البسيطة تشغيل/إيقاف، كشفت الدراسة أن الخلايا الغمدية الورمية توجد في عدة حالات مميزة. أظهر بعض الفصائل ميزات خلايا شديدة الانقباض، وأنتج البعض كميات كبيرة من المصغّر خارج الخلية، وأبدت فئات أخرى سمات التهابية، وحملت مجموعة فرعية حتى توقيعات تُرى عادةً في الخلايا البطانية. لم يكن نشاط Notch3 موزعاً بالتساوي: فقد كان ثرياً في مجموعة خلوية «تصنيعية» أو منتجة للمصفوفة وقليلاً في الفئة الأكثر انقباضاً. أشارت تحليلات المسار إلى أن الخلايا الغمدية يمكن أن تتحول من حالة انقباضية نحو حالة تصنيعية متكاثرة مع ارتفاع نشاط Notch3. وعند فحص بيانات بشرية لسرطان القولون والمستقيم، وجد الباحثون طيفاً مماثلاً من حالات الخلايا الغمدية ورأوا مجدداً نشاطاً أعلى لجين هدف لـNotch3 في الخلايا الغمدية المرتبطة بالورم والمتكاثرة، مما يعكس نتائج الفئران.
تحويل فوضى الأوعية إلى فرصة علاجية
بشكل عام، تصوّر الدراسة Notch3 كمفتاح أساسي يضبط هوية الخلايا الغمدية ومن خلال تأثيرها، بنية وعمل أوعية الورم. يدفع ارتفاع نشاط Notch3 الخلايا الغمدية نحو حالة متكاثرة وأقل انقباضاً مرتبطة بأوعية متضخمة ومتسربة تفضّل تقدم الورم. يرتبط انخفاض نشاط Notch3 بخلايا غمدية أكثر انقباضاً، وخلايا بطانية أكثر هدوءاً، وأوعية أكثر تطبيعاً قد تكبح نمو الورم وتحسّن توصيل الأدوية. عبر استهداف Notch3 بشكل محدد في الخلايا الغمدية، قد توجه العلاجات المستقبلية أوعية الورم بعيداً عن الفوضى ونحو الاستقرار، مقدمة زاوية جديدة لعلاج سرطان القولون والمستقيم المتقدم بالتزامن مع الأدوية الحالية.
الاستشهاد: Chalkidi, N., Stavropoulou, A., Arvaniti, VZ. et al. Notch3 regulates pericyte phenotypic plasticity in colorectal cancer. Commun Biol 9, 343 (2026). https://doi.org/10.1038/s42003-026-09629-4
الكلمات المفتاحية: سرطان القولون والمستقيم, البيئة الدقيقة للورم, الخلايا الغمدية, إشارة Notch3, أوعية دموية سرطانية