Clear Sky Science · ar
تنظيم TRIM47 البطاني لجدار الدماغ الدماغي وسلامة الحاجز الدماغي الدموي والذاكرة عبر مسار الإشارة KEAP1/NRF2 في الفئران
لماذا حماية الأوعية الدقيقة في الدماغ مهمة
مرض الأوعية الدموية الصغيرة الدماغية هو معطل صامت في الدماغ. يَتلف أصغر الأوعية الدموية، ويزيد من خطر السكتة الدماغية، ويقوّض الذاكرة والتفكير ببطء، ومع ذلك لا يزال الأطباء يفتقرون إلى علاجات تتعامل مع أسبابه البيولوجية الجذرية. يتعرض هذا البحث لبروتين محدد، TRIM47، الموجود في خلايا بطانة أوعية الدماغ، ليطرح سؤالاً بسيطاً لكنه حاسم: هل يساعد هذا البروتين في الحفاظ على سلامة الحاجز الدموي الدماغي، وهل لذلك تأثير على الإدراك؟
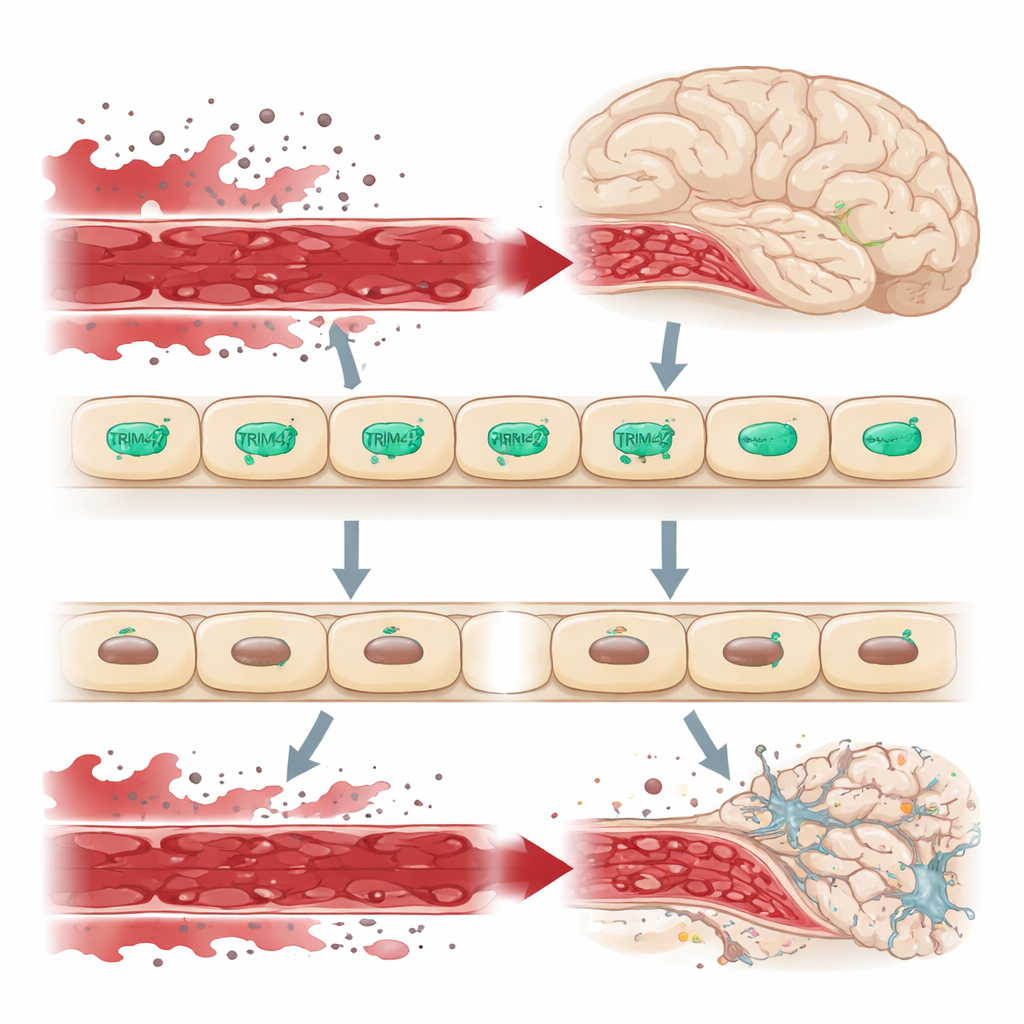
حارس عند حدود الدماغ
يُحمى الدماغ من دوران بقية الجسم بحاجز الدم–الدماغ، وهو بطانة محكمة من خلايا بطانية تتحكم بدقة فيما يمكن أن يدخل نسيج الدماغ. عندما يتسرب هذا الحاجز، تتسلل جزيئات ضارة من الدم إلى الدماغ، مسببة ضغطاً للخلايا العصبية والخلايا الداعمة ومساهمة في حالات مثل الخرف. أشارت دراسات جينية في مجموعات بشرية كبيرة إلى منطقة في الحمض النووي تحتوي على جين TRIM47 باعتبارها منطقة مخاطرة لمرض الأوعية الدموية الصغيرة الدماغية. يظهر TRIM47 نشاطاً خاصاً في الخلايا البطانية الدماغية، مما يوحي بأنه قد يكون حارساً مهماً لهذا الحاجز.
كيف يجهز TRIM47 الخلايا ضد الإجهاد التأكسدي
درس المؤلفون أولاً خلايا بطانية بشرية من الدماغ مزروعة في المختبر وخفضوا مستويات TRIM47 باستخدام تثبيط عبر الرنا. أدى ذلك إلى تغييرات واسعة في نشاط الجينات، وكان الشبكة الأكثر تأثراً تدور حول NRF2، المنظم الرئيسي للدفاعات المضادة للأكسدة في الخلية. في الظروف الطبيعية، يُكبَح NRF2 بواسطة بروتين آخر، KEAP1، الذي يوجِّهه نحو التحلل. أظهر الفريق أن TRIM47 يتصل بـ KEAP1 ويساعد على منع تحلل NRF2. بوجود TRIM47، يمكن أن يتراكم NRF2، وينتقل إلى النواة، ويشغّل جينات تزيل السموم من الجذور الحرة التفاعلية. عند فقدان TRIM47، تنخفض مستويات NRF2، وتقلّ فعالية جينات مضادات الأكسدة، وتصبح الخلايا البطانية أكثر عرضة للإجهاد التأكسدي.
من الأوعية المتسربة إلى مشاكل الذاكرة في الفئران
لمعرفة كيفية تجسيد هذه الآلية في دماغ حي، هندس الباحثون فئراناً تفتقر إلى جين Trim47 في أنحاء الجسم، وسلالة أخرى يمكن فيها حذف Trim47 فقط في الخلايا البطانية. طورت الحيوانات البالغة في كلا النموذجين مشاكل واضحة في التعلم المكاني والذاكرة، حيث فشلت في مهام مثل متاهة Y ومتاهة الماء لموريس بالرغم من حركة طبيعية. كشف فحص أدمغتهم أن الحاجز الدموي الدماغي أصبح متسرباً: تسربت ووسطات فلورية صغيرة وبروتينات دموية من الأوعية إلى الأنسجة المحيطة. تقلصت البروتينات «الختمية» الأساسية التي تشكل الوصلات المحكمة والوصلات اللاصقة بين الخلايا البطانية، خاصة Claudin-5 وOccludin. تنبهت الخلايا النجميّة الداعمة المجاورة، وهي خلايا على شكل نجم تتفاعل سريعاً مع الإصابة، رغم وجود علامات طفيفة فقط على التهاب واسع أو فقدان الخلايا العصبية في هذه المرحلة.
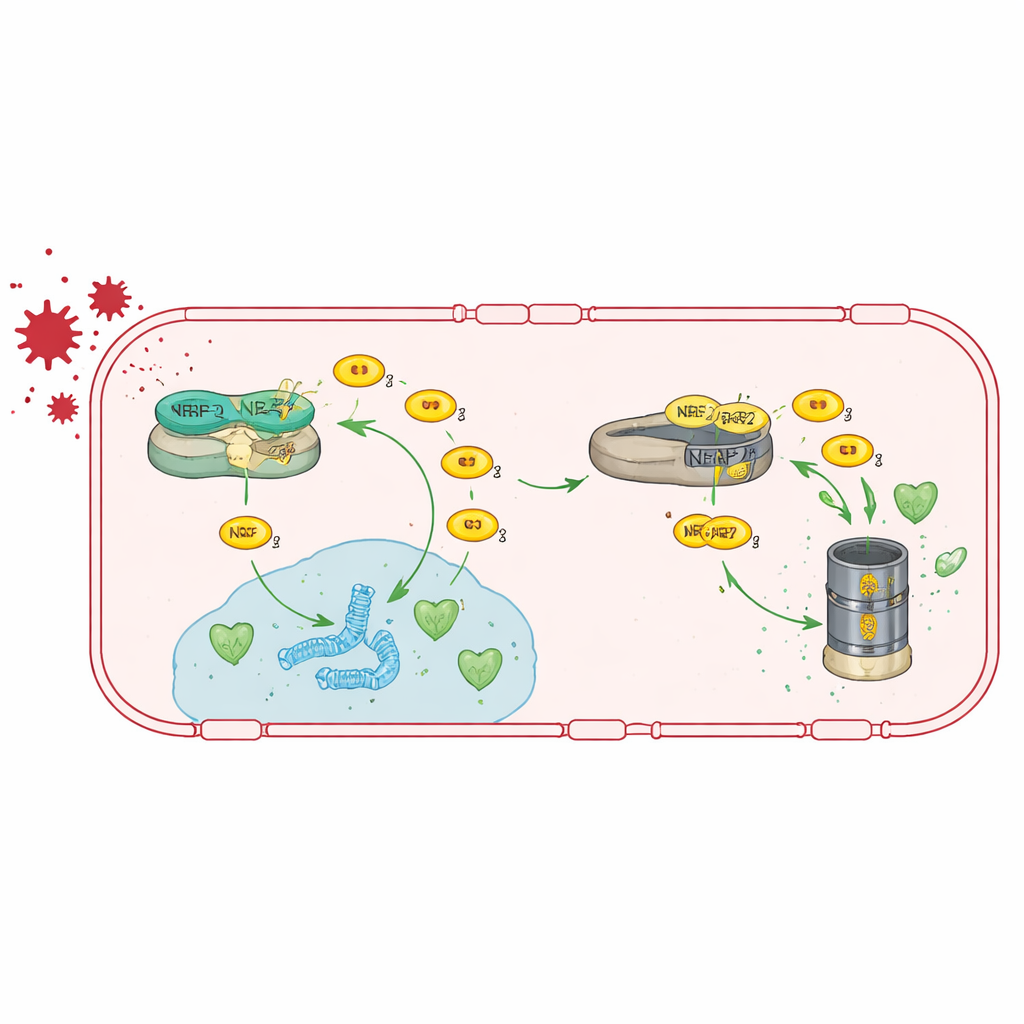
إعادة تشغيل مسار مضادات الأكسدة
لأن TRIM47 يعمل أساساً عبر تعزيز نشاط NRF2، اختبر الفريق ما إذا كان بإمكانهم تجاوز فقدانه بتنشيط NRF2 مباشرة. أطعمت الفئران الناقصة Trim47 نظاماً غذائياً يحتوي على ثالثي-بيوتيلهيدروكينون (tBHQ)، مركب معروف بتثبيت NRF2 وتشغيل جيناته الهدف. أعاد هذا العلاج نشاط جينات مضادات الأكسدة في الخلايا البطانية الدماغية، وأعاد تعبير جينات الوصلات المحكمة باتجاه الطبيعي، وخفف من تسرب الحاجز الدموي الدماغي. اللافت أن ذلك أيضاً أعاد تطبيع تنبيه الخلايا النجمية وأنقذ أداء الحيوانات في اختبارات الذاكرة، مما يشير إلى أن تعزيز هذا المسار المضاد للأكسدة يمكن أن يعكس كل من المشاكل الوعائية والمعرفية، على الأقل في الفئران.
دلائل من دم الإنسان وما الذي سيأتي لاحقاً
لجسر تجاربهم على الفئران مع مرض الإنسان، حلل الباحثون بروتينات متعلقة بمسار NRF2 في عينات دم لآلاف الأشخاص الذين أجروا فحوصاً تصويرية بالرنين المغناطيسي للدماغ. ارتبطت مستويات عدة بروتينات منظَمة بواسطة NRF2 بعلامات تصويرية لمرض الأوعية الدموية الصغيرة، مثل توسع الفراغات المحيطة بالأوعية وتغيرات في المادة البيضاء. يدعم هذا الفكرة القائلة إن تغيرات إشارات TRIM47–NRF2 ذات صلة بالبشر، وليس فقط في نماذج حيوانية تجريبية، وأن هذه البروتينات قد تخدم كعلامات حيوية لشدة المرض أو تقدمه.
ماذا يعني هذا لصحة الدماغ
تجسّد هذه الدراسة TRIM47 كحارس جزيئي يساعد أوعية الدماغ على مقاومة الأذية التأكسدية عبر تثبيت نظام NRF2 المضاد للأكسدة. عندما يغيب TRIM47 أو يتضرر، يضعف الحاجز الدموي الدماغي، ويتراكم الضرر الطفيف في الدماغ، وتبدأ الذاكرة بالتراجع. يمكن لإعادة تنشيط مسار NRF2 أن تسد الثغرات في الحاجز وتستعيد الإدراك في الفئران، مما يسلط الضوء على محور الإشارة هذا كهدف علاجي واعد لأشكال الخرف الوعائي. ومع أن tBHQ نفسه غير مناسب كدواء للبشر، قد تساعد مركبات أكثر أماناً معززة لـ NRF2 أو استراتيجيات تحاكي الدور الوقائي لـ TRIM47 يوماً ما في الحفاظ على صحة الدماغ بتقوية أصغر أوعيته وأكثرها هشاشة.
الاستشهاد: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
الكلمات المفتاحية: مرض الأوعية الدموية الصغيرة الدماغية, الحاجز الدموي الدماغي, TRIM47, مسار NRF2, الخرف الوعائي