Clear Sky Science · ar
مسار بين الوحدات الفرعية ضروري للارتباط الدافِع بالانتروبيا والتعاونية السلبية للنيوكليوتيدات الحلقية في قناة HCN2
كيف تستشعر مفاتيح النسّاحة الصغيرة في القلب الإشارات الكيميائية
يعتمد كل دقّة قلب والعديد من إيقاعات الدماغ على قنوات مجهرية تُفتح وتُغلق في أغشية خلايانا. تُدعى هذه القنوات قنوات النسّاحة HCN، وتتحكّم بها ليس فقط الفولتية الكهربائية بل أيضًا جزيئات رسول صغيرة تُعرف بالنيوكليوتيدات الحلقية. يطرح هذا البحث سؤالاً بسيط المظهر لكن ذا آثار بعيدة: كيف ترتبط هذه الجزيئات الصغيرة بقناة HCN2 بطريقة منسقة، وكيف يمكن لعيوب طفيفة في تلك العملية أن تسهم في اضطرابات مثل الصرع؟
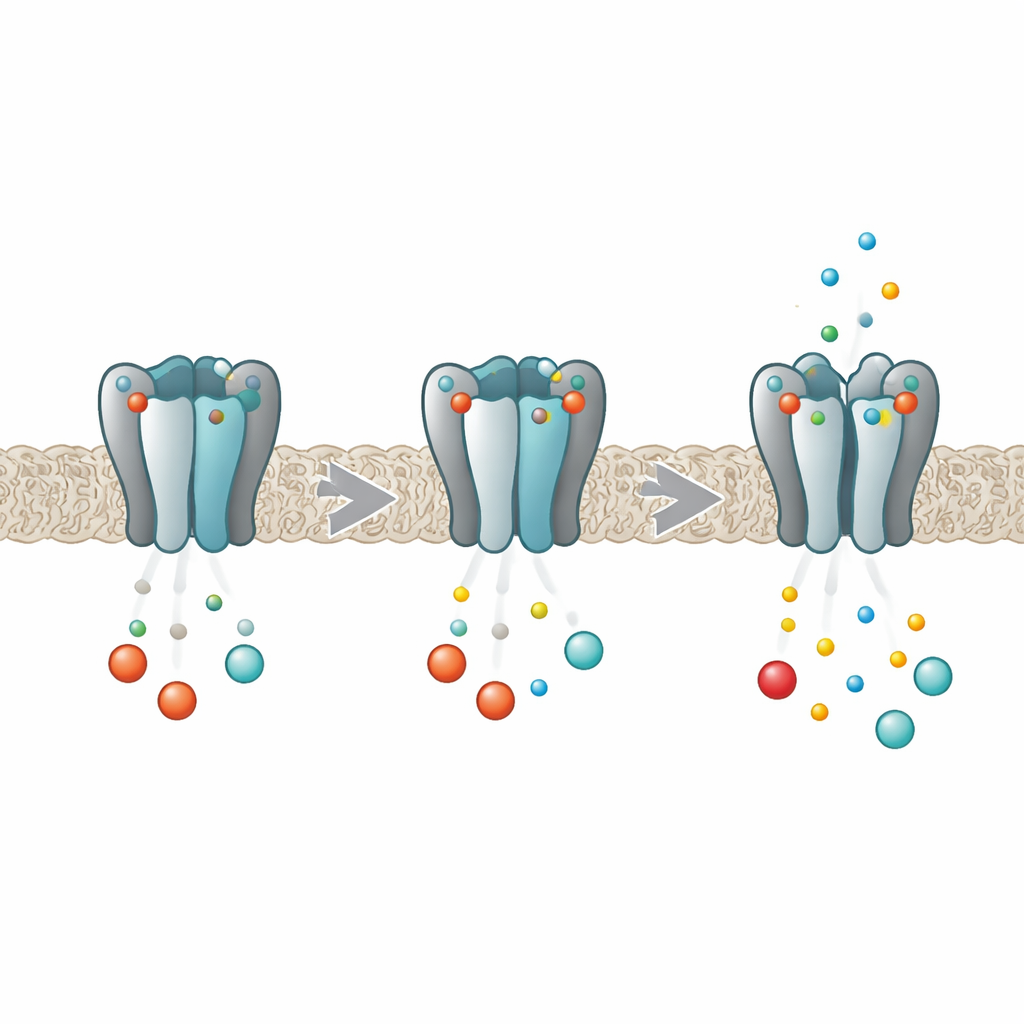
مُخَفِّف جزيئي لإيقاعات الجسم
تعمل قنوات HCN كمفاتيح تخفيف لشدة النشاط الكهربائي في خلايا القلب والدماغ. تتكوّن كل قناة من أربعة وحدات بروتينية متطابقة تشكل معًا مسامًا مركزية يتدفق من خلالها الأيونات. في عمق كل وحدة يوجد جيب قادر على التقاط النيوكليوتيدات الحلقية مثل cAMP وcGMP. عندما ترتبط هذه الرسل، تسهّل فتح المسام، مما يعزز التيار النسّاحي. أظهرت دراسات سابقة أن في النسخة HCN2، لا يحدث الارتباط بشكل مستقل في كل جيب؛ بل تؤثر المواقع الأربعة في بعضها البعض بحيث يكون الجزيء الأول أكثر قابلية للارتباط من الجزيئات اللاحقة، سلوك يعرف بالتعاونية السلبية. هدف العمل الجديد إلى كشف كيفية تواصل الوحدات الأربع مع بعضها خلال هذه العملية.
وحدات فرعية تشعر بجيرانها
جمع الباحثون بين محاكاة حاسوبية وقياسات مخبرية على أجزاء معزولة من ذيول قناة HCN2. باستخدام محاكاة ديناميكيات جزيئية طويلة، راقبوا كيف ينحني ويرتعش الجزء الذيلِي للقناة — الجزء الذي يحتوي جيوب النيوكليوتيدات الحلقية وموصل الـC‑linker الذي يتصل بالمسام — عند ارتباط أعداد مختلفة من جزيئات cAMP أو cGMP. وجدوا أنه عندما يثبت رسول في وحدة فرعية واحدة، لم يقتصر تأثيره على تثبيت تلك الوحدة فقط. بل غيّر بدقة ثبات جيرانه، أحيانًا بجعلهم أكثر صلابة وأحيانًا أكثر مرونة، رغم أن الشكل العام للبروتين نادراً ما تغير. كانت هذه التأثيرات بين الجيران تعتمد على عدد المواقع المشغولة ومواقعها حول الحلقة، بما يتوافق مع ما يُتوقّع من التعاونية السلبية.
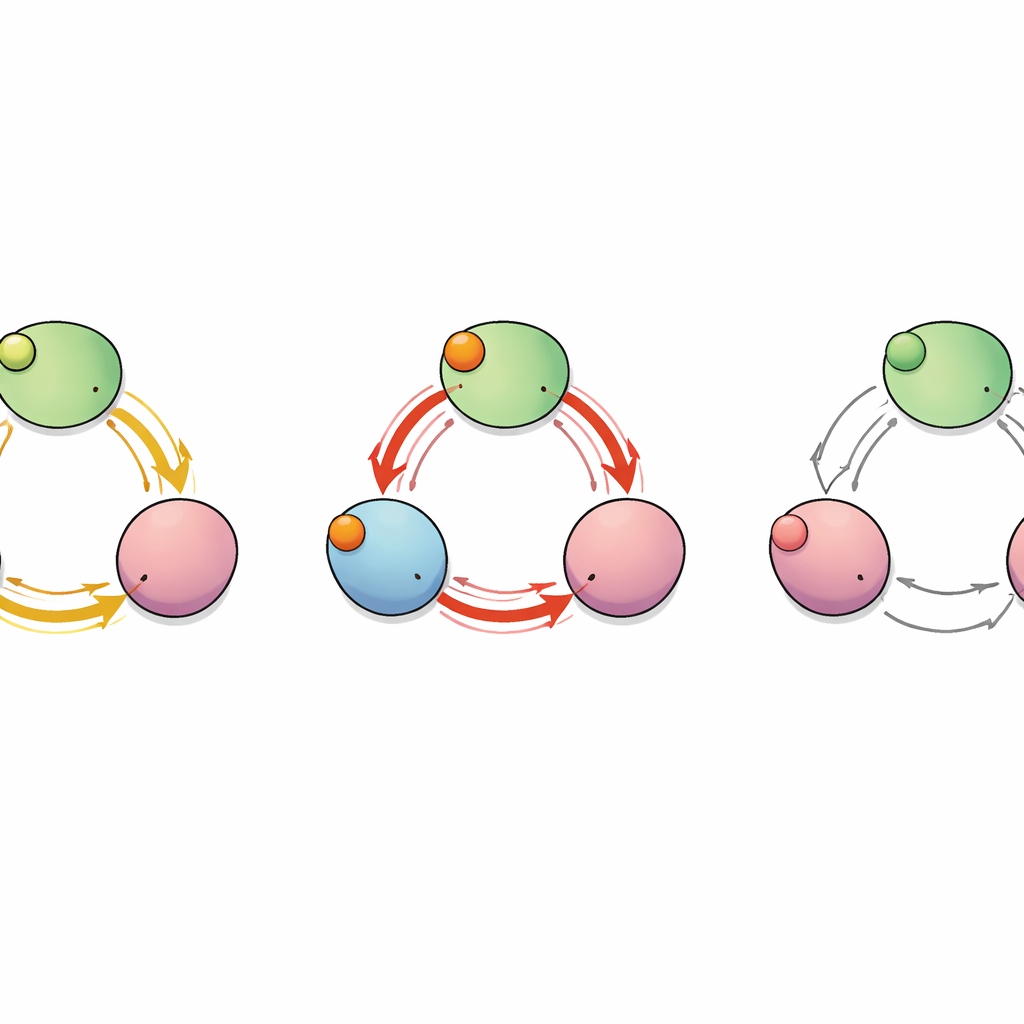
مسار مخفي بين الوحدات الفرعية
لمسح كيفية انتقال «إشارة» الارتباط عبر البروتين، اعتبر الفريق القناة شبكة من الأحماض الأمينية المتفاعلة. حسبوا أي البقايا تتحرك بتوافق خلال المحاكاة واستخدموا أدوات نظرية الرسوم لتحديد أقصر وأنجع مسارات الاتصال من جيوب الارتباط إلى قطع الـC‑linker التي تسيطر على المسام. كشفت هذه التحليلية عن عدة مسارات ممكنة، لكن اثنين برزا: أحدهما يبقى داخل وحدة فرعية مفردة والآخر يقفز من وحدة فرعية إلى جارتها. على طول هذا المسار بين الوحدات الفرعية، عملت بقايا واحدة — حمض الجلوتاميك في الموضع 488 (E488) — كعقدة حرجة تمر عبرها العديد من أقصر المسارات، ما يوحي بأنها قد تكون نقطة ترحيل رئيسية للتعاونية في الارتباط.
طفرات تقطع المحادثة
ثم توجه المؤلفون إلى تجارب مع ذيول القنوات المنقّاة لاختبار أهمية هذا المسار. غيّروا E488 والبيروتيين المجاور تيروزين 459 (Y459)، الذي يقع على الوحدة الفرعية المجاورة حيث يصل المسار. باستخدام قياس تشتّت الضوء الديناميكي، أكدوا أن البروتينات المتحولة لا تزال تتجمع في مركبات مكونة من أربع وحدات، لكنها لم تعد تظهر التضييق القوي الناتج عن الرابطة بين الوحدات كما في البروتين الطبيعي. كشفت المعايرة الحرارية المساواة، التي تتتبّع الحرارات الصغيرة للارتباط، تغيرًا أكبر: أظهر HCN2 البري النوع حدثي ارتباط مميزين، خطوة عالية الألفة مدفوعة أساسًا بزيادة في الانتروبيا (زيادة في الحركة الداخلية)، تلتها ثلاث خطوات أقل ألفة. بالمقابل، أظهر المتحورات عند E488 أو Y459 وضع ارتباط واحدًا فقط بمستوى ألفة متواضع، خالٍ من هذا التعزيز الانتروبي المفيد وفقدان سمة التعاونية السلبية.
لماذا تهم تغيّرات الانتروبيا الطفيفة
بتجميع هذه الأجزاء، يرسم البحث صورة لقناة HCN2 كحلقة دينامية من أربع وحدات فرعية متصلة عبر «مسارات محادثة» محددة. عندما يرتبط النيوكليوتيد الحلقِي الأول، يضبط حركات أجزاء بعيدة من الحلقة عبر E488 وY459، مما يجعل أحداث الارتباط اللاحقة أقل ملاءمة ويضبط استجابة المسام. لا يُدفع هذا التأثير بتغيّرات هيكلية كبيرة بل بتحولات في المرونة الداخلية — تغييرات في الانتروبيا غير مرئية في اللقطات الثابتة لكنها حاسمة للوظيفة. الطفرات التي تعطل البقايا الأساسية على طول هذا المسار بين الوحدات تخفض المحادثة، تلغي التعاونية السلبية، وترتبط بأمراض مثل الصرع العام مجهول السبب. للقراء العاديين، الخلاصة هي أن المفاتيح الحياتية في القلب والدماغ تعتمد على «همسات» جزيئية متناغمة بين وحدات البروتين، وفهم هذه الهمسات يساعد على تفسير الإيقاعات الطبيعية وما يحدث عندما تختل.
الاستشهاد: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
الكلمات المفتاحية: قناة أيونية HCN2, ارتباط النيوكليوتيدات الحلقية, تعاونية سلبية, اتصال جميعوستيري, طفرة الصرع