Clear Sky Science · ar
الحمض النووي الريبي الطويل غير المشفر P4HA2-AS1 يحفز التليف البيني الكلوي عبر ubiquitination من نوع K63 لبروتين ULK1 بوساطة TRIM32 واضطراب الالتهام الذاتي
لماذا يهم تندب الكِلى
يصيب مرض الكلى المزمن مئات الملايين من الناس حول العالم وغالبًا ما يتقدم بصمت حتى تصبح الغسيل الكلوي أو الزراعة الوسيلة الوحيدة للبقاء على قيد الحياة. في صلب هذا التدهور عملية تسمى التندب، حيث تُستبدل أنسجة الكِلى الطبيعية تدريجيًا بمادة صلبة غير وظيفية. يطرح هذا البحث سؤالًا بسيطًا لكنه حاسم: ما المحولات الجزيئية داخل خلايا الكِلى التي تدفعها نحو هذا التندب الضار، وهل يمكن إعادة ضبط هذه المحولات؟
مفتاح RNA مخفي في خلايا الكِلى
تقوم كِلياتنا بترشيح الدم عبر شبكات معقدة من الأنابيب الدقيقة. عند إصابة هذه الأنابيب بسبب انسداد تدفق البول أو ارتفاع سكر الدم أو فقدان التروية فجأة، يمكن أن تستجيب بوضع نسيج ندبي بين الخلايا. بحث الباحثون في كِلى الفئران المصابة بأنواع مختلفة من الضرر وقارنوها بكِلى سليمة باستخدام تسلسل الحمض النووي الريبي، وهي تقنية تكشف عن الجينات النشطة. اكتشفوا أن جزيئًا قليلاً المعروف باسم P4HA2-AS1، وهو حمض نووي ريبيل طويل غير مشفر لا يُنتج بروتينًا، كان مرتفعًا باستمرار في الكِلى المصابة والمشكِّلة للندوب وفي خلايا كِلوية بشرية موضوعة تحت إجهاد في المختبر. وُجد هذا الحمض النووي الريبي بشكل أساسي في الجزء المملوء بالسائل داخل الخلايا، مما يوحي بأنه قد يتحكم في بروتينات أخرى هناك. 
خفض مستوى الـ RNA لحماية الكِلى
لاختبار ما إذا كان P4HA2-AS1 مجرد مرافق أم محرك نشط للضرر، خفّض الفريق مستوياته في الفئران وفي خلايا كلوية بشرية مزروعة. في نموذج فأري راسخ يُربط فيه الحالب لإحداث انسداد طويل الأمد، أدت خفضات هذا الحمض النووي الريبي عبر إيصال فيروسي مستهدف إلى تراجع العديد من علامات التندب: بقيت الأنابيب أكثر سلامة، وانخفضت كميات الكولاجين وبروتينات الندبة الأخرى بين الخلايا، وتحسنت مؤشرات وظيفة الكِلى في الدم. في أطباق الخلايا البشرية، أدت تقليصات مستويات P4HA2-AS1 أيضًا إلى تراجع استجابة الإشارة القوية المسببة للتندب TGF‑β، مما أسفر عن إنتاج أقل للفايبروبكتين والكولاجين وعوامل أخرى محفزة للتليف. أظهرت هذه التجارب أن هذا الـ RNA ليس مجرد علامة للضرر بل يغذي عملية التندب بنشاط.
الالتهام الذاتي: من التنظيف إلى الضرر
سأل الباحثون بعد ذلك كيف يسبب هذا الـ RNA الضرر. أشارت بيانات التعبير الجيني والتصوير إلى الالتهام الذاتي، نظام إعادة التدوير الخلوي الذي يكسر البروتينات والعضيات التالفة. في الظروف الطبيعية، الالتهام الذاتي عملية مفيدة للحفاظ على الخلية، لكن عندما يُفعَّل بشدة ولمدة طويلة يمكن أن يدفع الكِلى المصابة نحو إصلاح خاطئ وتندب. في الخلايا الكلوية المجهدة، عزّز P4HA2-AS1 تدفّق المواد عبر مسار الالتهام الذاتي، مما أدى إلى تراكم الحويصلات المتعلقة بإعادة التدوير. عند حظر الـ RNA، عاد هذا النشاط المفرط إلى مستوى أقرب إلى الطبيعي، سواء في الخلايا أو في كِلى الفئران المصابة بالانسداد. كانت الفئران التي تفتقر إلى ULK1، الإنزيم المركزي لبدء الالتهام الذاتي، محمية أيضًا من التندب، وفي هذه الحيوانات لم يعد بإمكان زيادة التعبير عن P4HA2-AS1 تفاقم الضرر، مما يربط تأثيرات الـ RNA بقوة بهذا المسار.
سلسلة جزيئية ثلاثية الأجزاء
تعمق الفريق أكثر مستخدمًا تقنيات صيد بيوكيميائية لتحديد البروتينات التي ترتبط فعليًا بـ P4HA2-AS1. برز بروتين واحد: TRIM32، إنزيم يصنّف بروتينات أخرى بعلامات جزيئية صغيرة تُدعى يوبكويتين. يرتبط الـ RNA بـ TRIM32 ويَقيه من التحلل، ما يرفع مستوياته داخل الخلايا الكلوية. بدوره، يضيف TRIM32 المستقر نوعًا محددًا من سلاسل اليوبيكويتين إلى ULK1. بدلًا من إرسال ULK1 للتدمير، تعمل هذه السلسلة كتعزيز لقدرة ULK1 على تحفيز الالتهام الذاتي. عندما أزال العلماء TRIM32 في الفئران أو سكّتوه في الخلايا الكلوية، انخفض كل من التندب والالتهام الذاتي المفرط. إعادة إدخال TRIM32 في خلايا كان P4HA2-AS1 قد حُظر فيها أعادت جزئيًا استجابة التندب، ما يظهر أن هذا الإنزيم حلقة وسطى رئيسية في السلسلة. 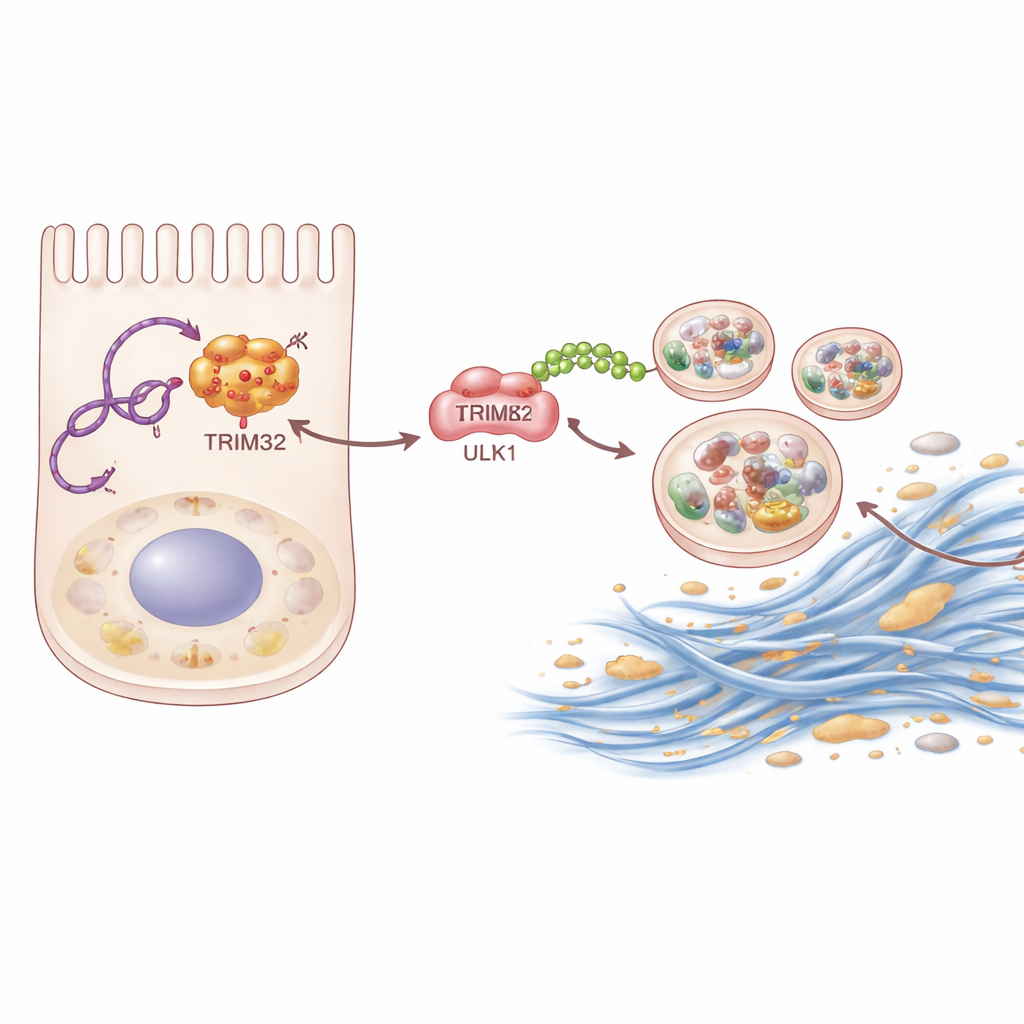
طرق جديدة نحو كِلى أقل صلابة
تظهر النتائج مجتمعة مسارًا جزيئيًا غير معروف سابقًا يربط بين الحمض النووي الريبي الطويل غير المشفر، تعليم البروتين بالعلامات، وإعادة تدوير الخلية بتراكم نسيج الندب الكلوي. في الكِلى المصابة، يرتفع P4HA2-AS1، يؤمن TRIM32، ينشط ULK1 بشكل مفرط، ويدفع الالتهام الذاتي إلى ما وراء نطاقه المفيد، مما يشجع تراكم بروتينات ليفية وفقدان الوظيفة. للمختصين غير المتخصصين، الخلاصة أن تندب الكِلى ليس صندوقًا أسود حتميًا: إنه يُدفع بواسطة محولات محددة قد تكون قابلة للعلاج. قد يوفر استهداف محور P4HA2-AS1–TRIM32–ULK1 — عن طريق خفض هذا الـ RNA المُشاغب أو ترويض TRIM32 أو ضبط نشاط ULK1 — يومًا ما علاجات جديدة لإبطاء أو منع تقدم مرض الكِلى المزمن.
الاستشهاد: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
الكلمات المفتاحية: مرض الكلى المزمن, تليف كلوي, الالتهام الذاتي, الحمض النووي الريبي الطويل غير المشفر, أنابيب الكِلى