Clear Sky Science · ar
السمنة تضعف التكوّن المنوي عبر فرط موت الخلايا بالحديد في خلايا لايدغ الناتج عن إكسوسومات الكبد حاملة miR-122-5p
لماذا الوزن والخصوبة مرتبطان
عادة ما تُناقش السمنة من منظور أمراض القلب والسكري، لكنها قد تقوض أيضًا خصوبة الذكور بهدوء. تكشف هذه الدراسة على الفئران عن طريقة مفاجئة يمكن بها للنظام الغذائي الغني بالدهون أن يخفض التستوستيرون ويضر بإنتاج الحيوانات المنوية: الكبد يرسل "فقاعات رسائل" صغيرة إلى الدم تُحدث نوعًا خاصًا من موت الخلايا في الخلايا المُنتِجة للهرمون في الخصية. فهم هذا التواصل الخفي من الكبد إلى الخصية قد يساعد في تفسير سبب معاناة الرجال ذوي الوزن الزائد غالبًا من انخفاض التستوستيرون والعقم، وقد يشير إلى أهداف علاجية جديدة.
رسائل خفية بين الأعضاء
تتواصل أعضاؤنا باستمرار مع بعضها عبر الهرمونات ووسائط كيميائية أخرى. أحد أشكال هذا التواصل يستخدم الإكسوسومات—فقاعات بحجم النانومتر تُفرزها الخلايا وتحمل دهونًا وبروتينات ومادة وراثية. بدأ الباحثون بتغذية الفئران إما نظامًا غذائيًا طبيعيًا أو نظامًا عالي الدهون أدى إلى السمنة ومقاومة الأنسولين وسوء التحكم في السكر بالدم. كانت خصى الفئران السمنة أصغر وأقل نشاطًا: انخفضت أعداد الحيوانات المنوية ومستويات التستوستيرون وحجم وعدد الأنابيب المنتجة للحيوانات المنوية. عندما فحص الفريق مؤشرات الخلايا الأساسية في الخصية، وجدوا خلايا لايدغ منتجة للتستوستيرون أقل وخلايا منوية مبكرة ومتأخرة أقل، مما أكد أن خط إنتاج الحيوانات المنوية بأكمله تضرر. 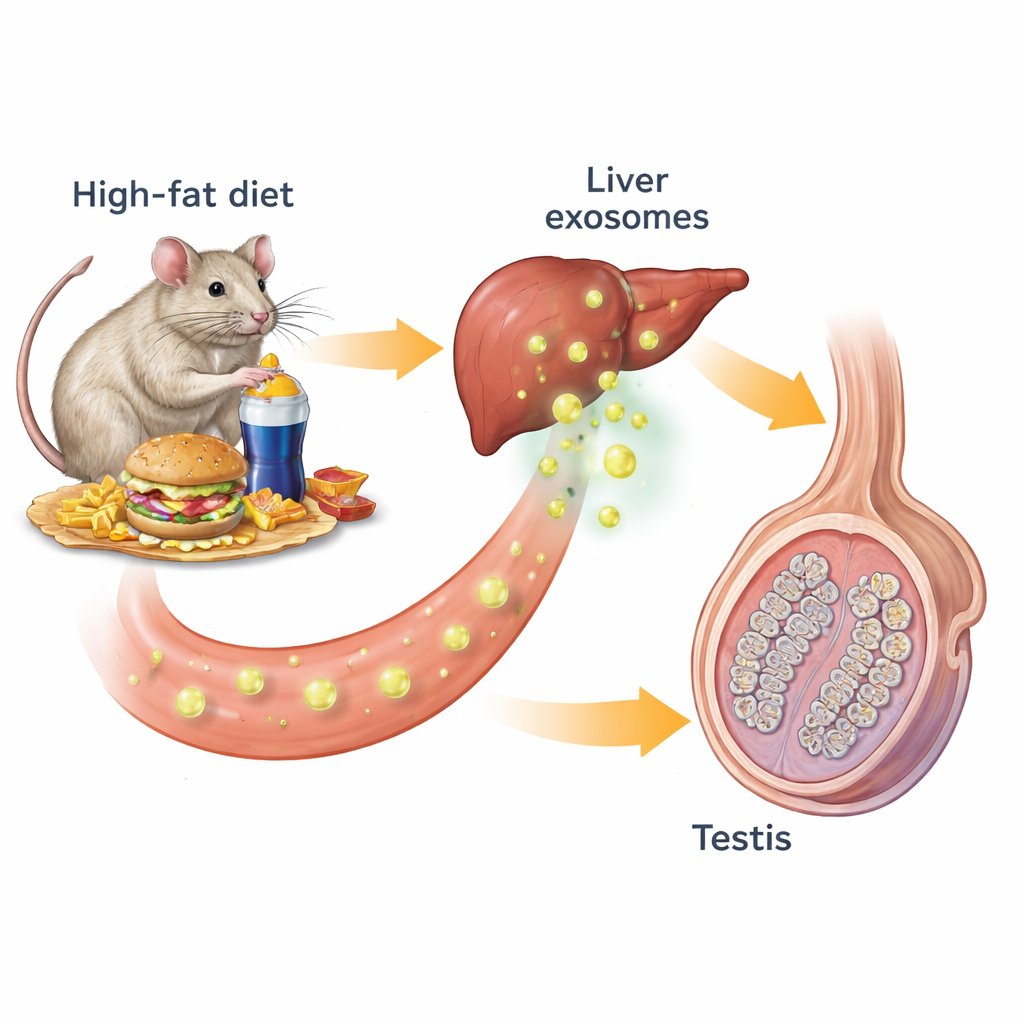
الإكسوسومات تنشر الضرر
لاختبار ما إذا كانت الإكسوسومات الدائرة تساهم في هذا الضرر، نقّى العلماء الإكسوسومات من دم الفئران السمنة والنحيلة. كانت حقن الإكسوسومات المأخوذة من الفئران السمنة في فئران سليمة ونحيلة كافية لتكرار العديد من المشكلات: أظهرت المستقبلات علامات اضطراب أيضي، وانخفضت مستويات التستوستيرون، وتدهورت أعداد الحيوانات المنوية وبنية الخصية. حجب إفراز الإكسوسومات في الفئران السمنة بدواء يسمى GW4869 عكس هذه التغيرات إلى حد كبير، فأعاد أعداد الحيوانات المنوية ومستويات التستوستيرون وبنية الخصية الطبيعية. تشير هذه النتائج إلى أن الإكسوسومات في مجرى الدم ليست مجرد مراقبين سلبيين؛ بل تحمل بنشاط إشارات ضارة من السمنة إلى الجهاز التناسلي.
شكل سام من موت الخلايا
ثم نظر الفريق في ما تفعله الإكسوسومات بالضبط بخلايا لايدغ. ركزوا على الفيروبتوزيس، وهو شكل موت خلوي مدفوع بالحديد يتميز بتراكم الحديد، والضرر التأكسدي للدهون، وإصابة الميتوكوندريا—محطات الطاقة في الخلية. في الفئران السمنة وفي فئران سليمة أُعطيت إكسوسومات من فئران سمنة، أظهرت الخصى مستويات أعلى من الحديد والمالونالدهيد، وهو نواتج أكسدة للدهون، وكذلك إصابة ميتوكوندريا واضحة تحت المجهر الإلكتروني. علاج الفئران السمنة بمركب يعيق الفيروبتوزيس، Ferrostatin-1، حافظ على خلايا لايدغ، وزاد التستوستيرون وأعداد الحيوانات المنوية، وحسّن صحة الميتوكوندريا. في مزرعة الخلايا، حمى نفس الدواء خلايا لايدغ المعزولة من الموت والإجهاد التأكسدي الناجم عن إكسوسومات من حيوانات سمنة. تُظهر هذه التجارب معًا أن الفيروبتوزيس هو الرابط الرئيسي بين السمنة وفشل إنتاج التستوستيرون.
رسالة الكبد ومفتاح SCD2
لتعقب الرسالة داخل الإكسوسومات، سَلَّل الباحثون حمولتها من الحمض النووي الريبي الصغير ووجدوا أن ميكروRNA معين، miR-122-5p، زاد بشدة في إكسوسومات الفئران السمنة. كان هذا الميكروRNA وفيرًا بشكل خاص في الكبد وفي الإكسوسومات المشتقة من الكبد، ويمكن تتبع تلك الإكسوسومات الكبدية وهي تسافر إلى الخصيتين. عندما خُفضت مستويات miR-122-5p تجريبيًا في الإكسوسومات، باتت خلايا لايدغ أقل عرضة للفيروبتوزيس وتحسّن إنتاج التستوستيرون، رغم أن الحيوانات ظلت محكومة بخلل أيضي. أظهرت اختبارات إضافية أن miR-122-5p يثبط مباشرة جينًا يُدعى Scd2، الذي يساعد في تحويل أنواع معينة من الدهون إلى أشكال تحمي الخلايا من الضرر التأكسدي. جعل تقليل Scd2 خلايا لايدغ أكثر عرضة للفيروبتوزيس وخفض التستوستيرون، في حين أن تعزيز Scd2 في الفئران السمنة أعاد جزئيًا مستويات الهرمون وإنتاج الحيوانات المنوية وبنية الميتوكوندريا. 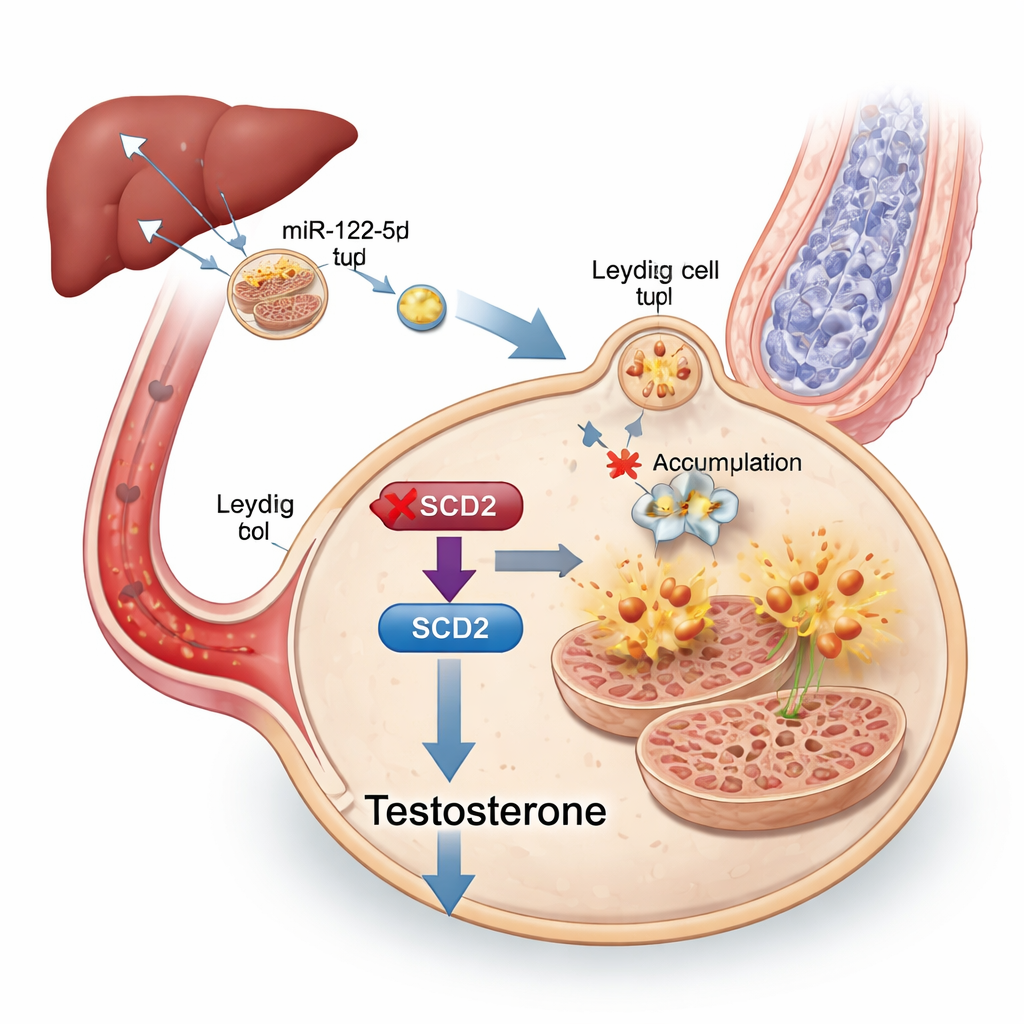
ماذا يعني ذلك لصحة البشر
بعبارات بسيطة، تُظهر هذه الدراسة أن النظام الغذائي العالي بالدهون يمكن أن يدفع الكبد لتحميل الإكسوسومات بوفرة مفرطة من miR-122-5p. تنتقل هذه الإكسوسومات عبر الدم إلى الخصيتين، حيث يطفئ الميكروRNA مفتاح Scd2 المتعلق بالتعامل مع الدهون في خلايا لايدغ. بدون Scd2، تتراكم في هذه الخلايا أضرار تأكسدية مدفوعة بالحديد، وتدخل في الفيروبتوزيس، وتنتج كمية أقل من التستوستيرون، وفي النهاية تدعم عددًا أقل من الحيوانات المنوية الصحية. على الرغم من أن هذا البحث أُجري على الفئران ولا بد من تأكيده لدى البشر، فإنه يحدد الإكسوسومات الكبدية، miR-122-5p، الفيروبتوزيس، وScd2 كعلامات حيوية واعدة وكمستهدفات دوائية محتملة لعلاج العقم الذكري المرتبط بالسمنة—ويؤكد سببًا آخر يجعل الأنظمة الغذائية عالية الدهون على المدى الطويل قد تضعف الصحة الإنجابية بهدوء.
الاستشهاد: Wang, N., Zhang, B., Chen, T. et al. Obesity impairs spermatogenesis via Leydig cell ferroptosis induced by liver-derived exosomal miR-122-5p. Commun Biol 9, 318 (2026). https://doi.org/10.1038/s42003-026-09612-z
الكلمات المفتاحية: السمنة والخصوبة لدى الذكور, التستوستيرون, الإكسوسومات, خلايا لايدغ, فرط الموت الخلوي بالحديد (فيروبتوزيس)