Clear Sky Science · ar
إنزيم إزالة ميثلة الهيستون KDM7A ينظّم سلبياً استقطاب البلعمية الليفية وتقدّم تليف الرئة
لماذا يهم تندّب الرئتين الجميع
عندما تتكوّن ندوب عنيدة في الرئتين، تصبح عملية التنفّس معاناة يومية. هذه الحالة المعروفة بتليف الرئة تصيب ملايين الناس ولا يوجد لها علاج شافٍ حالياً — هناك فقط أدوية تبطئ الضرر. في هذه الدراسة، يكشف الباحثون عن "مكبح" جزيئي مخفٍ داخل خلايا جهاز المناعة تُدعى البلعميات يساهم في كبح تندّب الرئة. فهم هذا المكبح قد يفتح الباب لعلاجات جديدة ليس لتليف الرئة فقط، بل وربما لأمراض أخرى تترافق فيها الندوب الضارة والالتهاب الجامح.
قصة خلايا مناعية متحوّلة الشكل
البلعميات هي خلايا مناعية في الصفوف الأمامية تَجوب الأنسجة، تزيل المخلفات وتساعد على إصلاح التلف. لكنها أيضاً خلايا متحوّلة: في بعض الحالات تصبح محارِبة مُحرِّضة للالتهاب، وفي حالات أخرى تتحوّل إلى مصلحَات قد تدفع لتكوّن الندب. هناك نوع معين من البلعمية المحفِّز للتليف، يُسمى البلعمية الموالية للتليف (Fib-Mac)، مرتبط بشدة بتليف الرئة. تنتج هذه الخلايا جزيئات تنشّط الخلايا الليفية التي تفرز كميات زائدة من الكولاجين ومكونات المصفوفة الأخرى، مما يقسّي الرئة تدريجياً. أراد المؤلفون معرفة كيف تقرّر "إعدادات" الجينات داخل البلعمية إن كانت ستصبح هذه الخلايا الخطرة Fib-Mac أم تبقى في حالات أكثر توازناً وحماية.
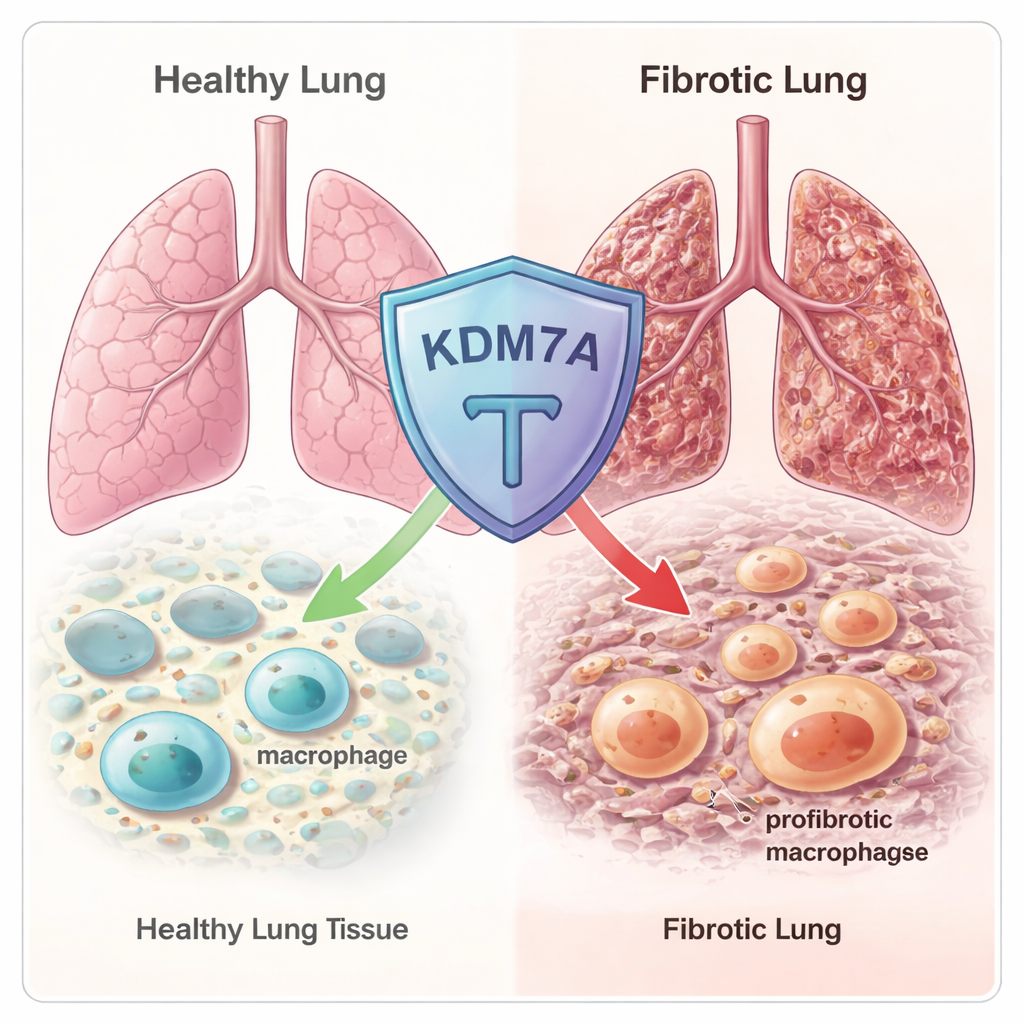
مكبح إيبيجينيتيكي مخفي في الجينوم
بدأ الفريق بمسح مئات المنظّمات الإيبيجينيتيكية المعروفة — البروتينات التي تضبط إحكام تغليف الحمض النووي وما تُفعّله أو تُطفئه من جينات. باستخدام تسلسل الرنا في كل من بلعميات بشرية وفأرية، وجدوا أن إنزيمًا يدعى KDM7A يُفعّل بقوة عندما تُدفع البلعمية نحو حالة شبيهة بالالتئام والليف. KDM7A هو "مزيل ميثلة الهيستون": يزيل وسمًا كيميائيًا معينًا من بروتينات الهيستون التي يلتفّ حولها الحمض النووي. هذا النمط ألمح إلى أن KDM7A قد يعمل كمكبح تغذوي راجع، يُفعّل تماماً عندما تبدأ البلعمية في الانجراف نحو هوية محفِّزة للندب.
لاختبار ذلك، استخدم الباحثون فئراناً تفتقر إلى جين Kdm7a وحفّزوا إصابة رئوية بالعقار الكيميائي المسمى بليوميسين، وهو نموذج معياري لتليف الرئة. في المراحل المبكرة بعد الإصابة، بدا نسيج الرئة مماثلاً في الحيوانات الطبيعية وتلك الناقصة Kdm7a. لكن بعد ثلاثة أسابيع، أظهرت الفئران المفقودة Kdm7a تندبًا أوسع بكثير وانهيار الحويصلات الهوائية الدقيقة ودرجات Ashcroft أعلى تقيس شدة التليف. كانت الجينات المشاركة في إنتاج الكولاجين ومسارات أخرى متصلة بالتليف أكثر نشاطًا في هذه الفئران المعدّلة، مؤكدة أن فقدان Kdm7a يجعل الرئتين أكثر عرضة لتكوّن ندبات طويلة الأمد وضارة.
كيف يوجّه KDM7A البلعمية بعيدًا عن مصير محفّز للندب
باستخدام تسلسل الرنا أحادي الخلية، ركّز المؤلفون على خلايا الرئة الفردية من الفئران المصابة. اكتشفوا أنه في غياب Kdm7a، توسّع فئة بلعمية معينة في النسيج الداعم للرئة بشكل كبير وتبنّت توقيعاً قوياً لِـ Fib-Mac، مع التعبير عن جينات مثل Arg1 وSpp1 وTrem2. أظهرت تجارب أخرى في بلعميات مزروعة أن إزالة Kdm7a عزّزت جينات مؤشرات Fib-Mac وأعادت توصيل أيض الخلايا نحو مسارات تدعم إنتاج الكولاجين والنشاط المستمر. بعبارة أخرى، KDM7A عادة ما يقيّد كلّاً من البرامج الجينية والتمثيل الغذائي التي تدفع البلعمية إلى حالة مولّدة للتليف.
وبالغوص أعمق، حدّد الباحثون شريكًا رئيسيًا في هذا النظام المكبح: بروتين مستشعر يُسمى TLR8 يكتشف أجزاء من الرنا داخل الخلايا المناعية. وجدوا أن KDM7A يساعد في إبقاء جين Tlr8 مفعّلاً عن طريق إزالة وسم كيميائي قمعي (H3K27me2) من منطقة معزّزة قريبة من Tlr8. عندما تعطّل Kdm7a، تراكم هذا الوسم، وانخفضت مستويات Tlr8، وتكاثرت سمات Fib-Mac. إن تقليص Tlr8 مباشرة في البلعمية دفعها أيضاً نحو هوية ليفية، بينما تفعيل أو إفراط إنتاج TLR8 أعادها للخلف حتى عند غياب Kdm7a. هذا يضع مسار KDM7A–TLR8 في مركز دائرة جزيئية تحمي الرئتين من التندّب المفرط.
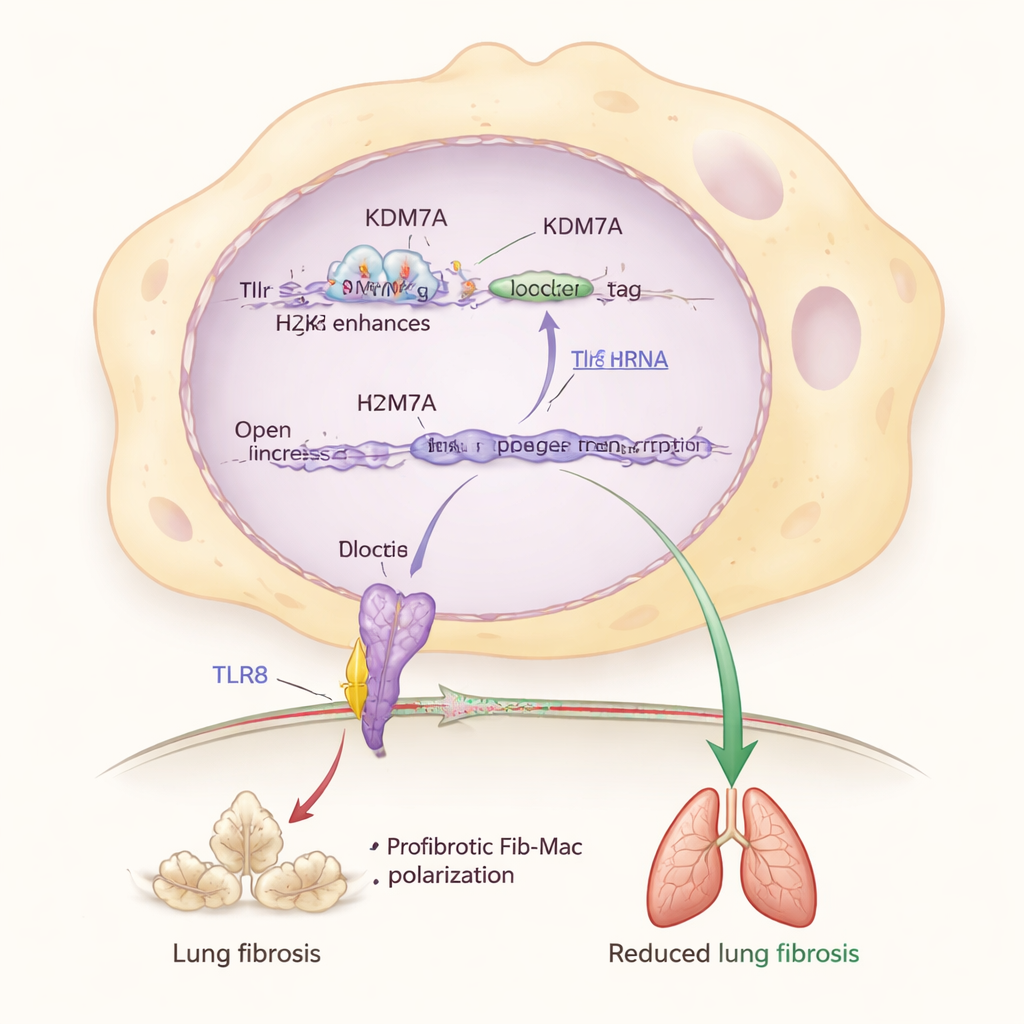
من الرئتين المتقدّمة في العمر إلى المرض البشري
لربط هذه النتائج بالبشر، فحص الفريق نسيج رئوي من مرضى يعانون من مرض رئوي ليفي. مقارنةً بنسيج الضابط غير المريض، احتوت الرئتان اللفيفيتان على عدد أكبر بكثير من البلعميات الحاملة لمؤشرات Fib-Mac، لكن هذه الخلايا نفسها أظهرت مستويات منخفضة بشكل ملحوظ من KDM7A وTLR8. وأكّد إعادة تحليل مجموعات بيانات أحادية الخلية موجودة لمرضى التليف الرئوي المجهول السبب هذا النمط: مع ارتفاع توقيعات Fib-Mac، انخفض تعبير KDM7A. كما نقّب الباحثون في أطلس فئري كبير ووجدوا أن تعبير Kdm7a وTlr8 في البلعميات ينخفض مع التقدّم في العمر لدى الذكور، مما يعكس المخاطر الأعلى للتليف الرئوي لدى الرجال الأكبر سنًا. يشير هذا إلى أن تضعف مكبح KDM7A–TLR8 المرتبط بالعمر والجنس قد يساعد في تفسير من هم الأكثر عرضة لتندّب رئوي شديد.
ماذا يعني هذا بالنسبة للعلاجات المستقبلية
بعبارة بسيطة، تُظهر هذه الدراسة أن جهازنا المناعي يحمل آلية أمان داخلية تمنع خلايا الإصلاح المفيدة من التحول إلى مفرطة النشاط وتصبح محرّكات لندوب دائمة. يعمل KDM7A، عبر TLR8، على منع البلعمية من الوقوع في وضع مولِّد للتليف وبالتالي يساعد على الحفاظ على نسيج رئوي مرن وفعال بعد الإصابة. عندما ينهار هذا النظام — عبر خسارة جينية أو التقدّم في العمر أو عوامل أخرى — تصبح البلعمية أكثر ميلاً لأن تكون "مكبّرات للندب" مما يزيد التليف سوءًا. من خلال كشف هذا المكبح الإيبيجينيتيكي، تشير الدراسة إلى استراتيجيات علاجية جديدة: أدوية تعزّز نشاط KDM7A أو تحاكي تأثيراته أو تنشّط TLR8 بعناية قد تكمل يوماً ما العلاجات المضادة للتليف الحالية وتوفر حماية أفضل ضد التندّب الرئوي التقدّمي والمحدود للحياة.
الاستشهاد: Funagura, N., Koga, T., Etoh, K. et al. Histone demethylase KDM7A negatively regulates fibrotic macrophage polarization and lung fibrosis progression. Commun Biol 9, 309 (2026). https://doi.org/10.1038/s42003-026-09610-1
الكلمات المفتاحية: تليف رئوي, البلعميات, علم التوارث الخارجي (الإيبيجينيتيكس), KDM7A, TLR8