Clear Sky Science · ar
التعرف على الغليكوليبيد والارتباط بواسطة Siglec-6 يعتمد على تداخلات مع غشاء الخلية
كيف تميز خلايانا الصديق من العدو
الجهاز المناعي يمسح خلايانا باستمرار، ليقرر متى يظل هادئًا ومتى يهاجم. جزء أساسي من هذه المراقبة يتضمن التعرف على الهياكل السكرية على أسطح الخلايا. تكشف هذه الدراسة أن مستقبلًا مناعيًا بشريًا يُدعى Siglec-6 لا يستخدم تلك السكريات فقط، بل يعتمد أيضًا على غشاء الخلية المحيط لاتخاذ قرارات ارتباط دقيقة بشكل استثنائي. قد يساعد هذا الأسلوب غير الاعتيادي في تفسير كيفية ضبط أجسامنا للإشارات المناعية ويفتح طرقًا جديدة للعلاجات المستهدفة.
حارس يستشعر السكريات على الخلايا المناعية
تنتمي عائلة السيغليكيات (Siglecs) إلى مستقبلات تقع على الخلايا المناعية وتتعرف على السكريات المحتوية على حمض السياليك، مما يساعد الجهاز المناعي على التمييز بين «الذاتي» و«غير الذاتي». تعتمد معظم السيغليكيات على بقاعدة بنيوية موحدة ومحفوفة بالحفاظ — حمض أميني أرجينين — لالتصاقها بهذه السكريات. إذا أزيل هذا الأرجينين، يفشل الارتباط عادةً. ومع ذلك، يُعد Siglec-6 شاذًا: أظهرت أعمال سابقة أنه قد يستمر في الارتباط ببعض الدهون الحاملة للسكريات حتى عند طفرته لهذا الأرجينين الأساسي. هدفت الدراسة الجديدة إلى كشف كيفية تمكن Siglec-6 من كسر هذه القاعدة الظاهرة وما يعنيه ذلك لدوره على خلايا البدينة وخلية الذاكرة البائية وخلايا المشيمة البشرية.
الدهون الخاصة التي يبحث عنها Siglec-6
على أسطح الخلايا، يمكن عرض السكريات على البروتينات والدهون. تركز هذه الدراسة على مجموعة من الدهون الحاملة للسكر تُدعى الغانغليوسيدات، لا سيما ثلاثة أنواع مترابطة وثيقة تُسمى GM1 وGM2 وGM3. كلها تُظهر رؤوسًا واحدة مكفوفة بحمض السياليك بارزة من الغشاء. أظهرت تجارب سابقة أن Siglec-6 يرتبط بقوة بـ GM1 عندما تكون جزءًا من غشاء، لكنه يرتبط بالكاد بـ GM2 أو GM3، مع أن رؤوس سكرياتها متشابهة جدًا. باستخدام محاكاة حاسوبية مفصلة لأغشية واقعية، أكد الباحثون أن حمض السياليك في GM1 وGM3 مكشوف وقابل للوصول بالمثل. بعبارة أخرى، الوصول الفيزيائي البسيط ليس سبب تميز GM1. بدلًا من ذلك، برزت سكر إضافي في طرف GM1 — الجالاكتوز النهائي — كعنصر حاسم يساعد في تموضع Siglec-6 بشكل صحيح مقابل الغشاء.
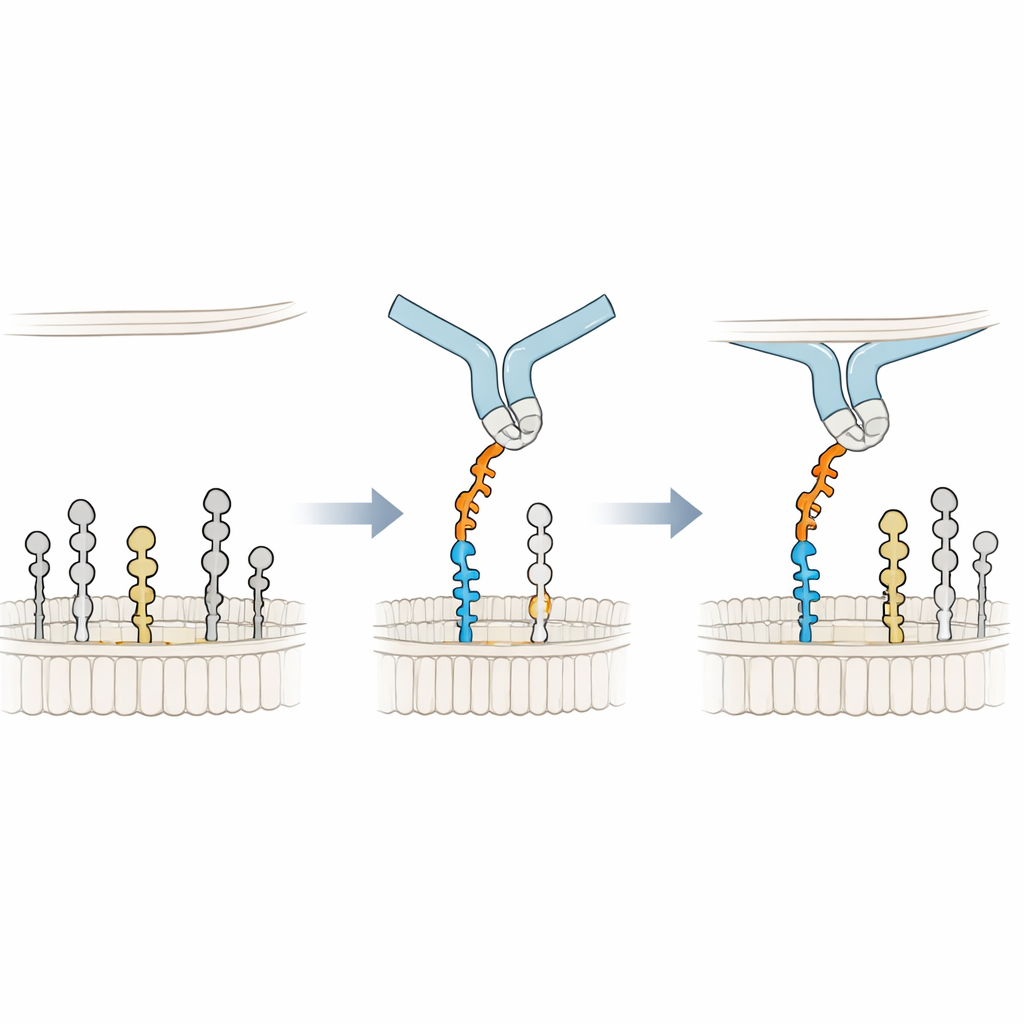
الاستناد إلى الغشاء للحصول على قبضة أفضل
لفهم آلية الارتباط بتفاصيل ذرية، بنى الباحثون نماذج ثلاثية الأبعاد لـ Siglec-6 وهو يتفاعل مع GM1 في غشاء وأجروا محاكاة طويلة للديناميكا الجزيئية. وجدوا أن Siglec-6 لا يزال يستخدم الأرجينين الكلاسيكي (Arg122) لملاقاة حمض السياليك، لكن هذا الاتصال يومض ويختفي عبر الزمن. ما يحافظ على ثبات المعقد هو أمر جديد: يتوغل تريبتوفان مجاور (Trp127) في الجزء الدهني من الغشاء، بينما يتفاعل ليسين مجاور (Lys126) مع مجموعات الرؤوس المشحونة للدهون المحيطة. يعمل هذا «الوتد» في الغشاء كمكمل لتفاعل السكر–الأرجينين المعتاد، مستعيرًا فعليًا طاقة ارتباط من بيئة الدهون. عندما تزال الجالاكتوز النهائي لـ GM1 لتقليد GM2، يتأرجح حلقة مرنة في Siglec-6 إلى الفراغ الناتج، تسحب المستقبل بعيدًا عن الغشاء وتفكك هذه القبضة المدعومة بالغشاء، موضحة فقدان الارتباط المستقر.
تجارب وضعت الآلية على المحك
اختبر الفريق بعد ذلك هذه الرؤى الحاسوبية في تجارب خلوية وكيميائية حيوية حية. مهندسوا خلايا لتعبّر عن Siglec-6 الطبيعي أو المطوّر وقيّموا مدى ارتباط هذه الخلايا بالحويصلات الدهنية المضيئة والأقراص الدهنية الصغيرة الحاملة لـ GM1. قللت طفرة الأرجينين الكلاسيكي الارتباط بشكل طفيف عندما كان GM1 في غشاء، مما يؤكد أن Siglec-6 لا يعتمد فقط على هذا البقايا في ذلك السياق. على العكس، أدت طفرة Trp127 إلى إلغاء الارتباط تقريبًا مع الحويصلات الحاملة لـ GM1، وأدت طفرة كل من Trp127 وLys126 معًا إلى تقليل الارتباط إلى حد كبير. نفس الطفرات، مع ذلك، ارتبطت طبيعيًا بالسكريات الشبيهة بـ GM1 المعروضة خارج الغشاء، مما يظهر أن البنية الأساسية لـ Siglec-6 كانت سليمة. كشفت تجارب الطيف الكتلي للأنواع الأصلية أيضًا أن Siglec-6 يمكنه الارتباط ليس فقط بـ GM1 بل أيضًا بالفوسفوليبيدات العادية، وأن هذا التفاعل مع الدهون يختفي عند إزالة Trp127. اللافت أن Siglec-6 يلتصق حتى بالحويصلات «العارية» الخالية من GM1، ومرة أخرى بطريقة تعتمد على Trp127، ما يوحي بأنه قد يبدأ بفحص الغشاء ثم يثبت ارتباطه عندما يواجه GM1.
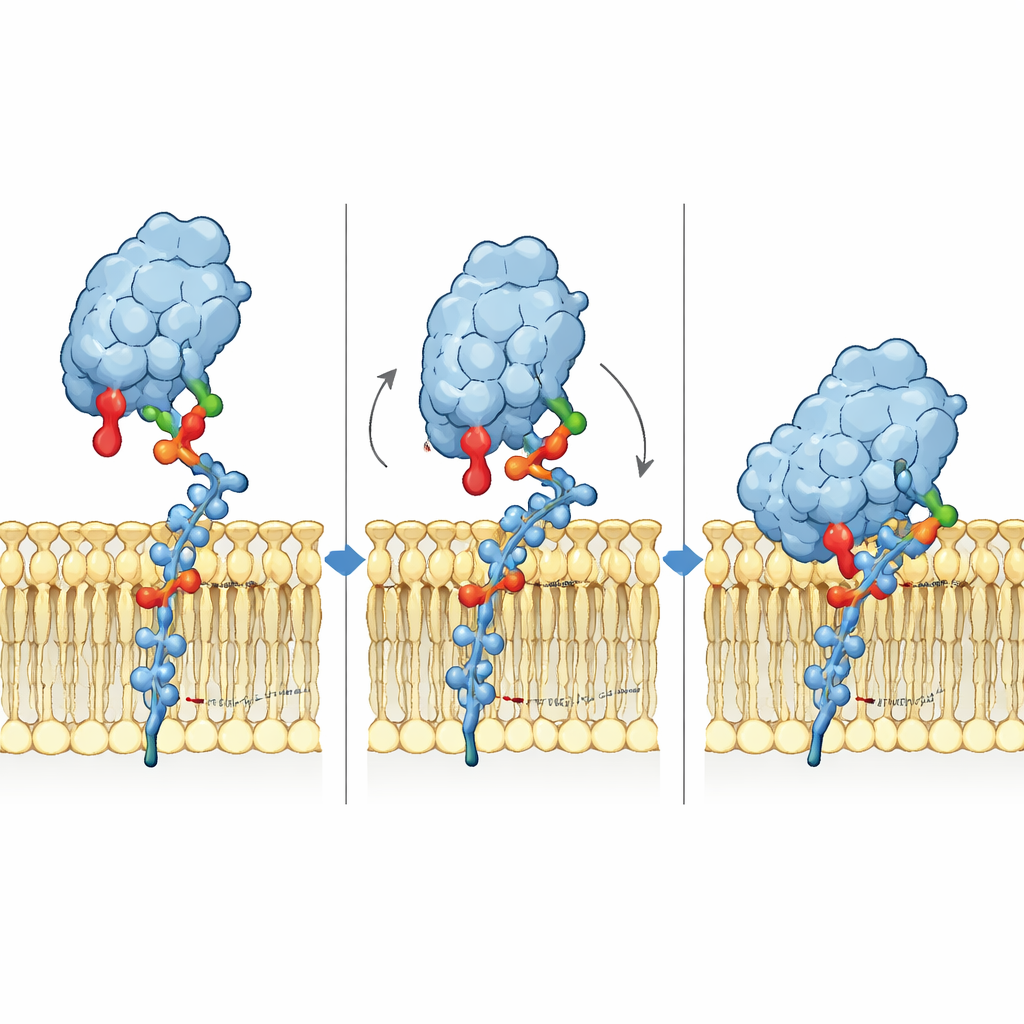
السكريات الحرة تروي قصة مختلفة
عندما اختبرت نفس الغانغليوسيدات الثلاثة كقطع سكرية عائمة بدلًا من كونها جزءًا من غشاء، تصرف Siglec-6 أشبه بباقي أقاربه. في المحلول، ارتبط بضعف وبشكل مماثل بـ GM1 وGM2 وGM3، والآن أضحى الأرجينين الكلاسيكي أساسيًا: خفضت طفرة Arg122 الارتباط بشدة، بينما كانت طفرة Trp127 ذات تأثير طفيف. يظهر هذا التباين أن Siglec-6 يبدّل الآليات اعتمادًا على ما إذا كان يواجه السكريات في غشاء أو في شكل حر. في الأغشية، يعتمد على شراكة تعاونية بين رأس السكر والجالاكتوز النهائي لـ GM1 والاتصال المباشر بالغشاء؛ في المحلول، يعود إلى نموذج التعرف الكلاسيكي المتمحور حول الأرجينين.
لماذا يهم هذا في تحكم الجهاز المناعي
مجتمعة، تكشف الدراسة أن Siglec-6 حساس مضبوط بدقة يستخدم السياق الفيزيائي للغشاء لصقل خصوصيته. من خلال تثبيت نفسه جزئيًا في الدهون المحيطة، يستطيع التعرف انتقائيًا على GM1 بين غانغليوسيدات متشابهة للغاية، محولًا قارئًا عامًا لحمض السياليك إلى كاشف عالي الدقة لنمط سطحي محدد. يبدو أن هذه الاستراتيجية المدعومة بالغشاء فريدة بين السيغليكيات المدروسة حتى الآن وقد تساعد Siglec-6 على مسح أسطح الخلايا بحثًا عن بصمات غليكوليبيد محددة تنظم الاستجابات المناعية أو تشير إلى أنسجة معينة، مثل المشيمة البشرية. قد يساعد فهم هذا النمط المزدوج للتعرف في تصميم علاجات وأدوات تشخيصية تستغل تركيبة Siglec-6 الفريدة من نوعها في استشعار السكر والغشاء.
الاستشهاد: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
الكلمات المفتاحية: Siglec-6, الغانغليوسيدات, غشاء الخلية, التعرف على الغليكوليبيد, تنظيم المناعة