Clear Sky Science · ar
تثبيط ATM يعزز كفاءة الإدخال الدقيق عن طريق قمع تنشيط مسارات الاستماتة الناجم عن AAV
جعل تحرير الجينات أكثر فعالية
يَعِد تحرير الجينات بتقنية CRISPR بعلاجات للأمراض الوراثية، ومحاصيل أقوى، وأدوات بحثية قوية. لكن إحدى حيلها الأكثر قيمة — إدراج حمض نووي جديد بدقة في موقع محدد من الجينوم، والمعروفة باسم «الإدخال الدقيق» (knock-in) — لا تزال تعمل بكفاءة منخفضة. يستكشف هذا العمل سبب قبول بعض الخلايا للحمض النووي الجديد بسهولة أكبر من غيرها ويكشف طريقة لحث الخلايا على إجراء تعديلات دقيقة بتكرار أكبر، خاصة عند استخدام الفيروس المعتمد على الغدد الكبدية (AAV)، وهو ناقل رائد للعلاج الجيني.
مراقبة إصلاح الحمض النووي في الوقت الحقيقي
لفهم ما يساعد أو يعيق الإدخال الدقيق للجينات، بنى الباحثون «لوحة أدوات» معقدة داخل خلايا جذعية جنينية فأرية. يستخدم هذا النظام الثلاثي للإبلاغ ثلاث علامات فلورية لتتبع، في نفس الخلايا، ما إذا كانت تقنية CRISPR قد قطعت الحمض النووي، وما إذا حدث إدخال دقيق بالفعل، وما إذا كانت الخلية قد ألصقت الحمض النووي المانح بطريقة أدق أكثر خطورة. من خلال قراءة تراكيب الألوان المختلفة بواسطة قياس التدفق الخلوي، تمكنوا من فصل التعديلات النمطية المعتمدة على القالب عن الإدخالات العُرضية والأخطاء والخلايا غير المعدلة. سمح لهم هذا التتبع جنبًا إلى جنب برسم خريطة لكيفية مساهمة مسارات إصلاح الحمض النووي المختلفة في كل نتيجة بدقة أعلى بكثير من الاختبارات التقليدية المعتمدة على PCR.
مساعدان للحمض النووي، واستجابتان متباينتان تمامًا
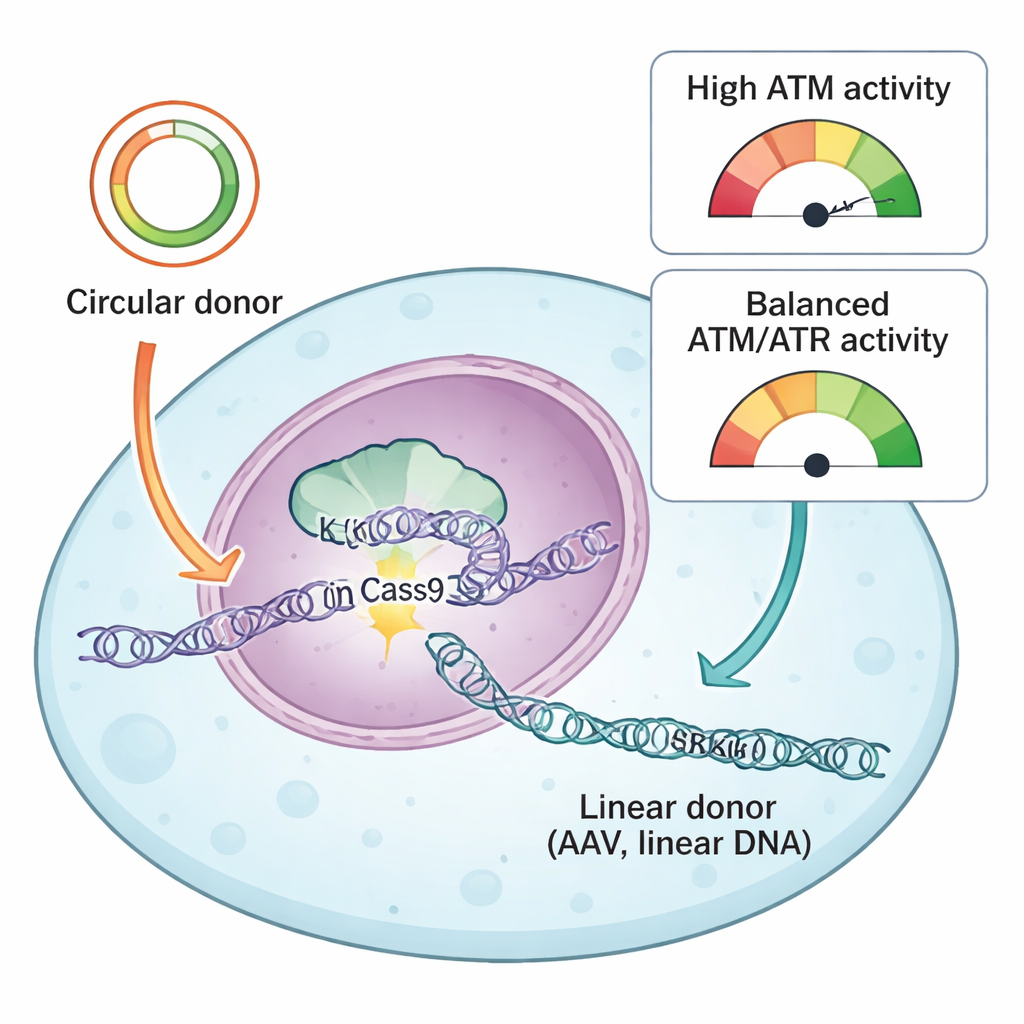
قارن الفريق نوعين شائعين من الحمض النووي المانح المستخدمين لتوجيه إصلاحات CRISPR: البلازميدات الدائرية وDNA المستمد من AAV الخطي. كلاهما يحملان «أذرع تماثل» تخبر الخلية أين تُدرَج السلسلة الجديدة، لكنهما يدخلان الخلية بأشكال فيزيائية مختلفة. البلازميدات الدائرية هي حلقات مغلقة من DNA مزدوج الشريط، بينما عادةً ما تصل الناقلات المانحة من AAV كمولات خطية أحادية الشريط. باستخدام نظام الإبلاغ ومكتبة من الأدوية التي تستهدف بروتينات استجابة تلف الحمض النووي، وجد المؤلفون أن بروتينًا رئيسيًا واحدًا، ATR، كان ضروريًا باستمرار لنجاح الإدخال الدقيق مع كلا النوعين من المانحين. أدى تثبيط ATR إلى خفض حاد في الإدخالات الدقيقة، بينما أدى تعزيز نشاط ATR بلطف عبر مسار KEAP1–NRF2 إلى زيادة كفاءة الإدخال الدقيق، لا سيما مع مانحي AAV.
عندما يعود حماية الحمض النووي بنتيجة عكسية
أظهر مستشعر تلف الحمض النووي المختلف، ATM، سلوكًا متباينًا بوضوح اعتمادًا على نوع المانح. مع البلازميدات الدائرية، أدى حظر ATM إلى تقليل كل من الإدخال الدقيق والإدخالات التي تتم عبر الربط النهائي، متوافقًا مع دوره الكلاسيكي في مساعدة الخلايا على إصلاح فُرَقات الشريط المزدوج. لكن مع الحمض النووي الخطي — سواء من AAV، أو AAV ذي شريطين مكملين ذاتيًا، أو بلازميدات قُطِّعت إلى قطع مستقيمة — كان لتثبيط ATM التأثير المعاكس: زاد من كفاءة الإدخال الدقيق. عزى الباحثون هذا الأثر إلى كيفية تفسير الخلايا لدفعات الحمض النووي الخطي. أدّت جرعات عالية من AAV إلى تنشيط قوي لـ ATM، مما فعّل بدوره p53 وcaspase 3، الفاعلان المحوريان في الموت المبرمج. كانت الخلايا التي استوعبت نسخًا كثيرة من الحمض النووي المانح، وبالتالي كانت تمتلك أعلى فرصة للإدخال الناجح، أيضًا الأكثر عُرضة للقتل بواسطة هذا نظام الإنذار.
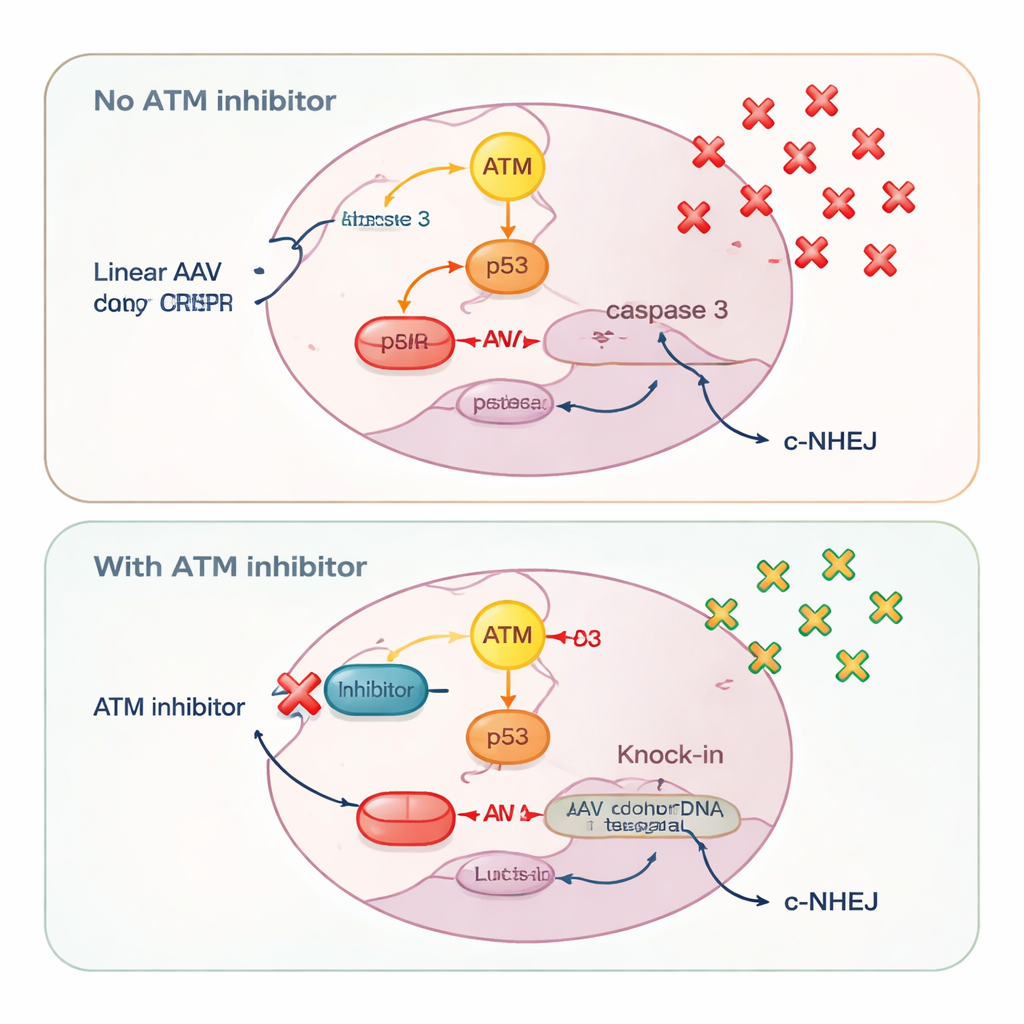
إنقاذ الخلايا الأقدر
بإضافة مثبطات ATM، كَبح العلماء مسار الموت ATM–p53–caspase 3. وفر ذلك للخلايا الحاملة لكميات عالية من الحمض النووي المانح فرصة للنجاة بما يكفي لإتمام الإدخال الدقيق. أكدت قياسات نسخ الجينوم الفيروسي أن تثبيط ATM زاد من عدد جزيئات AAV المحتفظ بها داخل الخلايا. في الوقت نفسه، قلل حظر ATM بشكل طفيف مسار إصلاح سريع وحاد يُسمى الإصلاح غير المتجانس النهائي الكلاسيكي (classical non-homologous end-joining)، كما بين ذلك انخفاض تنشيط DNA-PK، وهو إنزيم أساسي في ذلك المسار. أدى إضعاف خيار الإصلاح المتنافس هذا إلى دفع المزيد من قطوع CRISPR نحو الإدخال المعتمد على التماثل بدلًا من رقعات سريعة تتجاهل قالب المانح.
ماذا يعني هذا لعلاجات الجينات في المستقبل
بالنسبة لغير المتخصصين، الرسالة هي أن نفس آليات حماية الخلايا التي تحمينا من تلف الحمض النووي قد تُخربُ عن غير قصد التحرير الدقيق للجينات، لا سيما عند استخدام كميات كبيرة من حمض نووي فيروسي مانح. يوضح هذا العمل أن تعديل تلك الآليات بلطف — الحفاظ على نشاط ATR ولكن قمع ATM مؤقتًا عند وجود مانحين خطيين مثل AAV — يمكن أن يجعل عمليات الإدخال الدقيق بواسطة CRISPR أكثر موثوقية وكفاءة. قد تحسّن مثل هذه الاستراتيجية العلاجات الجينية وهندسة الخلايا ونماذج الأمراض من خلال مساعدة المزيد من الخلايا على قبول التغيير المقصود مع تجنب فقدان الخلايا غير الضروري.
الاستشهاد: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
الكلمات المفتاحية: التعديل الجيني CRISPR, تحرير الجينات بواسطة AAV, استجابة تلف الحمض النووي, تثبيط ATM, هندسة الجينوم