Clear Sky Science · ar
تصنيف قابلية تطوير النانوبودي لتحسين تصميم الأدوية العلاجية باستخدام محلل النانوبودي العلاجي
لماذا تهم أقارب الأجسام المضادة الصغيرة للأدوية المستقبلية
العديد من الأدوية الرائدة اليوم هي أجسام مضادة — بروتينات تلتصق بالأهداف المرضية بدقة عالية. فئة أحدث من الروابط الأصغر حجماً، المسماة النانوبوديز، قادرة على الانزلاق إلى جيوب يصعب الوصول إليها على الفيروسات والأورام وجزيئات أخرى. لكن القدرة على الارتباط بالهدف ليست كافية: يجب أن يكون المرشح الدوائي سهل التصنيع، مستقرًا في القنينة، وآمنًا داخل الجسم. تقدم هذه الورقة محلل النانوبودي العلاجي، أداة حاسوبية صممت لمساعدة العلماء على تقييم، مبكرًا ومن تسلسل الحمض الأميني فقط، أي النانوبوديز أكثر احتمالًا لأن تصبح أدوية عملية.
من فكرة واعدة إلى دواء عملي
تحويل بروتين إلى علاج حقيقي ينطوي على مجموعة من العقبات العملية المجتمعة تحت مصطلح «قابلية التطوير». يجب أن تُنتج البروتينات بكميات كبيرة، تبقى قابلة للذوبان، تتجنب التكتل، وتظل مستقرة أثناء الشحن والتخزين. على مدى العقد الماضي، تعلّم الباحثون كيف يتنبأوا بالعديد من هذه الخصائص للأجسام المضادة أحادية النسيلة كاملة الحجم، بدعم من بيانات سريرية واختبارات مخبرية متخصصة وفيرة. لكن النانوبوديز مختلفة هيكليًا: فهي تتألف من نطاق مفرد بدلًا من زوج سلاسل، غالبًا ما تملك حلقات ارتباط أطول، وتكشف مناطق سطحية تكون مدفونة في الأجسام المضادة التقليدية. نتيجة لذلك، قد تعطي الطرق المصممة للأجسام المضادة العادية إجابات مضللة عند تطبيقها على النانوبوديز.
محلل مصمم لخصوصيات النانوبودي
لمعالجة هذا الاختلاف، صمم المؤلفون محلل النانوبودي العلاجي (TNP)، مستندين إلى أداة سابقة للأجسام المضادة القياسية لكن أعيد هندستها حول بيولوجيا النانوبوديز. جمعوا تسلسلات النانوبوديز من مصادر عديدة: تجارب سريرية، مخزونات مناعية طبيعية، براءات اختراع، أوراق علمية، وهياكل بلورية معروفة. باستخدام متنبئات بنى عميقة مُكيَّفة للأجسام المضادة أحادية النطاق، أنتجوا نماذج ثلاثية الأبعاد لهذه التسلسلات. ومن كل نموذج قياسوا طول حلقات الارتباط، مدى امتداد حلقة رئيسية من جسم البروتين، وكيف تُرتَّب تجمعات البقايا الكارهة للماء والمشحونة على السطح — ميزات تؤثر بقوة على الذوبانية، والتجمع، والالتصاق غير النوعي.
جانبان بنيويان، وكلاهما قابل للتطبيق
واحدة من أكثر النتائج بروزًا تتعلق بحلقة الارتباط الرئيسية، المعروفة باسم CDR3. عندما قام الفريق بتكميم مدى «تكتل» هذه الحلقة — بمقارنة طولها بمدى امتدادها من البروتين — وجدوا انقسامًا واضحًا إلى نمطين بنيويين. في أحد الفرعين، تكون الحلقة أطول وتطوى فوق جانب البروتين، مكونة العديد من الاتصالات المساعدة مع مجموعة من البقايا المميزة. في الفرع الآخر، تبرز الحلقة أكثر كما في جزء من جسم جسم مضاد تقليدي. تحتل النانوبوديز في المرحلة السريرية كلا النمطين، وعند مقارنة الباحثين بعشرات القياسات المخبرية العملية — مثل التجمع، والتراكم الذاتي، والثبات الحراري — لم يروا عقوبة منهجية لأي من النمطين. هذا يعني أن مصممي الأدوية ليسوا مضطرين لتفضيل شكل حلقة واحد على الآخر عمومًا، طالما أن الخصائص الأخرى مقبولة.
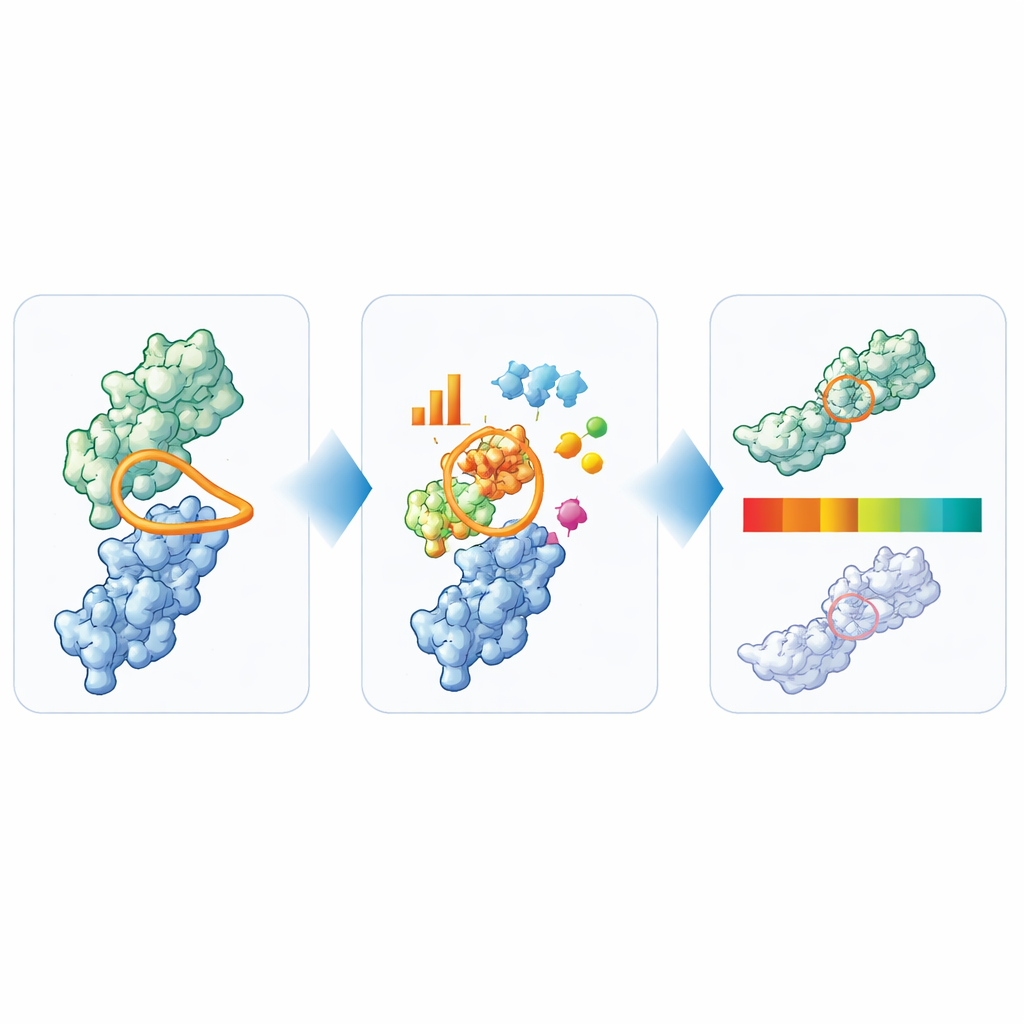
تحويل البنية إلى إشارات مرورية بسيطة
من تحليلهم الواسع، استخلص المؤلفون ستة ميزات رئيسية تلتقط معًا أهم مخاوف قابلية التطوير للنانوبوديز: الطول الإجمالي للحلقات، الطول والكتلة المحددة لـ CDR3، وأحجام الرقع السطحية الكارهة للماء والموجبة والسالبة حول موقع الارتباط. ثم استخدموا 36 نانوبودي وصلت إلى الاختبارات السريرية لتحديد حدود عملية لكل مقياس. تُوسم القيم في المنطقة المركزية المألوفة بـ «أخضر»، والقيم الحدية بـ «كهرماني»، والمتباعدة الواضحة بـ «أحمر». لاختبار مدى معلوماتية هذه الإشارات، طبقوا TNP على 72 نانوبودي إضافية خاصة وقارنوا العلامات بمجموعة واسعة من الاختبارات المخبرية. عادة ما أظهرت النانوبوديز التي صنفها TNP كمتباعدة بوضوح عدة إشارات تحذيرية تجريبية أيضًا، بينما كانت النانوبوديز التي بدت نظيفة حسابيًا أكثر سلوكًا جيدًا في المختبر.
ما يعنيه ذلك لعلاجات الغد
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن شكل ونمط السطح للنانوبودي يمكن الآن تحويلهما إلى ملف قابلية تطوير بسيط قبل أن تبدأ الأعمال المخبرية المكلفة. لا يحل محل محلل النانوبودي العلاجي التجارب، ولا تزال التباينات بين التنبؤات والاختبارات تحدث، خصوصًا لأن الاختبارات المخبرية أُجريت على نانوبوديز ملتصقة بقطع أكبر من الأجسام المضادة. لكن من خلال الإشارة سريعًا إلى المرشحين ذوي الحلقات الطويلة جدًا أو المطوية بإحكام أو ذوي الرقع السطحية الإشكالية، يساعد TNP في توجيه الانتباه نحو النانوبوديز التي من المرجح أن تصبح أدوية موثوقة. ومع دخول مزيد من النانوبوديز في التجارب السريرية وتوسيع مجموعة المراجع، ينبغي أن تصبح هذه الأداة أدق، مما يسرع تصميم أدوية صغيرة ومتينة شبيهة بالأجسام المضادة لمجموعة واسعة من الأمراض.
الاستشهاد: Gordon, G.L., Gervasio, J., Souders, C. et al. Characterising nanobody developability to improve therapeutic design using the Therapeutic Nanobody Profiler. Commun Biol 9, 344 (2026). https://doi.org/10.1038/s42003-026-09594-y
الكلمات المفتاحية: النانوبوديز, قابلية تطوير الأدوية البيولوجية, التحليل الحاسوبي, هندسة الأجسام المضادة, ثبات البروتين