Clear Sky Science · ar
تدهور TUBB3 الوسيط بواسطة DTX1 في خلايا كوبفر يخفف تقدم سرطان الكبدة عن طريق تنظيم استقطاب M1/M2
لماذا تهم «الجيران» المناعية في الكبد
يفكر معظم الناس في السرطان على أنه مرض ناتج عن خلايا خارجة عن السيطرة. لكن الأورام تعيش في حي مزدحم من الخلايا المناعية والأوعية الدموية والأنسجة الداعمة التي يمكن أن تحارب السرطان أو تساعده بهدوء على النمو. تبحث هذه الدراسة في سرطان الكبد — وتحديداً سرطان الخلايا الكبدية — وتكشف كيف يمكن لبروتين داخل خلايا مناعية متخصصة في الكبد أن يميل الميزان بين استجابة مضادة للسرطان وبيئة مواتية للورم. قد يفتح فهم هذا المفتاح الخفي طرقاً جديدة لتحسين العلاجات المناعية الحالية.
سرطان الكبد الذي يقوده محيطه
الكبد غني بالخلايا المناعية، بما في ذلك مجموعة مقيمة تسمى خلايا كوبفر التي تساعد عادة في الحفاظ على صحة العضو. في سرطان الكبد تتحول العديد من هذه الخلايا إلى بلاعم مرتبطة بالأورام يمكن أن تهاجم السرطان (حالة شبيهة بـ M1) أو تحميه (حالة شبيهة بـ M2). المرضى الذين تحتوي أورامهم على كثافة عالية من البلاعم من النوع M2 عادة ما تكون نتائجهم أسوأ وغالباً ما يستجيبون بشكل ضعيف للعقاقير التي تفتح المكابح المناعية، مثل مثبطات PD-1. بدأ المؤلفون بالتنقيب في قواعد بيانات جينية عامة وعينات مرضى للبحث عن جزيئات مرتبطة بكل من سرطان الكبد وهذه البلاعم، وركزوا على بروتين بنيوي يسمى TUBB3 وُجد بكمية غير متوقعة في نسيج الورم.
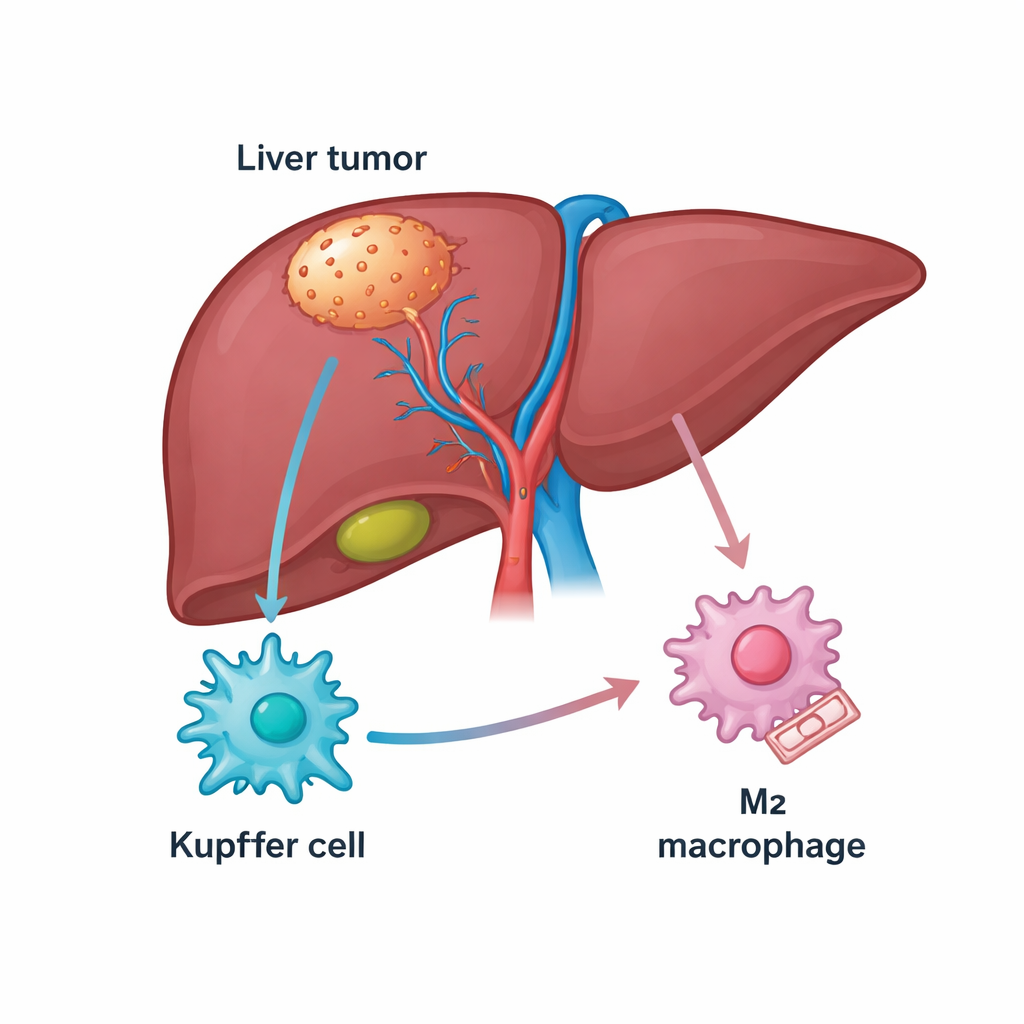
بروتين مفاجئ يدفع الخلايا المناعية لمساعدة الأورام
يُعرف TUBB3 بشكل أساسي كجزءٍ من «السكك» المجهرية داخل الخلايا، لكنه رُبط أيضاً بسلوك عدواني ومقاومة للعقاقير في عدة أنواع من السرطان. هنا وجد الباحثون أن مستويات TUBB3 كانت أعلى بكثير في أورام الكبد عنها في النسيج الصحي المجاور، وأن المرضى ذوي مستويات TUBB3 الأعلى كانوا يميلون إلى بقاء أقصر. باستخدام تقنيات التلوين، أظهروا أن TUBB3 كان مركَّزاً بشكل خاص في خلايا كوبفر داخل الأورام، وكان وجوده مرتبطاً بقوة بعلامات الحالة المساعدة للورم من نوع M2. بعبارة أخرى، كانت خلايا كوبفر المليئة بـ TUBB3 أكثر ميلاً للتصرف بطرق تُضعف الهجوم المناعي وتدعم نمو السرطان.
إعادة برمجة البلاعم لكبح أورام الكبد
لاختبار السببية، قلل الفريق مستويات TUBB3 في خلايا كوبفر في تجارب مخبرية. عندما تم خفض TUBB3، أنتجت هذه الخلايا إشارات أقل من النوع M2، وإشارات أكثر من النوع M1، وأفرزت عدداً أقل من الجزيئات التي تقمع النشاط المناعي عادة. نمت خلايا سرطان الكبد المعرّضة لهذه البلاعم المعاد برمجتها بوتيرة أبطأ، انقسمت أقل، وكانت أقل قدرة على الهجرة والغزو. في الفئران، أدى خلط خلايا سرطان الكبد مع خلايا كوبفر ناقصة TUBB3 إلى أورام أصغر، ومزيد من موت خلايا السرطان، وتدفق أكبر لخلايا CD8 القاتلة المزوَّدة ببروتينات مدمرة. وإذا أزيلت البلاعم من الحيوانات تماماً، اختفى الجزء الأكبر من فائدة حجب TUBB3، مما يؤكد أن التأثير يمر عبر هذه الخلايا المناعية وليس عبر خلايا السرطان وحدها.
كشف مكبح داخلي في مسار إشارة رئيسي
استقصت الدراسة أيضاً كيف يمارس TUBB3 هذا التأثير. ركز المؤلفون على مسار نمو وبقاء معروف يتحكم فيه بروتينان هما PTEN وAKT، والذي يشكل أيضاً ما إذا كانت البلاعم تتبنى هوية M1 أو M2. وجدوا أن خفض TUBB3 زاد من PTEN، مما قلل بدوره من «وسوم الفسفرة» المفعلة على AKT، دافعاً البلاعم نحو الحالة المحاربة للورم. عندما أعادوا تنشيط AKT صناعياً، عادت البلاعم إلى نمط M2 واستعادت خلايا السرطان سلوكها العدواني، حتى في غياب TUBB3. وضع هذا TUBB3 فوق PTEN وAKT كنوع من المقبض الداخلي لسلوك البلاعم.
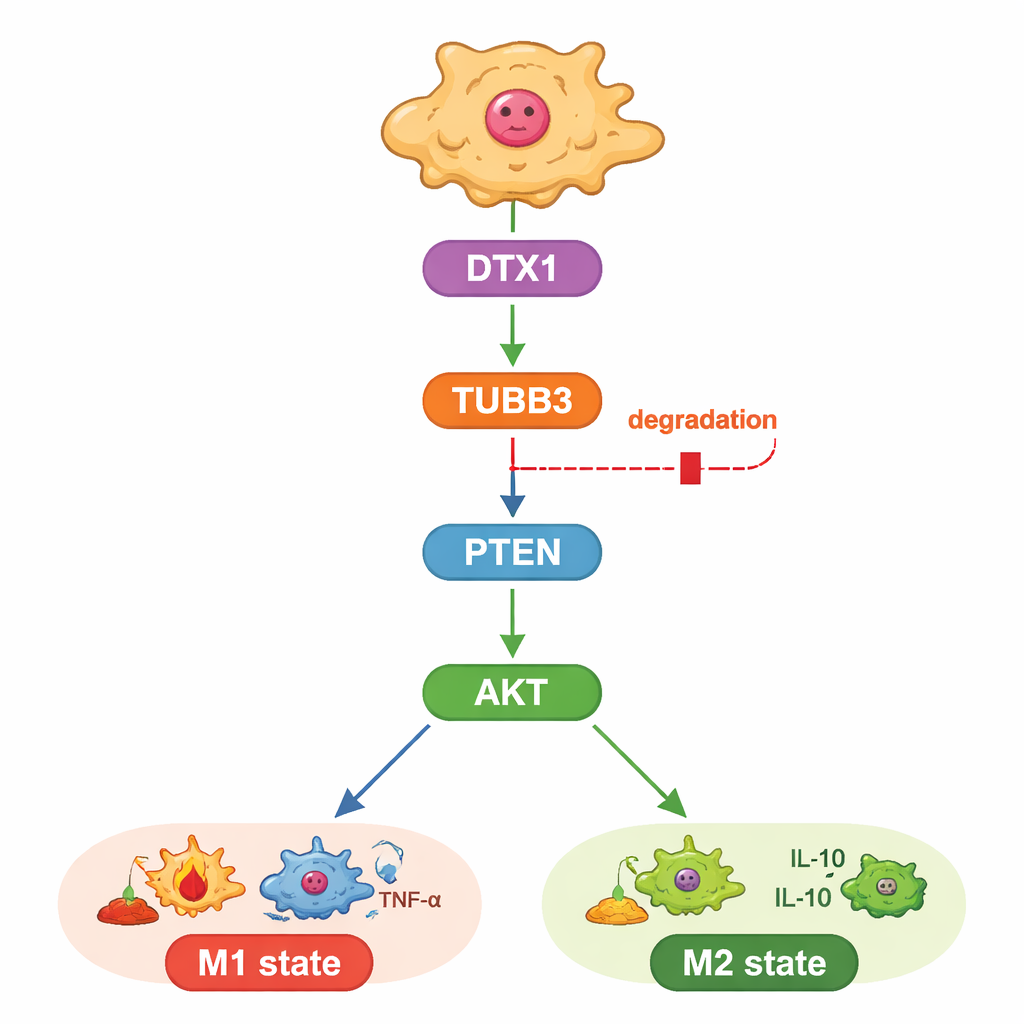
وسم نفايات مدمج يمكن إعادة تشغيله
أخيراً، سأل الباحثون لماذا يتراكم TUBB3 بكثرة في أورام الكبد. من خلال الجمع بين التنبؤات المعلوماتية الحيوية وبيانات التعبير الجيني، حدّدوا إنزيمًا يسمى DTX1، جزءاً من عائلة تضع وسم التخلص من البروتينات، كمنظم محتمل. كانت مستويات DTX1 أقل في أورام الكبد منها في النسيج السليم، وربطت بمآلات أفضل لدى المرضى وبوجود أكبر لبلاعم من النوع M1. في الخلايا، أدى تعزيز DTX1 إلى تسريع تحلل TUBB3، وخفض نشاط AKT، ودفع البلاعم نحو الحالة المحاربة للورم، مما قيد نمو خلايا السرطان. إلغاء هذا التأثير عن طريق إعادة إدخال TUBB3 إضافي أمحو فوائد DTX1، سواء في الأطباق الخلوية أو في أورام الفئران. معاً، ترسم هذه النتائج خطاً واضحاً من DTX1 عبر TUBB3 وPTEN/AKT إلى الطابع المناعي للورم.
ما الذي يعنيه هذا لعلاج سرطان الكبد في المستقبل
لغير المتخصصين، الرسالة الأساسية أن هذا العمل يحدد نظام تحكم مخفي داخل الخلايا المناعية المقيمة في الكبد يقرر ما إذا كانت تساعد أو تعيق السرطان. عندما يكون إنزيم وسم النفايات DTX1 منخفضاً، يتراكم TUBB3، وينشط مسار نمو، وتنزلق خلايا كوبفر إلى وضع يدعم الورم ويقلل فعالية العلاج المناعي. قد تعيد استعادة هذا المسار — بخفض TUBB3، أو تعزيز DTX1، أو ضبط إشارة PTEN/AKT بعناية — إيقاظ الدفاعات المناعية المحلية وجعل علاجات مثل مثبطات PD-1 أكثر فاعلية. رغم أن مثل هذه الاستراتيجيات لا تزال في مرحلة تجريبية، فإنها تبرز وعد علاج ليس فقط خلايا الورم، بل أيضاً «الجيران» المناعية المحيطة التي تؤثر بشدة على سلوك سرطان الكبد.
الاستشهاد: Sun, J., Sun, T., Zhang, Y. et al. DTX1-mediated degradation of TUBB3 in Kupffer cells mitigates hepatocellular carcinoma progression by regulating M1/M2 polarization. Commun Biol 9, 311 (2026). https://doi.org/10.1038/s42003-026-09593-z
الكلمات المفتاحية: سرطان الكبدة, البلاعم المرتبطة بالأورام, خلايا كوبفر, العلاج المناعي, إشارات AKT