Clear Sky Science · ar
آليات هيكلية لإنزيم التفكيك WRN تكشف حالات تصاوغ وفرص اكتشاف أدوية لسرطانات MSI-H
لماذا هذا مهم لعلاج السرطان
تحمل بعض الأورام ضعفًا داخليًا: فهي تواجه صعوبة في إصلاح الأخطاء في حمضها النووي. يعمل بروتين يسمى إنزيم التفكيك WRN كأداة جزيئية للإصلاح تُبقي هذه الأورام الهشة على قيد الحياة. تكشف هذه الدراسة، بتفصيل ذري، كيف يتحرك WRN على طول الحمض النووي وكيف يمكن لأدوية تجريبية إعاقة حركته — مما يوفر خارطة طريق لعلاجات جديدة تقتل هذه الخلايا السرطانية الضعيفة بشكل انتقائي مع الحفاظ على الأنسجة السليمة.
عامل صيانة الحمض النووي تحت المجهر
ينتمي إنزيم التفكيك WRN إلى طاقم صيانة الخلية، ويساعد على فك الحلزون المزدوج للحمض النووي حتى يمكن رصد وإصلاح الضرر. الأشخاص الذين يولدون دون WRN عامل يعمل يصابون بمتلازمة فيرنر، اضطراب نادر يتميز بالشيخوخة المبكرة، مما يبيّن مدى أهمية هذا البروتين للحفاظ على الجينوم. الأورام ذات «عدم استقرار الميكروساتلايت–عالي» (MSI‑H) — عيب شائع في سرطان القولون وبعض السرطانات الأخرى — تظهر اعتمادًا خاصًا على WRN. عند إيقاف WRN في هذه الخلايا، ينهار حمضها النووي الهش بسرعة وتموت الخلايا السرطانية. هذا يجعل WRN هدفًا دوائيًا جذابًا، لكن حتى الآن افتقر العلماء إلى رؤية واضحة لكيفية تغير شكل البروتين عندما يلتقط الحمض النووي، يحرق وقودًا كيميائيًا، ويتحرك على المادة الوراثية.
مراقبة تمدد WRN وانقباضه
استخدم المؤلفون البلَّورة بالأشعة السينية لالتقاط عدة «لقطات» عالية الدقة لنواة إنزيم التفكيك البشري WRN. حلّوا هياكل WRN بمفرده وبـ WRN المرتبط بالحمض النووي أحادي الشريطة وجزيء وقود شبيه بـATP غير قابل للكسر. كشفت هذه الصور أن البروتين مبني من فُقرتين رئيسيتين متصلتين بمفصل مرن يتصرف مثل مفصل يتنفس. في حالته الساكنة الخالية من الوقود، يتخذ WRN شكلًا مدمجًا «مغلقًا» تجلس فيه الفقرات بجوار بعضها. عندما يكون الوقود الشبيه بـATP والحمض النووي حاضرين، تتأرجح الفقرات بعيدًا إلى حالة أكثر «انفتاحًا» تستطيع احتضان الحمض النووي في أخدود موجب الشحنة. حلقة عطِرية صغيرة داخل WRNتعيد تشكيل نفسها إلى حلزون قصير وتتحشر بين قواعد الحمض النووي، فتعمل كالعتلة التي تساعد البروتين على التقدم دون الانزلاق إلى الخلف.
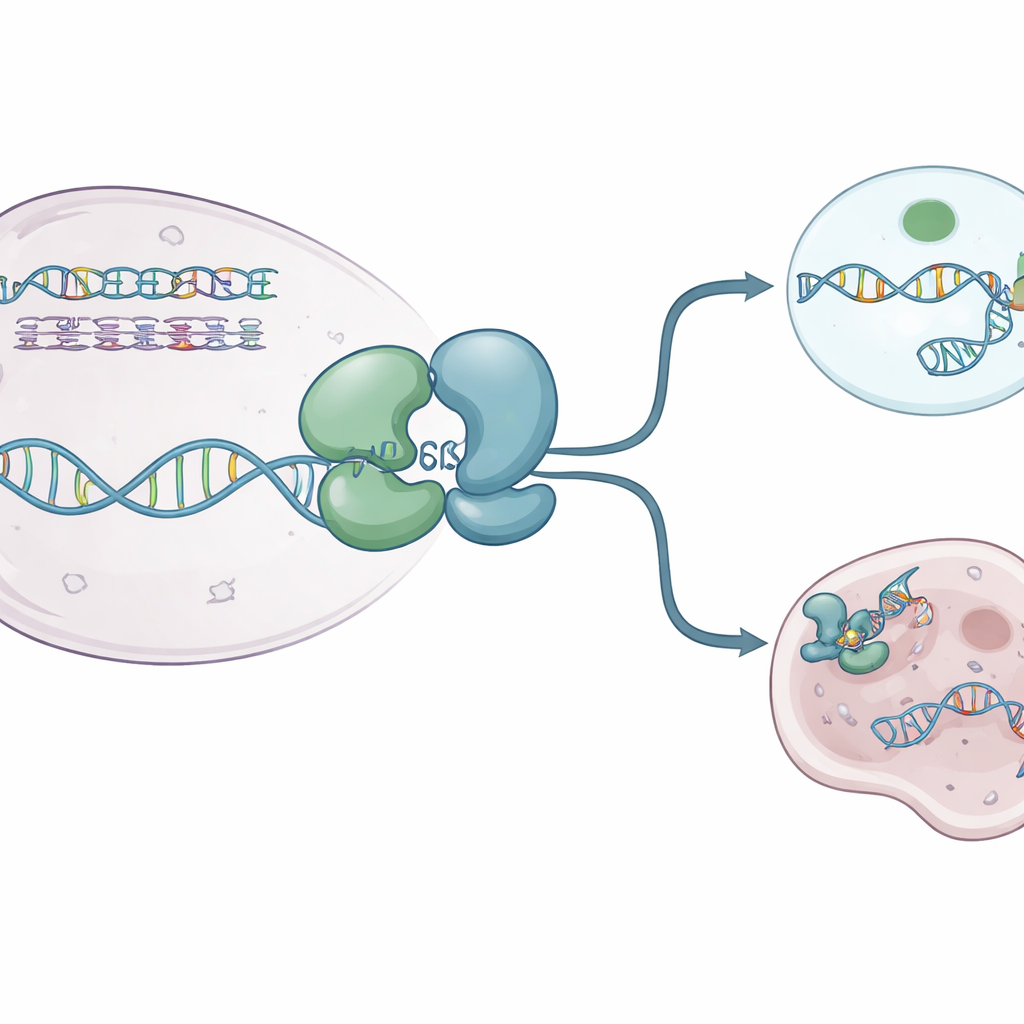
كيف تُطفأ WRN الأدوية الحالية
دخلت عدة مركبات حابسة لـWRN مؤخرًا تجارب سريرية. إنها لا تسد الأخدود الفعّال للبروتين مباشرة. بدلًا من ذلك، تعمل عن بُعد، مُمسِكة بمنطقة المفصل وتُقفل WRN في أشكال لا تستطيع الارتباط بالحمض النووي بشكل صحيح. بعض الجزيئات، مثل HRO761 ومرشّح سريري ذو صلة من GSK، تقلب إحدى الفقرات بحوالي 180 درجة بالنسبة للأخرى، مكونة شكلًا «ملتويًا» دراميًا يجلس بعيدًا عن الحمض النووي. أخرى، بما في ذلك VVD‑133214 ومركب ذو صلة درس هنا، تثبّت WRN في ترتيب «مغلق» بإحكام يفشل في كشف الأسطح الأساسية لالتقاط الحمض النووي. أكدت تجارب فيزيائية حيوية أنه عندما تكون هذه الأدوية مرتبطة، لا يستطيع WRN تكوين مركب مستقر مع الحمض النووي أحادي الشريطة، مما يقطع فعليًا الصلة بين استخدام ATP وفك لفائف الحمض النووي.
كيف تتعلّم الخلايا السرطانية الهرب
لمعرفة كيف قد تتجنب الأورام هذه الأدوية، نمّى الفريق خلايا سرطان القولون MSI‑H في وجود مثبطات WRN لأسابيع إلى أشهر. ظهرت مجموعات مقاومة بسرعة. أظهر التحليل الجيني أنه، في كل حالة، اكتسبت الخلايا تغييرًا واحدًا دقيقًا في جين WRN قرب مفصل ارتباط الدواء. أحد الطفرات أضعف تأثير مثبط «الحالة الملتوية» HRO761، بينما خفضت طفرة أخرى الحساسية تجاه VVD‑133214 الذي يفضّل الحالة المغلقة. بالإضافة إلى ذلك، رفعت العديد من الخلايا المقاومة إنتاج WRN، مانحة نفسها نسخًا أكثر من الهدف مما قلل جزئيًا من أثر الدواء. تعكس هذه النتائج أنماط المقاومة المرصودة مع أدوية سرطانية مستهدفة أخرى، حيث يمكن لتعديلات هيكلية صغيرة في البروتين الهدف أو الإفراط في التعبير أن تُخفف من العلاج.
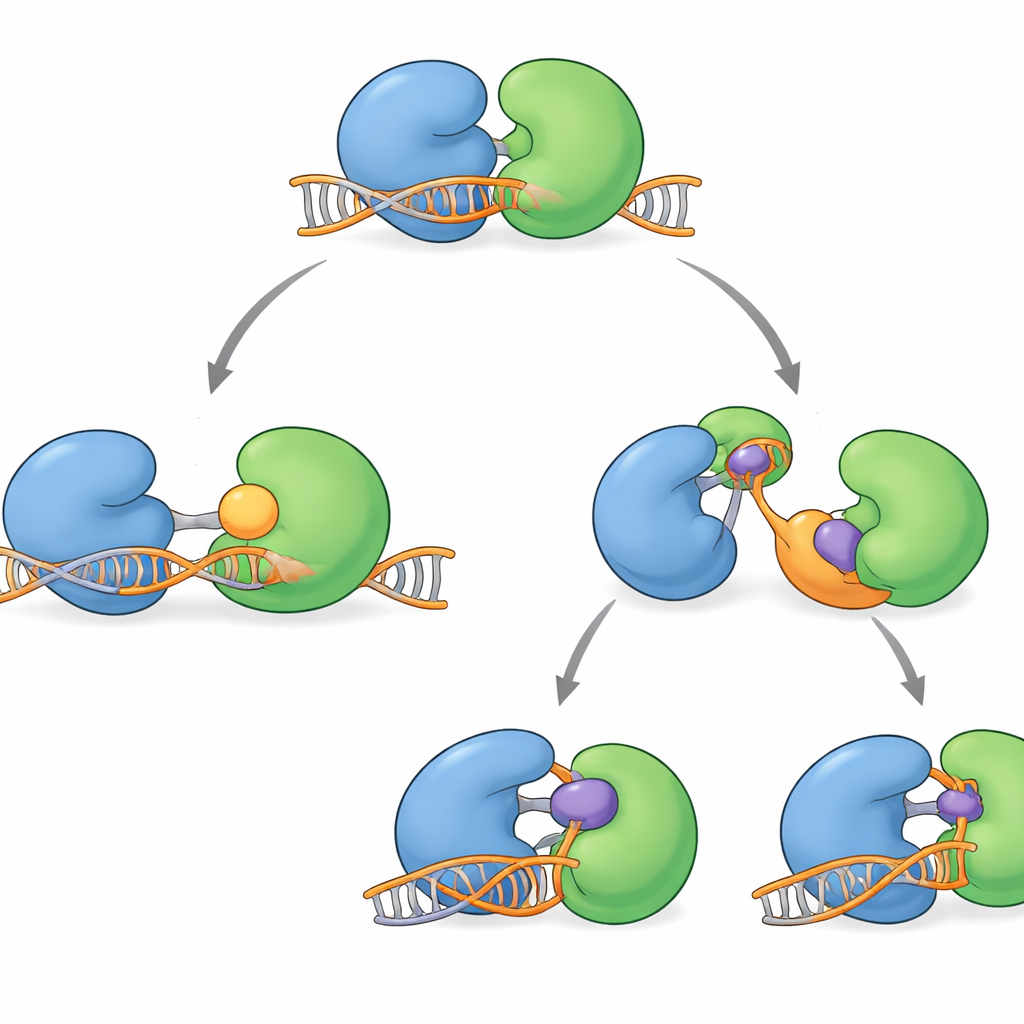
نظرة مستقبلية لمثبطات WRN أذكى
تجمع الهياكل الجديدة معًا دورة عمل كاملة لـWRN بينما يلتقط الحمض النووي، يتقدم خطوة، ثم يعيد ضبط نفسه. كما تُظهر أن مركبات اليوم السريرية تثبت بشكل أساسي أشكال البروتين «بعيدًا عن الحمض النووي». للناظر العام، الفكرة الأساسية هي أننا نفهم الآن أين يكون WRN عرضة وكيف قد تتكيف الأورام. هذا يقترح موجة جديدة من المثبطات التي ترتبط بـWRN عندما يكون مثبتًا على الحمض النووي، مما قد يحبسه في حالة سامة — تمامًا مثل الأدوية الناجحة التي تحبس إنزيمات إصلاح الحمض النووي الأخرى. مثل هذه المثبطات لـWRN «على الحمض النووي»، المستخدمة بمفردها أو إلى جانب عوامل قائمة، قد توفر طرقًا أكثر ديمومة لاستغلال الضعف الخفي في سرطانات MSI‑H.
الاستشهاد: Fletcher, C.T., Mornement, A.A., Barrett, C. et al. Structural insights into WRN helicase reveal conformational states and opportunities for MSI-H cancer drug discovery. Commun Biol 9, 334 (2026). https://doi.org/10.1038/s42003-026-09584-0
الكلمات المفتاحية: إنزيم التفكيك WRN, عدم استقرار الميكروساتلايت, إصلاح الحمض النووي, مثبطات آلوستركية, مقاومة الدواء