Clear Sky Science · ar
PiR48444 يثبط تمايز الخلايا الجذعية الميزانشيمية إلى خلية عظمية وتجديد العظم عبر استهداف مثيلة m6A لِـ BMP2 بواسطة METTL7A/eIF4E
لماذا تصنع الجزيئات الصغيرة فرقًا في كسور العظام
الكسور وفقدان العظام المرتبط بالعمر مشاكل شائعة، ويسعى الأطباء لاستخدام الخلايا الجذعية لمساعدة الجسم على إعادة بناء الهيكل العظمي التالف. ومع ذلك، لا تشكل هذه الخلايا دائمًا عظامًا جديدة بكفاءة كما نريد، لا سيما لدى كبار السن أو في الأنسجة الملتهبة. تكشف هذه الدراسة عن جزيء RNA صغير، يُدعى piR48444، يعمل كفرامل جزيئية على الخلايا الجذعية المكوّنة للعظم. بإطلاق هذه الفرملة، يُظهر الباحثون أنه قد يصبح بالإمكان تعزيز إصلاح العظم والحماية من فقدانه.
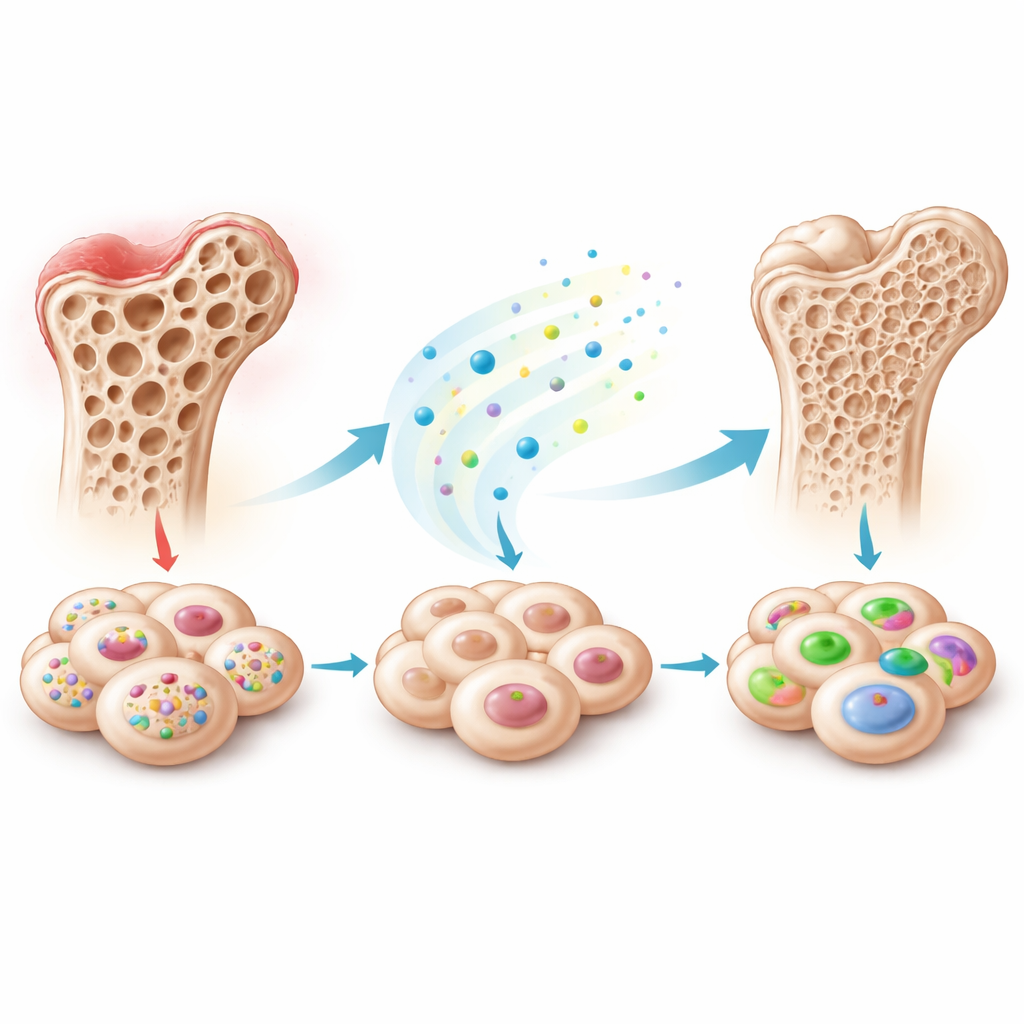
فرملة خفية داخل أنواع عديدة من الخلايا الجذعية
ركز الفريق على الخلايا الجذعية الميزانشيمية، وهي خلايا متعددة الاستخدامات يمكن أن تتحول إلى عظم أو غضروف أو دهون وغيرها، وتُستَخلص من أنسجة متعددة مثل نخاع العظم، أسنان الأطفال المتساقطة، والدهون. عندما تُحفَّز هذه الخلايا لتصبح عظمًا في المختبر، يتغير نشاط آلاف الجينات وجزيئات RNA الصغيرة. عبر تسلسل هذه الجزيئات في خلايا جذعية من أسنان الأطفال المتساقطة، وجد الباحثون أن أحد جزيئات RNA الصغيرة، piR48444، ينخفض باستمرار مع انتقال الخلايا نحو تكوين العظم. ثم فحصوا أنواع خلايا جذعية أخرى ورأوا نفس النمط: الخلايا التي تصنع مزيدًا من العظم كان لديها مستويات أقل من piR48444، ما يوحي بأن هذا الجزيء قد يقيد عادة قدرة الخلايا على تشكيل العظم.
من أطباق المختبر إلى عظام حية
لاختبار هذه الفكرة، عدّل العلماء مستويات piR48444 في عدة أنواع من الخلايا الجذعية. عندما خفضوا مستوى piR48444، رَكَّزت الخلايا مزيدًا من الكالسيوم، وفعّلت جينات مرتبطة بالعظم، وبدا نسيجها تحت المجهر أقرب إلى نسيج عظمي غير ناضج. عندما أجبروا الخلايا على إنتاج كمية إضافية من piR48444، حدث العكس: انخفض النشاط المرتبط بالعظم. انتقل الفريق بعد ذلك إلى نماذج حيوانية. استُخدمت خلايا جذعية معطَّلة فيها piR48444 لملء عيوب صغيرة في جماجم الفئران. هذه الخلايا المعدلة أنتجت عظامًا جديدة أكثر بكثير من الخلايا الضابطة، كما أظهرت الفحوص الشعاعية ثلاثية الأبعاد وصبغات الأنسجة، ما يشير إلى أن حجب piR48444 يمكن أن يحسّن إصلاح العظم في كائنات حية.
حماية العظام الهشة في المرض والشيخوخة
ليس الإصابات فقط هي ما يسبب فقدان العظم، بل الالتهاب والشيخوخة أيضًا. في خلايا نخاع العظم الجذعية المعرضة لسموم بكتيرية، وفي خلايا جذعية من حيوانات مسنة، كانت مستويات piR48444 مرتفعة بشكل غير عادي بينما كانت علامات بناء العظم منخفضة. صنع الباحثون «أنتاغومير»—جزيء قصير مصمم لتحييد piR48444 في مجرى الدم—وحَقنوه في فئران تعاني من فقدان العظم الناتج عن الالتهاب أو في فئران مسنة طبيعيًا. في كلا النموذجين، احتفظت الحيوانات المعالجة بمساحة أكبر من العظم الإسفنجي الداخلي، مع أعمدة عظمية دقيقة أكثر كثافة وتعددًا، بينما بقيت القشرة العظمية الصلبة الخارجية دون تغيير. هذا يشير إلى أن حجب piR48444 يمكن أن يحمي بشكل انتقائي الجزء الإسفنجي الهش والنشط أيضيًا من الهيكل العظمي، وهو الأكثر عرضة للخطر خلال الشيخوخة والالتهاب المزمن.
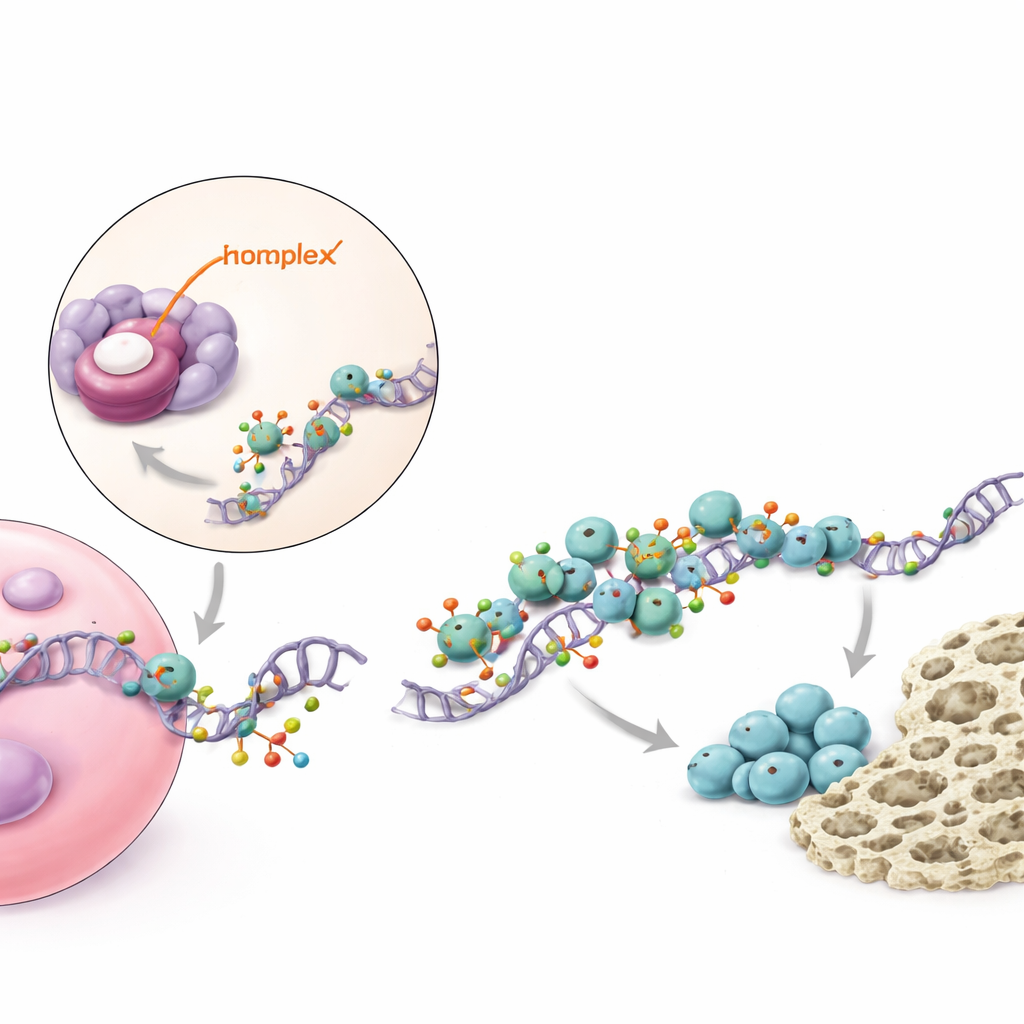
تتابع جزيئي يعزز إشارة أساسية للعظم
بالتعمق أكثر، رسمت الدراسة خريطة لكيفية تأثير piR48444 داخل الخلايا. يرتبط هذا الـ RNA الصغير ببروتين يُدعى METTL7A ويقوم بكبحه؛ يعمل METTL7A كإنزيم يعدّل جزيئات الرسول التي تحمل المخطط الخاص بـ BMP2، وهو عامل نمو معروف يشجع بشدة تكوّن العظم. يضيف METTL7A علامات كيميائية صغيرة لرسائل BMP2، ما يجعلها أكثر استقرارًا وأسهل قراءةً لآلية صنع البروتين في الخلية. كما يتعاون METTL7A مع بروتين آخر، eIF4E، الذي يساعد في بدء إنتاج البروتين. عندما يكون piR48444 وفيرًا، يُقمع METTL7A، وتقل الرسائل الموسومة من BMP2 وتُترجم أقل، فيُنتَج بروتين BMP2 بنسبة أقل، فتصبح الخلايا أقل ميلاً للتحول إلى عظم. عند حجب piR48444، يرتفع مستوى METTL7A وBMP2، مما يدفع الخلايا نحو تكوين العظم.
ما يعنيه هذا لإصلاح العظم في المستقبل
ببساطة، يكشف المؤلفون سلسلة تحكم يكون فيها RNA صغير (piR48444) مكمّدًا لإنزيم مساعد (METTL7A)، والذي بدوره يحد من إشارة قوية لبناء العظم (BMP2). بقطع هذه السلسلة عند مستوى piR48444، يمكنهم جعل أنواع مختلفة من الخلايا الجذعية أفضل في تشكيل العظم وتقليل فقدانه في الفئران. رغم أن السلامة، والتأثيرات غير المستهدفة، والنتائج الطويلة الأمد لا تزال بحاجة لاختبارات دقيقة، تشير الدراسة إلى piR48444 كعلامة محتملة في الدم لمخاطر هشاشة العظام وكهدف واعد لأدوية تهدف إلى تعزيز تجدد العظم المعتمد على الخلايا الجذعية في العيادة.
الاستشهاد: Zheng, Z., Li, X., Qin, W. et al. PiR48444 inhibits MSC osteogenic differentiation and bone regeneration via targeting METTL7A/eIF4E-mediated BMP2 m6A methylation. Commun Biol 9, 337 (2026). https://doi.org/10.1038/s42003-026-09583-1
الكلمات المفتاحية: تجديد العظم, الخلايا الجذعية الميزانشيمية, هشاشة العظام, الحمض النووي الريبي غير المشفر, إشارة BMP2