Clear Sky Science · ar
سيش CISH، نقطة تفتيش داخلية رئيسية، بالمقارنة والتكامل مع نقاط التفتيش المناعية السرطانية الحالية والناشئة
رفع الفرامل عن الخلايا المحاربة للسرطان
غيّرت العلاجات المناعية للسرطان توقعات الكثير من المرضى، لكن نسبة كبيرة من الأشخاص ما زالوا لا يحصلون على فائدة تُذكر أو لا يستجيبون بالمرة. تدرس هذه الدراسة طريقة جديدة لتعزيز خلايا تي الخاصة بالجسم — القتلة في جهاز المناعة — عن طريق تعطيل «مكابح» داخلية تسمى CISH. بخلاف الأدوية الحالية التي تؤثر على مفاتيح على سطح الخلية، تستهدف هذه الاستراتيجية نظام ضبط مدفون داخل الخلية، بهدف جعل الخلايا التائية المهندسة أكثر قدرة بكثير على العثور على الأورام وتدميرها، حتى عندما تحاول السرطانات التمويه.
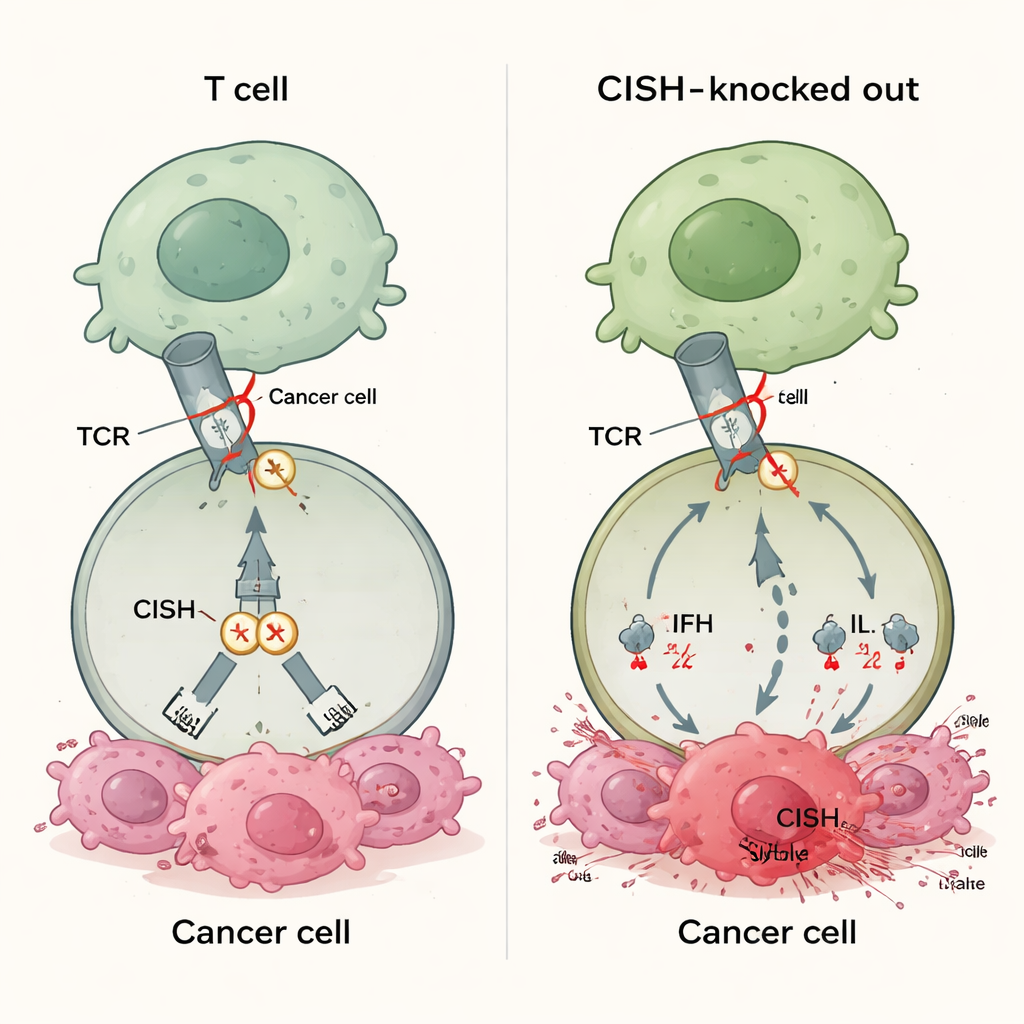
نوع جديد من مكابح المناعة
تمنع معظم الأدوية المناعية المعتمدة بروتينات مثل PD-1 على سطح خلايا تي. تعمل هذه الأدوية فقط عندما تعرض الأورام جزيئات شريكة متطابقة مثل PD-L1، والعديد من السرطانات إما لا تُعبّر بما يكفي من هذه الشريكات أو تفقدها مع الزمن. هذا يفسر جزئياً لماذا 30–60% من المرضى لا يستجيبون لعلاجات نقاط التفتيش الحالية. تنتمي CISH إلى فئة مختلفة من المكابح التي تجلس داخل خلية تي. تُشغّل عندما يستشعر مستقبل خلية تي هدفًا، ثم تُخفّض الإشارة عبر تعزيز تدمير بروتين إشارِي رئيسي. وبما أن هذا الفعل لا يعتمد على ربط الجزيئات المُعبر عنها من قبل الورم، فقد يؤدي تعطيل CISH، من حيث المبدأ، إلى تعزيز استجابات الخلايا التائية عبر أنواع عديدة من السرطان بغض النظر عن حالة PD-L1 أو علامات حيوية أخرى.
وجهاً لوجه مع نقاط التفتيش الحالية
استخدم الباحثون تحرير الجينات بتقنية CRISPR لإزالة CISH وقارنوا الخلايا التائية الناتجة بخلايا تخلت عن PD-1 أو عن عدة مكابح داخلية أخرى. عندما حفّزوا الخلايا التائية بشكل ضعيف — حالة تهدف إلى محاكاة الأورام التي تعرض كميات قليلة فقط من المستضد — أنتجت الخلايا التي حُذفت منها CISH كمية أكبر بكثير من الرواسب المناعية الرئيسية، بما في ذلك إنترفيرون-غاما، TNF-ألفا، وIL-2. كانت هذه الخلايا أيضاً أكثر «متعددة الوظائف»، بمعنى أن خلايا تي فرادية يمكنها أداء عدة مهام في آنٍ واحد، وهو سمة تشير إلى نشاط قوي مضاد للورم. بالمقابل، لم يُجدِ حذف PD-1 وحده في هذه الظروف ذات الإشارة الضعيفة. عبر اختبارات متعددة، عزز غياب CISH التنشيط، وقدرة القتل، وتكوين خلايا تي شبيهة بالذاكرة المستديمة بشكل أقوى من إزالة نقاط تفتيش داخلية مرشحة أخرى مثل RASA2، CBLB، SOCS1، REGNASE1، HPK1، أو PTPN1/2.
التعاون مع مفاتيح داخلية أخرى
بما أن إشارة خلية تي تتحكم بها العديد من المسارات المتداخلة، تساءل الفريق عما إذا كان الجمع بين حذف CISH وإزالة مكابح أخرى قد يمنح فوائد إضافية. باستخدام تحرير CRISPR متعدد الأهداف، وجدوا أن حذف CISH مع SOCS1 أو HPK1 أو RASA2 زاد أكثر من إنتاج السيتوكينات المفيدة تحت التحفيز الضعيف. في نموذج ورم قائم حول طفرة شائعة في KRAS، كانت الخلايا التائية المهندسة بمستقبل محدد لـKRAS أفضل في قتل خلايا السرطان عندما أُزيلت CISH، وتضاعف هذا التأثير عند اقتران غياب CISH بحذف SOCS1 أو RASA2. تقترح هذه النتائج أن CISH يتحكم في عقدة غير قابلة للاستبدال تمامًا في بيولوجيا خلية تي ويمكن أن تتعاون مع شركاء محددين لصقل القتل الموجه للورم.
جعل خلايا CAR-T أقوى أمام الأورام الماكرة
اتجه الباحثون بعد ذلك إلى إعداد ذي أهمية سريرية: خلايا CAR-T المستهدفة لبروتين CD19 على الخلايا البائية. أنشأوا خلايا لِيوكيميا تعبّر مستويات مختلفة من CD19 لمحاكاة أورام تفقد مستهدَفاتها أو تقللها للهروب من العلاج. كانت خلايا CAR-T الخالية من CISH أفضل بكثير في تدمير خلايا السرطان، حتى عندما كان CD19 نادراً، وأفرزت إشارات تنشيط واستدعاء أكثر. وفي الوقت نفسه، أفرزت كميات أقل من جزيئات معروفة بإضعاف الخلايا التائية أو تعزيز نمو الورم، مثل الجالاكتين-1، الجالاكتين-3، 4-1BB القابل للذوبان، IL-1α، والجليكوبروتين EMMPRIN/CD147. معاً، تشير هذه التغيرات إلى خلايا CAR-T أكثر عدوانية وأقل عرضة للكبت، مناسبة بشكل خاص لبيئات الورم العدائية ذات المستضدات الضعيفة.
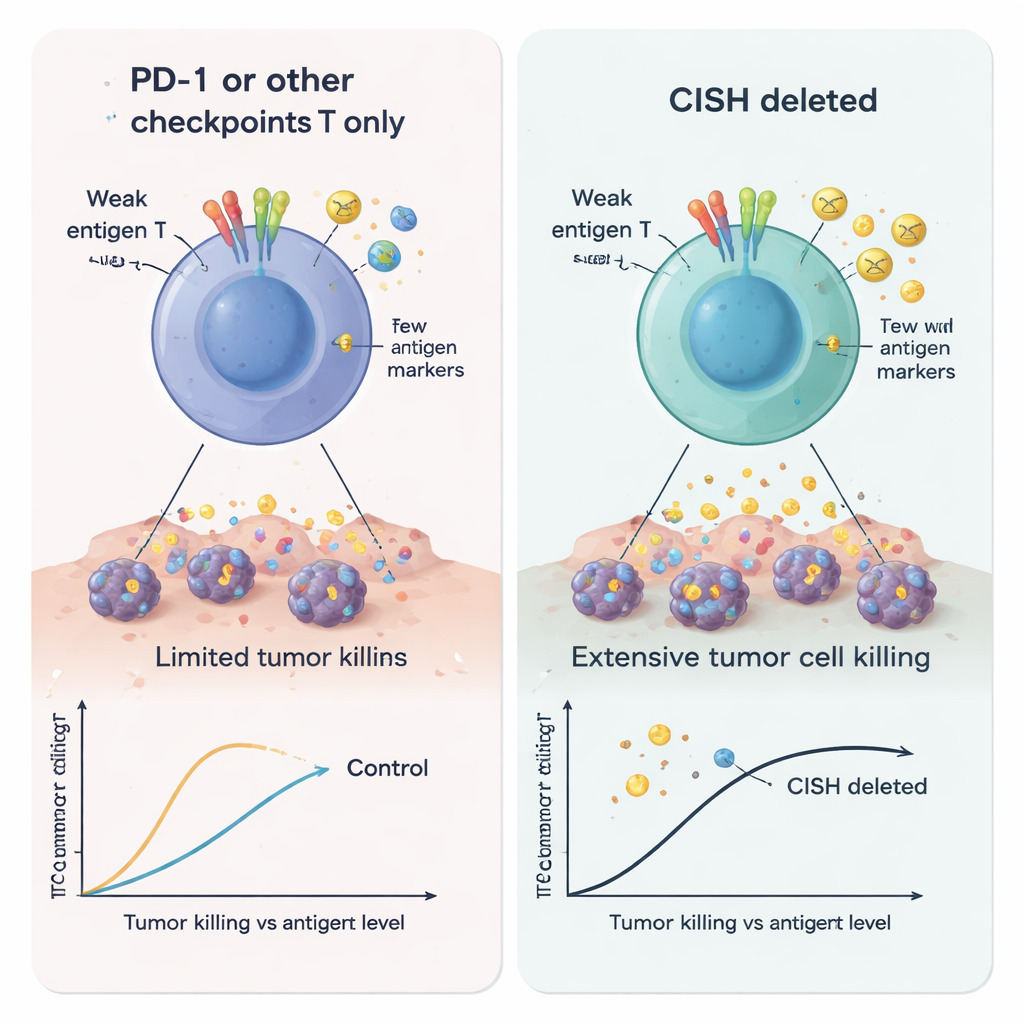
من حوض المختبر إلى المرضى
بعيداً عن أنابيب الاختبار والصحون الزرعية، وصلت فكرة استهداف CISH بالفعل إلى المرضى. أدت تجربة أولى على الإنسان باستخدام لمفاويات متسللة للورم محررة لحذف CISH في شخص مصاب بسرطان القولون والمستقيم المتقدم إلى استجابة كاملة استمرت لأكثر من عامين، على الرغم من مقاومة السرطان لعدة علاجات سابقة. من خلال إظهار أن CISH نقطة تفتيش داخلية قوية وقابلة للاستهداف دوائياً تزيد حساسية خلية تي حتى لإشارات الورم الباهتة، تساعد هذه الدراسة على تفسير تلك النتيجة السريرية اللافتة وتدعم الجهود لتطوير علاجات مستقبلية — سواء خلايا محررة جينياً أو حبوب — تخفف هذه الفرملة الداخلية بأمان وتوسع امتداد العلاج المناعي للسرطان.
الاستشهاد: Cano, F., Bravo-Blas, A., Colombe, M. et al. CISH, a key intracellular checkpoint, in comparison and combination to existing and emerging cancer immune checkpoints. Commun Biol 9, 319 (2026). https://doi.org/10.1038/s42003-026-09579-x
الكلمات المفتاحية: العلاج المناعي للسرطان, خلايا تي, علاج CAR-T, نقاط تفتيش مناعية, تحرير الجينات بـ CRISPR