Clear Sky Science · ar
طفرة ممرِضة في α‑SNAP تعيق ارتباط دهون الغشاء عبر إخفاء حلقة هيدروفوبية حاسمة
كيف يمكن لتغيير بروتيني طفيف أن يعطل تطور الدماغ
خلايا دماغنا تنقل باستمرار حمولة داخل فقاعات صغيرة تُدعى الحويصلات، ويُعد البروتين المساعد ألفا‑SNAP محورياً في إنجاز هذه التوصيلات. طفرة نادرة في ألفا‑SNAP، معروفة في سلالة فئران تُدعى «hyh»، تسبب مشاكل شديدة في تشكل الدماغ وتوازن السوائل. يطرح هذا العمل سؤالاً يبدو بسيطاً لكنه ذو عواقب كبيرة: هل ذلك التبديل الحرفي الوحيد في ألفا‑SNAP يمنعه من الالتصاق بغشاء الخلية، وهل قد يكون هذا سبباً رئيسياً لاضطراب نمو الدماغ؟
عامل رصيف خلوي يقوم بمهام متعددة
عادة يعمل ألفا‑SNAP كعامل رصيف للحويصلات، مساعداً إياها على الاندماج مع أغشية الخلايا حتى تُفرَج أو يُعاد تدوير الحمولات. يتعاون مع مجموعة بروتينات تُسمى SNAREs وماكينة مستهلكة للطاقة تُدعى NSF لسحب الأغشية معاً ثم إعادة ضبط النظام للجولة التالية. بخلاف دوره الكلاسيكي هذا، يشارك ألفا‑SNAP أيضاً في التحكم في عمليات مثل التنظيف الذاتي الخلوي (الالتهام الذاتي)، موت الخلايا، دخول الكالسيوم، واستشعار الطاقة. كل هذه الوظائف تعتمد بصورة أو بأخرى على قدرة ألفا‑SNAP على ملامسة والغوص جزئياً في السطح الدهني للأغشية.
حلقة مخفية وطفر ة مقلِقة
أعمال سابقة أظهرت أن ألفا‑SNAP يستخدم «حلقة» قصيرة دهنية قرب أحد طرفي البروتين لتتعلق بالأغشية. في البروتين السليم تبرز هذه الحلقة ويمكنها الغوص في الطبقة الخارجية للغشاء. في فأر hyh تم استبدال وحدة بناء واحدة في الوضع 105، مولدة طفرة M105I. استخدم المؤلفون محاكاة حاسوبية ليروا كيف يغيّر هذا التبديل شكل البروتين. وجدوا أن البروتين الطافي يصبح أكثر تراصّاً قليلاً ويميل للتواء بحيث تُطوى الحلقة الكارهة للماء إلى الداخل، مبتعدة عن الماء والأغشية. ونتيجة لذلك يقترب البروتين الطافي من الأغشية بزاوية أكثر انبساطاً ويميل إلى الضغط عليها بمنطقة أقل لزوجة، مما يقلل كلاً من وقت التماس وعمق الغوص. حسابات طاقة الارتباط دعمت هذا الاستنتاج: البروتين البري استقر في حالة طاقة منخفضة ومقيد بقوة، بينما فضّل الطافي اتصالات أضعف وأسطحاً أكثر سطحية.
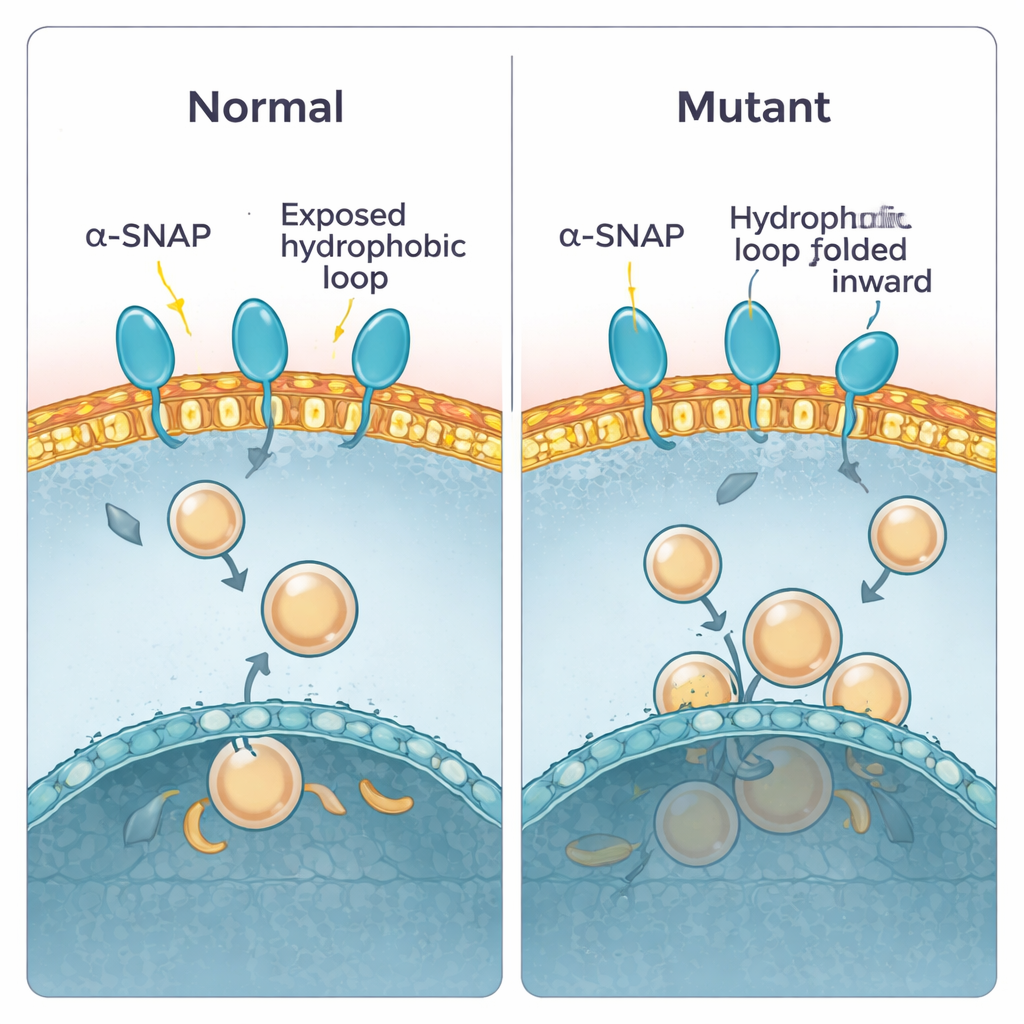
اختبار التنبؤ في المختبر
لفحص هذه التنبؤات، نقّى الفريق كلّاً من ألفا‑SNAP الطبيعي والمتغير واختبر سلوكهما في إعدادات تجريبية مختلفة. أولاً، استخدموا منظفاً يفصل إلى طور مائي وطور زيتي، مما يحاكي الاختيار بين الماء والغشاء. توزّع ألفا‑SNAP الطبيعي بالتساوي تقريباً، متسقاً مع سطح متوازن جزئياً دهني. النسخة الطافية كانت أقل ميلاً لدخول الطور الزيتي، ما يشير إلى أن أجزائها الدهنية مدفونة أكثر بالفعل. بعد ذلك، سمحوا للبروتينات بالتفاعل مع «صفائح» غشاء بلازمي مسطحة مُحضّرة من خلايا وصوّروا عدد بقع الارتباط. مرة أخرى، كان ألفا‑SNAP الطبيعي منتشر النطاق على الغشاء، بينما ارتبط الطافي بنسبة أقل بكثير. أخيراً، حرّكوا فقاعات غشائية اصطناعية (ليبوزومات) مصنوعة من دهون دماغية عبر تدرجات سكرية. ارتقى ألفا‑SNAP البري مع الحويصلات الغنية بدهون الغشاء البلازمي، بينما تخلّف الطافي، إذ ارتبط بشكل ضعيف إلا عندما صُنعت الحويصلات من مزيج غشائي داخلي مختلف.
العواقب في الدماغ النامي
انتقل الباحثون بعد ذلك إلى أدمغة أجنة الفئران النامية، مركزين على مرحلة تكون فيها خلايا عصبية جديدة. عبر فصل محتويات الخلايا إلى مجموعات ذائبة ومتحارضة بالغشاء، أظهروا أن مستويات ألفا‑SNAP الكلية كانت منخفضة بالفعل في أدمغة hyh، لكن الأهم من ذلك أن الكسر المتعلق بالارتباط بالأغشية كان منخفضاً بشكل غير متناسب مقارنة بالفئران الطبيعية. عندما فصلوا أنواع الأغشية المختلفة، وجدوا أن أكبر خسارة كانت في الغشاء البلازمي، السطح الخارجي للخلية، بينما كانت الأغشية الداخلية متأثرة بدرجة أقل بكثير. أخبرتهم الميكروسكوبية نفس القصة: في النسيج الطبيعي، كان ألفا‑SNAP يحدّد الخلايا بنمط قرص العسل المتوافق مع علامة سطح معروفة. في أدمغة hyh، تلاشى هذا التلوين الحاد للحافة وتحول إلى توهّج داخلي أكثر تباعداً، مما يدل على أن البروتين الطافي يفشل في البقاء مثبتاً على حافة الخلية حيث يكون اندماج الحويصلات والإشارات في أشد نشاطهما.
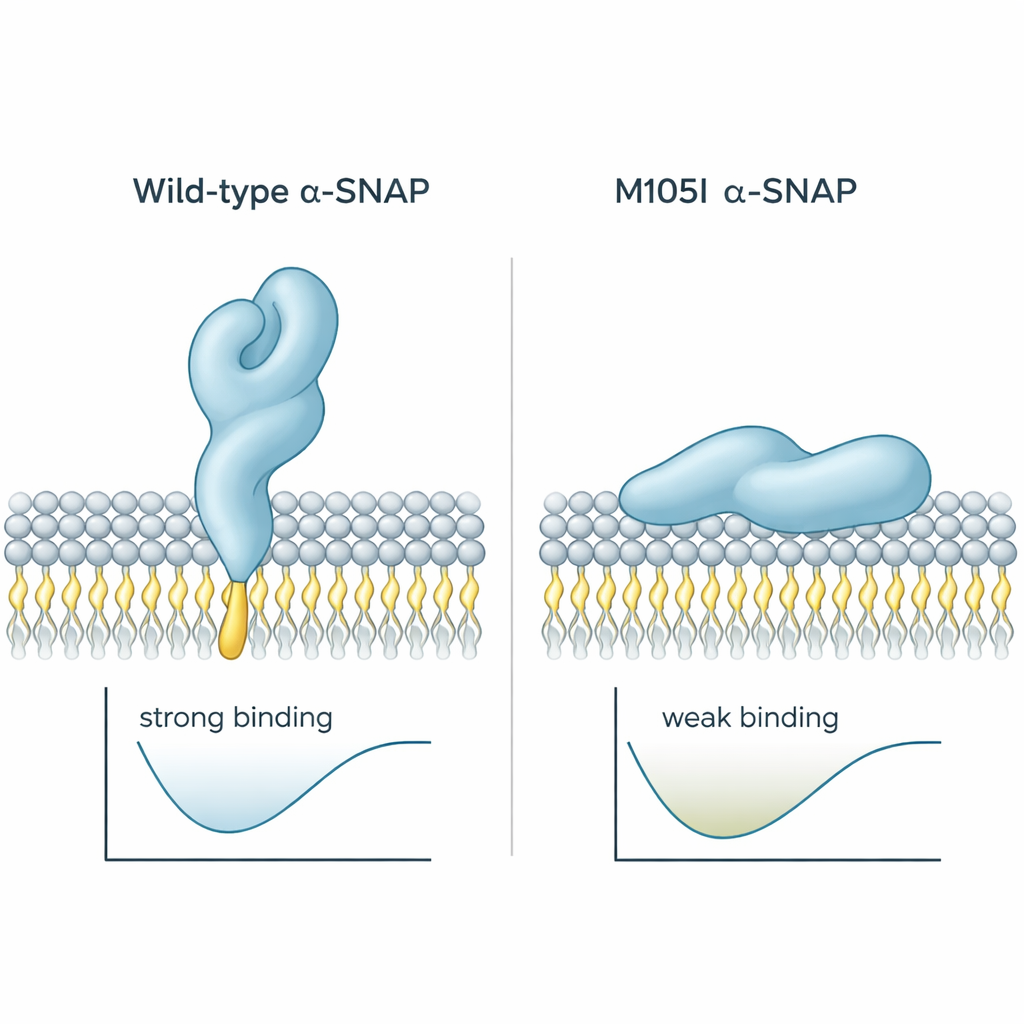
لماذا يهم ذلك للمرض
تُظهر النتائج مجتمعة أن طفرة M105I تفعل أكثر من مجرد خفض كمية ألفا‑SNAP؛ إنها تغيّر طيّ البروتين بحيث تُخفى حلقة القبض الحيوية على الغشاء. يجعل هذا من الأصعب على ألفا‑SNAP الإمساك بالغشاء البلازمي وتبني الوضعية الملائمة لتنظيم آليات الاندماج. في دماغ نامٍ، حيث يكون التوصيل الدقيق للإشارات ومواد البناء على سطح الخلية أمراً أساسياً، من المحتمل أن تساهم هذه الخللة الهيكلية الطفيفة في الاستسقاء الدماغي، وسوء توصيل القشرة، والعيوب الأخرى المرصودة في فئران hyh. للقراء غير المتخصصين، الرسالة واضحة: حتى تغيير بسيط في شكل بروتين واحد يمكن أن يعيد تشكيل طريقة تواصل الخلايا وبالتالي طريقة بناء الدماغ.
الاستشهاد: Méndez-Ruette, M., Bedoya, M., Hinrichsen, B. et al. A pathogenic mutation in α-SNAP impairs membrane lipid binding by concealing a critical hydrophobic loop. Commun Biol 9, 294 (2026). https://doi.org/10.1038/s42003-026-09578-y
الكلمات المفتاحية: ألفا‑SNAP, الارتباط بالغشاء, طفرة بروتينية, تطوّر الدماغ, اندماج الحويصلات