Clear Sky Science · ar
تطوير روابط بروهيبتين مشتقة من الكابسيسين للتأثير على تفاعل كيناز أوروورا A/PHB2 والميتوفاجي في خلايا السرطان
لماذا تهم مادة من الفلفل الحار في السرطان
يعزى إحساس الحرقة للفلفل الحار إلى الكابسيسين، وهي جزيء صغير يرتبط ببروتينات في خلايانا. تستكشف هذه الدراسة منعطفًا مفاجئًا لذلك التوابل المألوفة: أعاد الباحثون تصميم الكابسيسين لصنع جزيئات شبيهة بالأدوية تستهدف «محطات الطاقة» في خلايا السرطان — الميتوكوندريا — وتعتدل عملية تستخدمها تلك الخلايا للحفاظ على مصانع الطاقة في حالة جيدة. وبما أن خلايا السرطان تعتمد كثيرًا على ميتوكوندريات فعالة لتغذية نموها السريع، فإن القدرة على تعطيل هذا النظام الداعم بشكل انتقائي قد تفتح مسارًا جديدًا للعلاجات المضادة للسرطان.
محطات طاقة الخلية وطاقم التنظيف الداخلي لها
توازن الميتوكوندريا باستمرار بين بناء وحدات جديدة وإعادة تدوير الوحدات التالفة. الجانب المعني بإعادة التدوير، المسمى الميتوفاجي، يعمل كنظام مراقبة جودة: تُوسَم الميتوكوندريا البالية وتُحلّل بينما تبقى الأكثر صحة. تستولي العديد من خلايا السرطان على هذا التوازن، وتستخدم الميتوفاجي للتخلص من الميتوكوندريات الضعيفة وتخصيب «الأداء العالي» منها التي تنتج كميات كبيرة من ATP، عملة طاقة الخلية. وُجد مؤخرًا أن بروتينًا يدعى كيناز أوروورا A (AURKA)، الذي يُنتج بكمية زائدة في الأورام، يتواجد داخل الميتوكوندريا حيث يتعاون مع بروتين آخر، بروهيبتين‑2 (PHB2)، ومواءم البلعمة الذاتية LC3. معًا يشكلون معقدًا يعزز الميتوفاجي ويدعم إنتاج الطاقة العالي في خلايا السرطان.
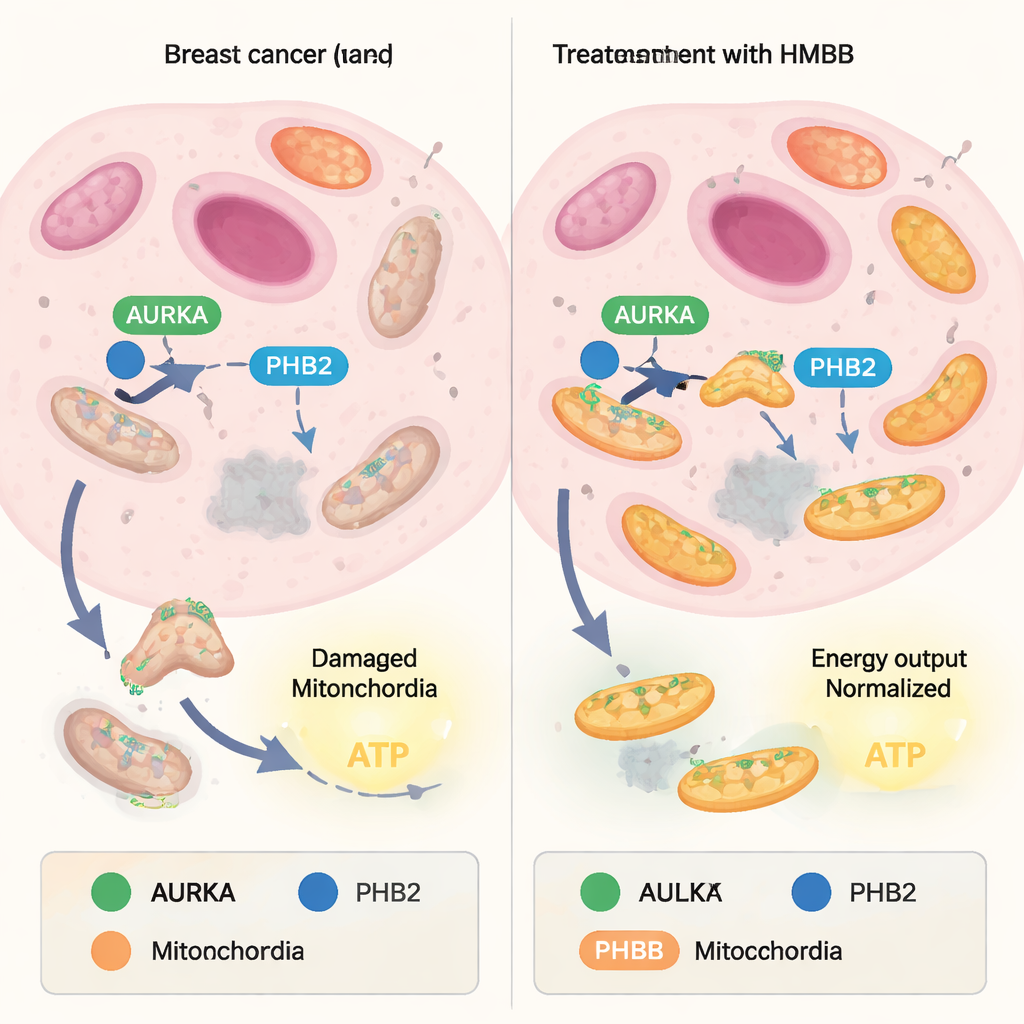
من الكابسيسين الحار إلى أدوات جزيئية مصممة
أعمال سابقة أظهرت أن مركبًا طبيعيًا يدعى زانثوهومولون يمكنه الارتباط بـ PHB2 وتعطيل معقد AURKA–PHB2–LC3، مما يوقف الميتوفاجي ويخفض إنتاج ATP الميتوكوندري. ومع ذلك، فإن البنية الكيميائية لزانثوهومولون ليست مثالية لتطوير الأدوية. في هذه الدراسة، لجأ المؤلفون إلى الكابسيسين، وهو رابط طبيعي آخر لـ PHB، وتسائلوا عما إذا كان يمكن إعادة تشكيله إلى أدوات أكثر عملية. أكدوا أولًا أن الكابسيسين يضعف قليلاً التفاعل بين AURKA وPHB2 في خلايا سرطان الثدي الحية، باستخدام تقنية تصوير (FRET/FLIM) تقيس مدى قرب بروتينين موسومين من بعضهما. ثم صنّعوا 16 جزيئًا مستوحى من الكابسيسين عن طريق تعديل «الذيل» و«الرأس» العطري في البنية الأصلية، واختبروا بشكل منهجي كيف أثر كل نسخة على شراكة AURKA–PHB2 داخل الميتوكوندريا.
اكتشاف «لاصق» جزيئي يربط البروتينات معًا
أظهرت الجزيئات المعدلة تأثيرات مختلفة بشكل لافت. بعضها، مثل الكابسيسين نفسه أو مشتق يدعى المركب 5، جعل AURKA وPHB2 ينفصلان بسهولة أكبر. والبعض الآخر لم يفعل شيئًا تقريبًا. إلا أن مجموعة فرعية — وخاصة جزيء أُطلق عليه المركب 13، ولاحقًا اسم HMBB — كان لها التأثير المعاكس وشَدَّت الترابط بين AURKA وPHB2 بشكل ملحوظ. ساعدت محاكاة الالتحام الحاسوبي في تفسير هذا السلوك. كان الكابسيسين والمركب 5 يميلان إلى الاندساس في الموقع النشط لـ AURKA بطرق تخلق اصطدامات مادية مع PHB2، مما يدفع البروتينين بعيدًا عن بعضهما. بالمقابل، دخلت المركبات 12 و13 في الموقع النشط لـ AURKA وتلامست في الوقت ذاته مع جيب تثبيطي معروف على PHB2 دون إحداث اصطدام. بدلاً من ذلك، سمحت أشكالها أن تعمل كـ «لاصق جزيئي»، جاعلة جسرًا بين AURKA وPHB2 ومُثبِّتةً المعقد.
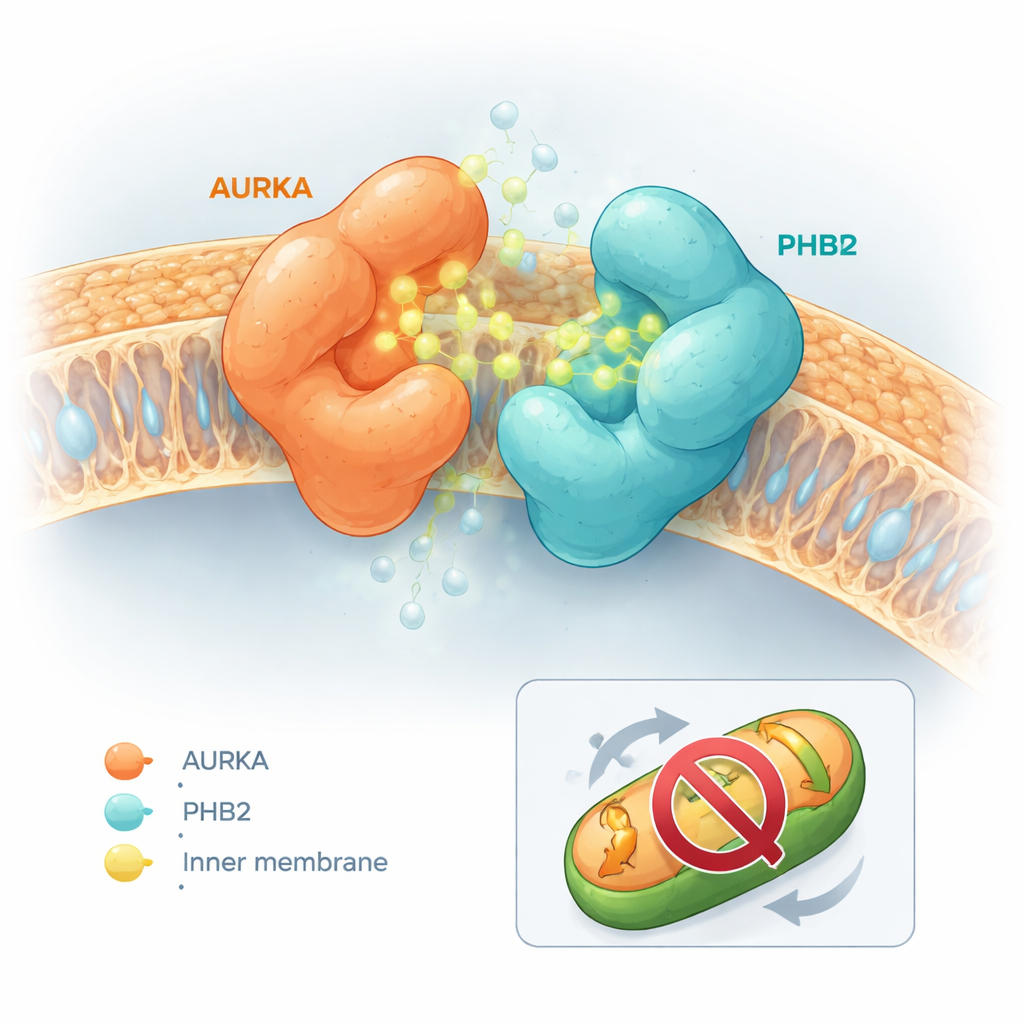
حجب التنظيف الميتوكوندري دون إيقاف مركز التحكم في الخلية
كان سؤال محوري هو ما إذا كان سلوك اللصق الجزيئي هذا يعطل AURKA في كل أنحاء الخلية، وهو ما قد يسبب آثارًا جانبية واسعة، أم أنه يعمل بشكل أكثر انتقائية. باستخدام جهاز استشعار فلوري منفصل يبلغ عن تنشيط AURKA عند المراكز الصنوية — البُنى التي تنظم آلية انقسام الخلية — لاحظ الفريق أن HMBB لم يخفّض نشاط AURKA في هذه المواقع. ومع ذلك، في اختبارات ميتوكوندرية، عكس HMBB فقدان كتلة الميتوكوندريا الذي يسببه عادة فرط إنتاج AURKA في خلايا سرطان الثدي. في الخلايا التي تصنع مستويات عالية من AURKA بطبيعتها، زاد HMBB المحتوى الميتوكوندري، مما يدل على أن الميتوفاجي المدفوع بـ AURKA تم حجبه. وفي الخلايا ذات مستويات منخفضة من AURKA، لم يكن لـ HMBB تأثير كبير، مما يبرز اعتماده على مسار AURKA–PHB2.
ماذا قد يعني هذا لعلاجات السرطان المستقبلية
تُظهر النتائج مجتمعة أن مشتقات الكابسيسين المصممة بعناية يمكن أن تضبط بدقة كيفية تفاعل AURKA وPHB2 داخل الميتوكوندريا. من خلال العمل كلاصق جزيئي، يقفل HMBB ومركبات مشابهة AURKA وPHB2 معًا في تكوين يمنع البرنامج الاعتيادي للميتوفاجي من المضي قدماً، دون إيقاف أدوار AURKA الأساسية في أماكن أخرى من الخلية. للمختصر المفهوم للقارئ العام، الفكرة الرئيسية هي أن المؤلفين أنشأوا جزيئات نموذجية تتداخل بشكل انتقائي مع كيفية حفاظ خلايا السرطان على محطات طاقتها، مما قد يضعف إمدادها بالطاقة مع الحفاظ على وظائف الخلايا الطبيعية. ورغم أن هذه المركبات لا تزال في مرحلة مختبرية مبكرة، فإنها توضح استراتيجية واعدة: استخدام جزيئات صغيرة شبيهة بالأدوية لاستهداف شراكات بروتينية محددة داخل الميتوكوندريا وبالتالي تقويض المزايا الأيضية التي تعتمد عليها العديد من الأورام.
الاستشهاد: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
الكلمات المفتاحية: ميتوكوندريا, ميتوفاجي, كيناز أوروورا A, مشتقات الكابسيسين, أيض السرطان