Clear Sky Science · ar
إعادة تقييم خصوصية عناصر استجابة بروتين Gα في إشارة GPCR
لماذا تهم هذه المحولات الخلوية الصغيرة الطب
تعمل كثير من الأدوية الحالية عن طريق قلب «مفاتيح» جزيئية على سطح خلايانا تُدعى مستقبلات مقترنة ببروتين G أو GPCR. تنقل هذه المفاتيح الرسائل إلى داخل الخلية عبر بروتينات مساعدة تُعرف ببروتينات G وفي النهاية تشغّل أو تطفئ جينات. لعقود، اعتمد الباحثون على اختبارات بسيطة تُنتج ضوءًا لرصد أي بروتينات G يستخدمها دواء أو مستقبل معين. تطرح هذه الدراسة سؤالًا أساسيًا لكنه حاسم: هل تخبرنا هذه الاختبارات بالفعل بما نعتقد؟ وهل يمكن أن نثق بها عند تصميم جيل جديد من الأدوية الدقيقة؟
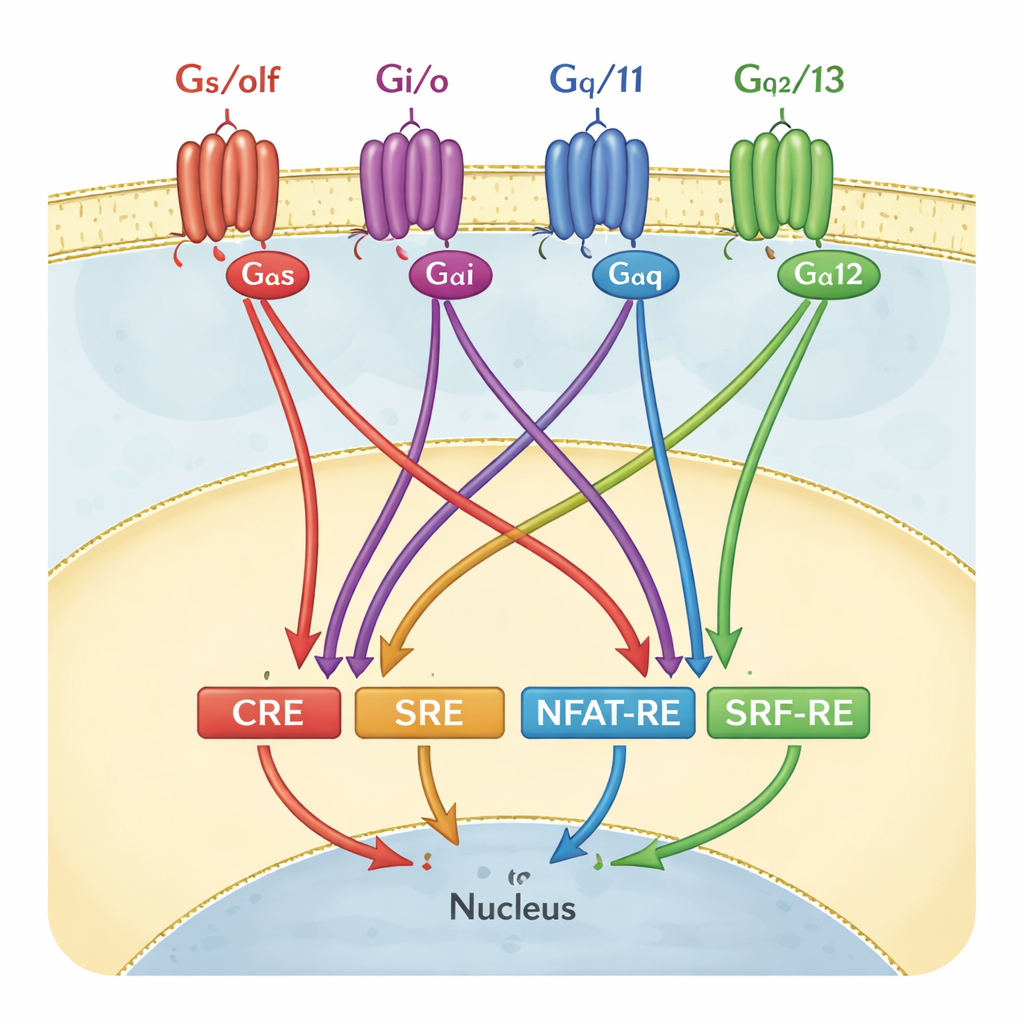
كيف يقرأ العلماء عادة إشارات GPCR
لتتبع نشاط GPCR، تستخدم مختبرات كثيرة تجارب جينات مراسلة. في هذه الاختبارات، تُهندَس الخلايا بحيث تضيء عندما يُنشَّط مفتاح جيني معين أو «عنصر استجابة». أربعة من هذه العناصر شائعة جدًا: CRE وSRE وNFAT‑RE وSRF‑RE. لطالما عُومِل كل منها كبديل لفرع واحد من إشارة بروتين G—على سبيل المثال CRE لعائلة Gαs/olf، أو SRF‑RE لعائلة Gα12/13. في الكتب الدراسية ومسارات الفحص، تُرسم هذه الأزواج غالبًا كما لو كانت مخططات توصيل واحد لواحد: شغّل بروتين G محدد، ولن يضيء إلا مرسل واحد.
اختبار مخطط التوصيل القديم
تحدى المؤلفون هذه الصورة بشكل منهجي باستخدام خلايا بشرية من نوع HEK293 حُذِفت فيها عائلات بروتين G محددة—أو حتى جميع بروتينات G—بتحرير جيني. ثم أعادوا إدخال أنواع بروتين G واحدة تلو الأخرى. في هذه الخلايا عبّروا عن تسعة مستقبلات GPCR مختلفة، اختيرت لتمثيل مستقبلات تُشير إما بشكل انتقائي أو عبر عدة شركاء من بروتين G. بقياس مدى توهج كل من المراسلين الأربعة عبر تراكيز دوائية متعددة، تمكنوا من رؤية أي بروتينات G كانت مطلوبة فعليًا لكل عنصر استجابة، وأيها يمكن أن تساهم بشكل غير مباشر.
مسارات متداخلة بدلًا من قنوات نظيفة
تقلب النتائج نموذج «مستقبل واحد—مراسل واحد» النظيف. بينما بقي CRE يعتمد أساسًا على بروتينات Gαs/olf—المسار الكلاسيكي لرفع cAMP—يمكن لعائلات بروتين G أخرى أن تؤثر بشكل ملحوظ في نشاط CRE، لكن فقط عندما يتواجد Gαs/olf. بالنسبة للمراسلين الثلاثة الآخرين، SRE وNFAT‑RE وSRF‑RE، برزت عائلة Gαq/11 كسائق رئيسي، رغم أن SRE وSRF‑RE كانت مرتبطة تقليديًا بفروع أخرى من بروتين G. تصرّف SRE وSRF‑RE بشكلٍ مشابه بشكل خاص، مما يشير إلى أنهما يستندان إلى آليات مشتركة لاحقة بدلًا من طرق منفصلة ومنعزلة. في كثير من الحالات، قدمت بروتينات G إضافية مثل Gα12/13 وGαi/o دفعًا إضافيًا أو نشاطًا خلفيًّا، مما يبرز شبكة من التداخل بدلًا من قنوات منفصلة.
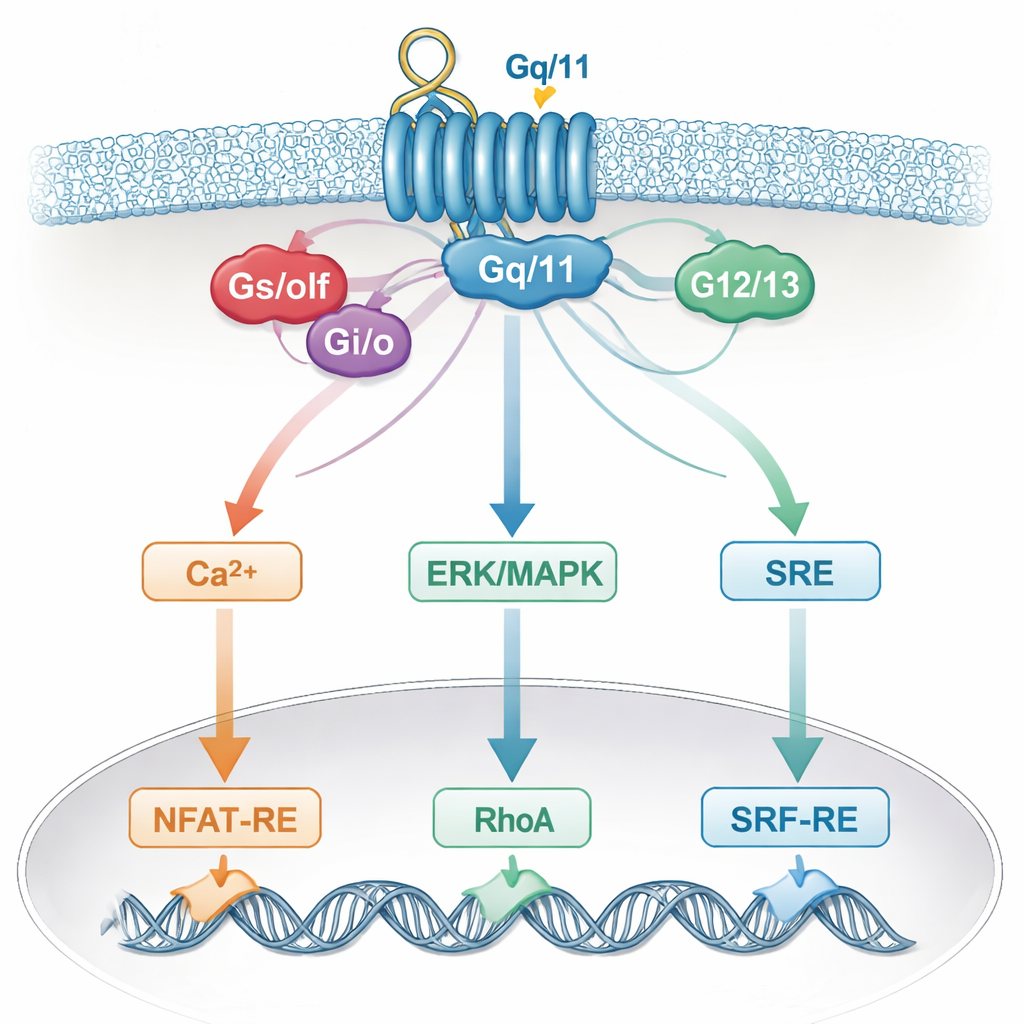
لماذا تغمّ الشبكة الخلوية قراءاتنا
تعكس هذه الضبابية في الخصوصية على الأرجح كيف تدمج الخلايا الحقيقية الإشارات. يمكن لمستقبل واحد أن ينشط بروتينات G متعددة، والتي تتقارب بعد ذلك على مراسلات مشتركة مثل الكالسيوم أو ERK/MAPK أو RhoA أو cAMP، وعلى مساعدات مشتركة مثل وحدات Gβγ. وهذه المسارات المشتركة تغذي بدورها نفس مفاتيح الجينات في النواة. ونتيجة لذلك، يُصبح المراسل الذي كنا نعتقد أنه يستجيب لعائلة واحدة من بروتين G «يستمع» فعليًا إلى عدة عائلات. تضيف عوامل خاصة بنوع الخلية والمجموعة الدقيقة من المستقبلات الموجودة مزيدًا من التعقيد، ما يعني أن الاستنتاجات المستقاة من نظام خلوي واحد قد لا تنطبق في نظام آخر.
ما يعنيه هذا لاكتشاف الأدوية
الخلاصة لغير المتخصصين هي أن العديد من اختبارات GPCR القائمة على الوميض المستخدمة على نطاق واسع أقل خصوصية مما تدل عليه تسمياتها. لا تزال هذه الاختبارات تفيد في إظهار أن مستقبلًا ما نشط وتحديد المسارات الواسعة المشاركة تقريبًا، لكنها ليست دليلًا موثوقًا على أن عائلة بروتين G محددة—وفقط تلك العائلة—هي المعنية. يجادل المؤلفون بأن على الباحثين ومطوري الأدوية اعتبار هذه المراسلين مؤشرات خشنة وإقرانهم بأساليب أكثر مباشرة تراقب تفاعلات البروتينات في الوقت الحقيقي. ستعطي هذه المقاربة صورة أصح عن كيفية توجيه الأدوية المحتملة لإشارات الخلية، وتساعد على تجنب اختصارات مضللة في السعي نحو علاجات أكثر أمانًا واستهدافًا.
الاستشهاد: Saito, A., Kise, R., Yamaguchi, S. et al. Re-evaluating Gα protein–response element specificity in GPCR signaling. Commun Biol 9, 288 (2026). https://doi.org/10.1038/s42003-026-09569-z
الكلمات المفتاحية: إشارة GPCR, بروتينات G, اختبارات المراسل, شبكات إشارة الخلية, اكتشاف الأدوية