Clear Sky Science · ar
العلاج الديناميكي المحفز بالنظائر الإشعاعية يحفّز مسارات وفاة خلوية مكملة من النيكروبْتوسيس والموت المبرمج في السرطان
قلب حيل السرطان ضده
السرطان سيئ السمعة في التملص من أفضل علاجاتنا، خصوصًا في الأورام العدوانية للثدي التي تنتشر في الجسم. تستكشف هذه الدراسة نهجًا مبتكرًا يُسمى العلاج الديناميكي المحفز بالنظائر الإشعاعية (RaST)، والذي يستخدم متعقبات التصوير الطبي وجسيمات نانوية حساسة للضوء لقتل خلايا السرطان بطرق توقظ جهاز المناعة أيضًا. يهم هذا العمل القراء لأنه يقترح كيف يمكن إعادة توظيف أدوات التصوير الحالية ومواد ذكية لخلق ضبط للسرطان مدفوع بالمناعة يدوم أطول بدلًا من انكماشات مؤقتة للأورام.
طريقة جديدة لإنارة الأورام من الداخل
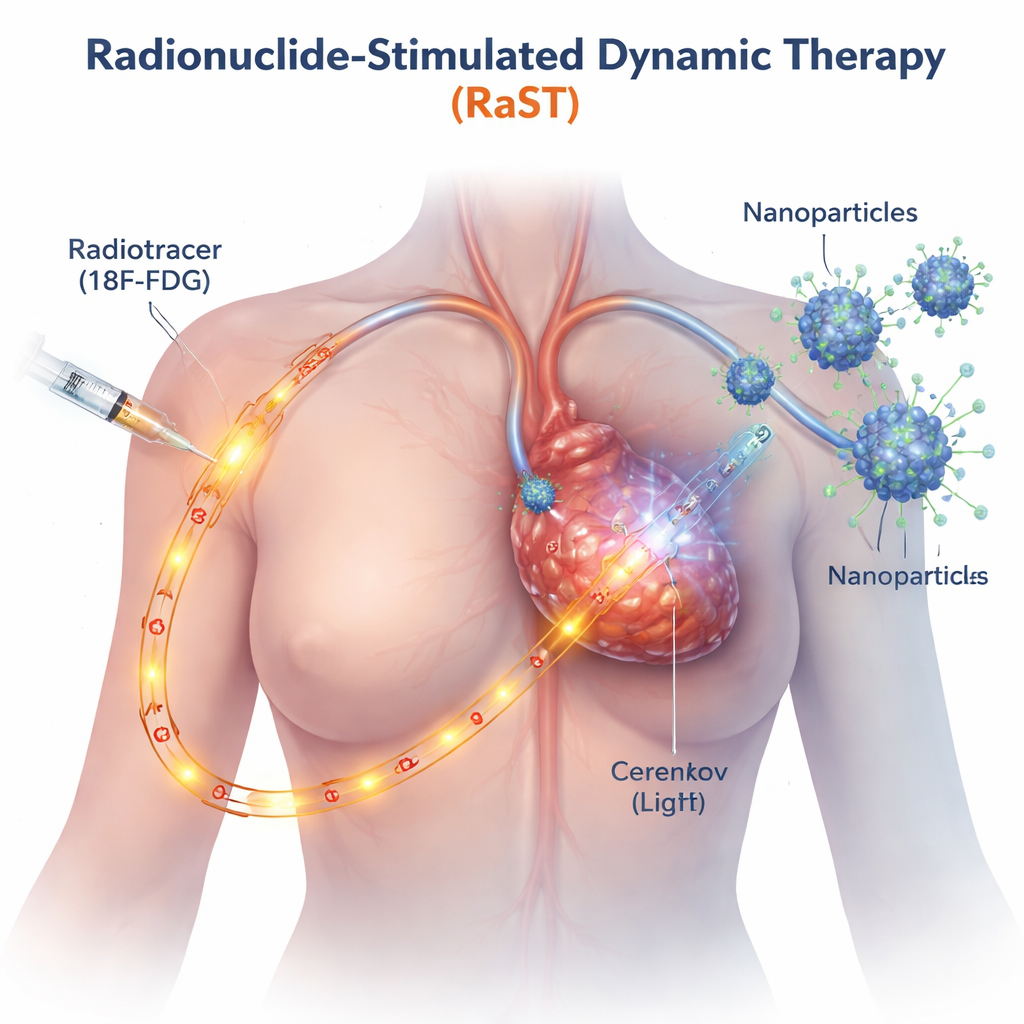
تعمل العلاجات التقليدية المعتمدة على الضوء فقط حيث يصل شعاع خارجي، مثل الجلد أو الأورام السطحية. يتجاوز RaST هذا القيد باستخدام سكر مشع، شبيه بالمتعقب المستخدم في فحوص PET، والذي يتجمع بشكل طبيعي في الخلايا السرطانية سريعة النمو. أثناء عبور هذا المتعقب عبر الورم، ينبعث منه بريق أزرق خافت يعرف بإشعاع شيرنكوف. صمّم الباحثون جسيمات نانوية صغيرة من ثاني أكسيد التيتانيوم مغلفة ببروتين يستهدف السرطان بحيث تتجه أيضًا إلى الورم. عندما يلتقي المتعقب والجسيمات النانوية، يشغّل الضوء الداخلي الجسيمات، التي تنتج بدورها دفعات من جزيئات أكسجين تفاعلية—جزيئات شديدة التفاعل تتلف خلايا السرطان من الداخل.
إطلاق مسارين مميزين للموت الخلوي
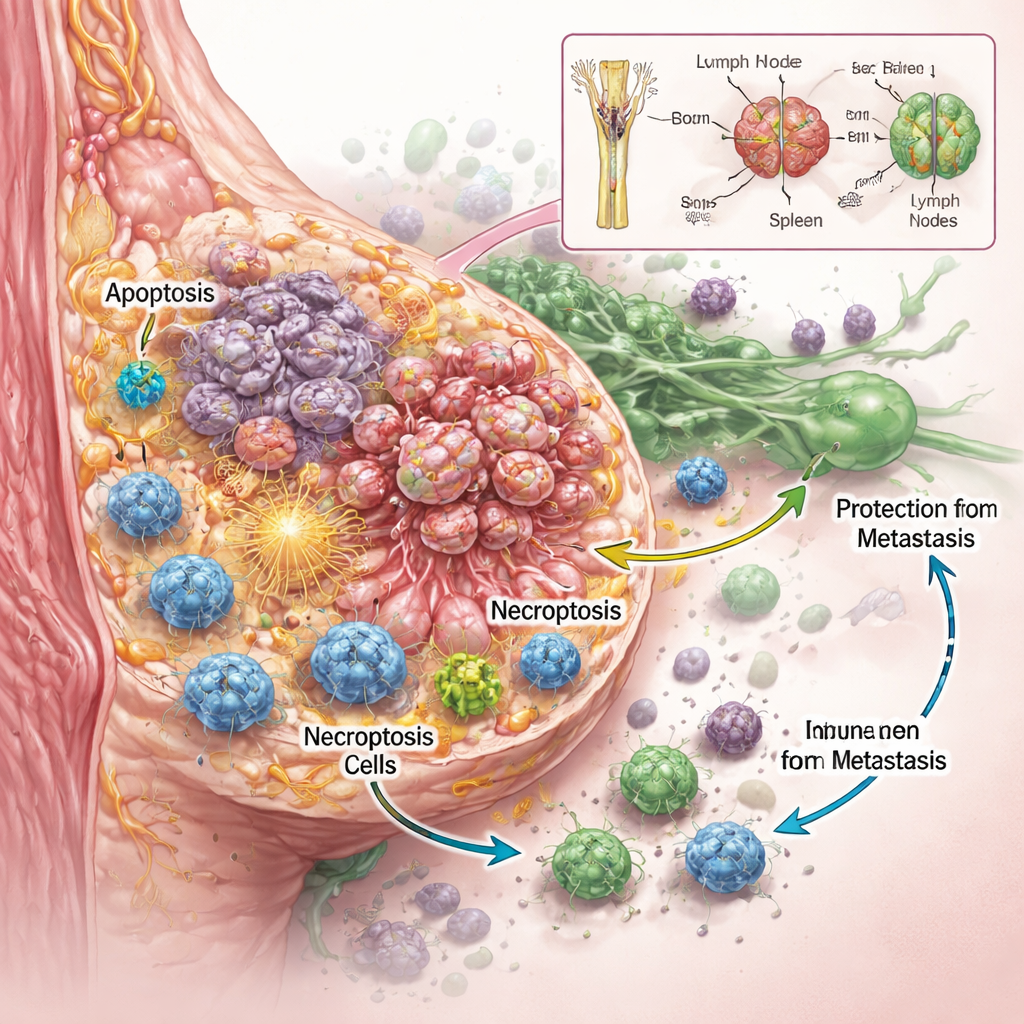
أراد الفريق أن يعرف ليس فقط ما إذا كان RaST يقتل خلايا السرطان، بل كيف يفعل ذلك. باستخدام عدة سلالات خلوية عدوانية من سرطان الثدي في المختبر، وجدوا أن جرعات مضبوطة بعناية من المتعقب المشع والجسيمات النانوية تعمل معًا لإتلاف خلايا الورم بشكل أكثر فعالية من كل مكوّن بمفرده، حتى في أنواع معروفة بمقاومتها للعلاج الكيميائي القياسي. كشفت صور مفصّلة وقياسات بروتينية أن RaST فعّل برنامجين منظمين للموت الخلوي في آنٍ واحد. أحدهما هو الاستماتة (apoptosis) التي تُوصف غالبًا بـ«الانتحار الخلوي»، حيث تفكك الخلايا نفسها بطريقة منظمة. والآخر هو النيكروبْتوسيس (necroptosis)، شكل أكثر انفجارًا للموت الخلوي حيث تنتفخ الخلايا، وتمزق، وتفرز إشارات جزيئية للضرر إلى محيطها. يمكن أن تعمل هذه الإشارات، المعروفة بالجزيئات المرتبطة بالضرر والسيتوكينات الالتهابية، كمنارات تجذب وتفعّل خلايا الجهاز المناعي.
تجنيد الجهاز المناعي للسيطرة الدائمة
لفهم ما إذا كان لهذا النمط الالتهابي في قتل الورم أثر في الكائنات الحية، اختبر الباحثون RaST في نماذج فأرية من سرطان الثدي. في الفئران التي تفتقر إلى دفاعات مناعية رئيسية، لم يفعل RaST الكثير لإيقاف نمو الورم أو انتشاره إلى الرئتين، رغم توليده لكمية كبيرة من الموت الخلوي المحلي. لكن في الفئران ذات الجهاز المناعي السليم، أدى العلاج نفسه إلى استجابات جزئية وكاملة للأورام ومنع النقائل إلى الرئتين. امتلأت الأورام المعالجة بـRaST بخلايا مناعية—وخاصة الخلايا النخاعية مثل البلعميات والخلايا الشجيرية—الماهرَة في التهام المواد الميتة وعرض شظايا الورم للخلايا التائية. أظهرت اختبارات الدم موجات من إشارات منشطة ومنظمة للمناعة مع مرور الوقت، ما يوحي بأن RaST يطلق هجومًا مناعيًا مبدئيًا ثم يتحول لاحقًا إلى حالة أكثر توازنًا مع تقلص الأورام أو استقرارها.
مطاردة البقايا المخفية والحماية من الانتكاس
حتى في الفئران التي بدا أن الأورام قد شُفيت تمامًا بواسطة RaST، كشفت صبغة تصوير حساسة للغاية لاحقًا جيوبًا صغيرة من خلايا سرطانية متبقية مخبأة داخل العقد اللمفاوية. وبشكل ملحوظ، لم تُطوِّر هذه الحيوانات أورامًا جديدة أو نقائل بعيدة على مدى شهور عديدة. أظهرت التحليلات الكيميائية أن جسيمات ثاني أكسيد التيتانيوم، التي كانت وفيرة أولياً في العظام والكبد، أُعيد توزيعها تدريجيًا إلى الطحال والعقد اللمفاوية—وبالضبط المراكز التي يجوبها فيها الخلايا المناعية. ربما تحافظ هذه الهجرة البطيئة على مصدر محلي من الأكسجين التفاعلي متاحًا للخلايا المناعية، مما يساعدها على التعرف على هذه البقايا السرطانية الخفيّة والسيطرة عليها قبل أن تنمو أو تنتشر مجددًا.
ماذا قد يعني هذا لرعاية السرطان المستقبلية
بعبارات بسيطة، يُظهر هذا العمل أن RaST أكثر من مجرد وسيلة لتسميم خلايا الورم. من خلال الجمع بين المتعقبات المشعة، والجسيمات النانوية المستجيبة للضوء، ودفاعات الجسم الذاتية، يدفع هذا النهج خلايا السرطان إلى شكلين من الموت المبرمج الذي ينبه الجهاز المناعي بقوة. في الحيوانات ذات المناعة السليمة، يؤدي ذلك إلى ضبط دائم للأورام العدوانية في الثدي ويمنع النقائل، حتى عندما تبقى بضع خلايا سرطانية في العقد اللمفاوية. بينما يبقى الكثير على الطريق قبل أن يُختبر هذا النهج على نطاق واسع في البشر، تشير الدراسة إلى علاجات مستقبلية لا تهدف ببساطة إلى تقليص الأورام، بل إلى إعادة تشكيل العلاقة بين السرطان والموت الخلوي والمناعة بحيث يساعد الجسم على إبقاء المرض تحت السيطرة على المدى الطويل.
الاستشهاد: Egbulefu, C., Black, K., Su, X. et al. Radionuclide-stimulated dynamic therapy induces complementary immunogenic necroptosis and apoptosis cancer cell death pathways. Commun Biol 9, 275 (2026). https://doi.org/10.1038/s42003-026-09555-5
الكلمات المفتاحية: سرطان الثدي, جسيمات نانوية, العلاج المناعي, العلاج بالنظائر المشعة, النيكروبْتوسيس