Clear Sky Science · ar
تحسين توقع kcat من خلال آلية انتباه واعية للبقايا وتمثيلات مدرَّبة مسبقًا
لماذا تهم التوقعات الأسرع للإنزيمات
الإنزيمات هي القوى الصغيرة التي تُبقي الخلايا – بل والصناعات بأكملها – عاملة. تُسارع التفاعلات الكيميائية التي تدير أيضنا، وتُصنّع الأدوية، وتُحرّك عمليات تصنيع أكثر استدامة. الرقم الرئيس الذي يصف سرعة عمل الإنزيم يُعرف بعدد الدورة أو kcat. قياس kcat في المختبر بطيء ومكلف، لذلك يلجأ العلماء إلى الذكاء الاصطناعي لتوقعه من تسلسل البروتين ومعلومات التفاعل. تُقدّم هذه الدراسة نموذج PMAK الجديد، الذي لا يتنبأ بـ kcat بدقة أكبر من الأدوات السابقة فحسب، بل يساعد أيضًا في تحديد أي أجزاء الإنزيم هي الأكثر أهمية لنشاطه.
من العمل المعملي الشاق إلى التوقعات الذكية
تقليديًا، يتطلب تحديد kcat قياسًا دقيقًا لمقدار سرعة تحويل الإنزيم للرابط إلى المنتج تحت ظروف محكمة، مثل درجة حرارة ودرجة حموضة ثابتتين. إجراء هذا لآلاف الإنزيمات غير عملي، ما يحد من قدرتنا على نمذجة شبكات أيضية كاملة أو تصميم محفزات حيوية جديدة. حاولت طرق الحوسبة السابقة سد هذه الثغرة، لكن كثيرًا منها اعتمد على خصائص مصمَّمة يدويًا أو على تصور مبسّط للإنزيم وركيزة مفردة. كانت تعمل جيدًا غالبًا فقط عندما تكون الإنزيمات الجديدة مماثلة جدًا لما وُجد في بيانات التدريب، وكانت تعاني مع الإنزيمات الجديدة حقًا أو التفاعلات المختلفة أو الطفرات المهندَسة.
تعليم الحواسيب "لغة" الإنزيمات والتفاعلات
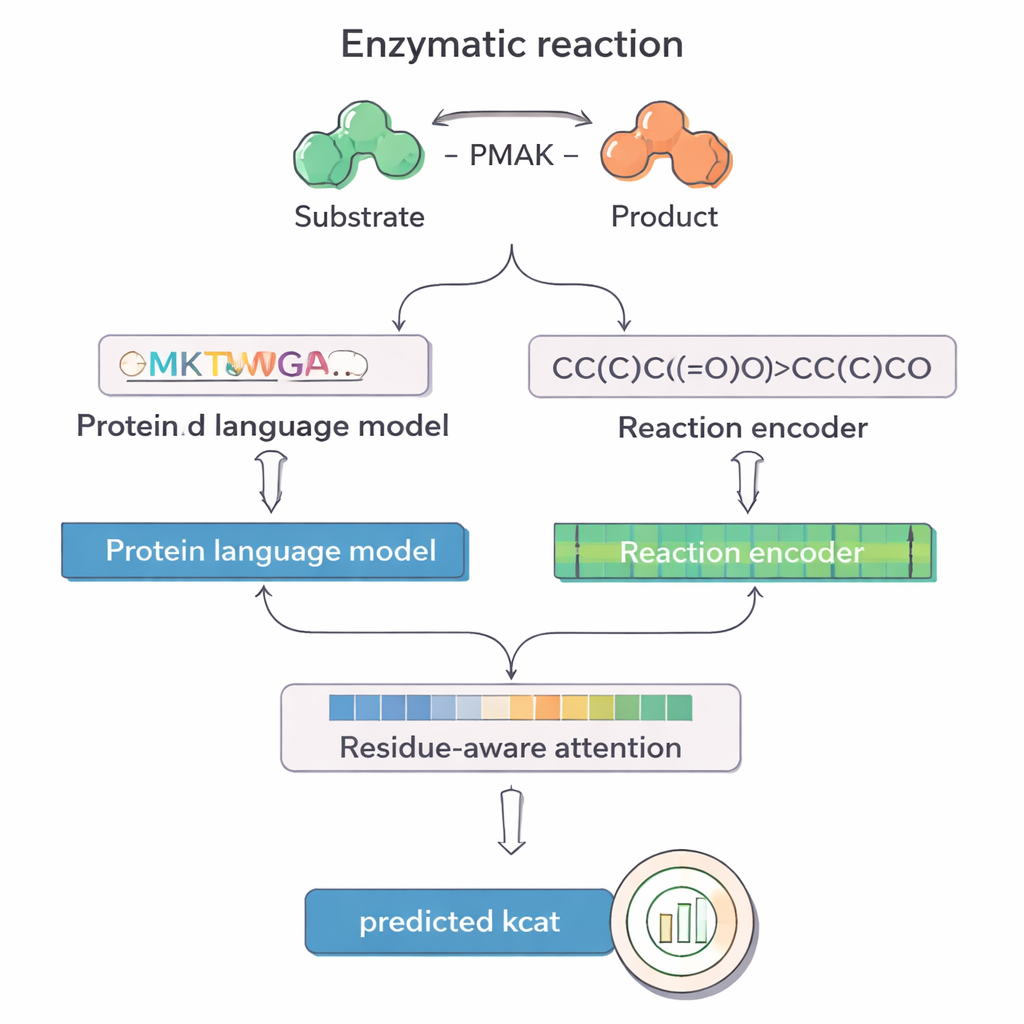
يستفيد PMAK من التقدّم الحديث في "نماذج اللغة" التي طُوّرت أصلاً للنصوص، لكن أعيد تدريبها على مجموعات هائلة من تسلسلات البروتين والتفاعلات الكيميائية. يحول نموذج واحد، يُسمى ProT5، تسلسل الأحماض الأمينية للإنزيم إلى تمثيل عددي غني يلتقط الأنماط المتعلمة من ملايين البروتينات. ونموذج آخر، RXNFP، يفعل الشيء نفسه للتفاعلات الكاملة المكتوبة كسلاسل SMILES، التي تشفّر جميع المتفاعلات والنواتج. يغذّي PMAK هذين التمثيلين المتعلَّمين إلى شبكة عصبية تُوائم أبعادهما وتتيح للنموذج أخذ كل من الإنزيم وسياق التفاعل الكامل في الاعتبار معًا، بدلًا من معالجتهما بشكل منفصل.
تسليط الضوء على أهم الوحدات البنائية
ابتكار مركزي في PMAK هو آلية "انتباه واعية للبقايا". بدلًا من معاملة كل حمض أميني في الإنزيم على أنه مهم على قدم المساواة، يتعلم النموذج إعطاء أوزان أعلى لبقايا معينة تهمها أكثر بالنسبة للتفاعل المعني. تعمل درجات الانتباه هذه ككشاف ضوء على التسلسل: عندما قارن الباحثون هذه الدرجات بالمواقع الفعّالة ومواقع الارتباط المعروفة من هياكل البروتين، وجدوا أن PMAK يبرز البقايا الوظيفية بوتيرة أعلى بكثير من الصدفة. كما أن النموذج آتى بنتائج جيدة حتى عندما عُرّفت المواقع الفعالة بشكل أوسع لتشمل البقايا المجاورة في الفراغ الثلاثي الأبعاد، مما يشير إلى أنه يلتقط إشارات بنيوية وكيميائية دقيقة ذات صلة بالتحفيز.
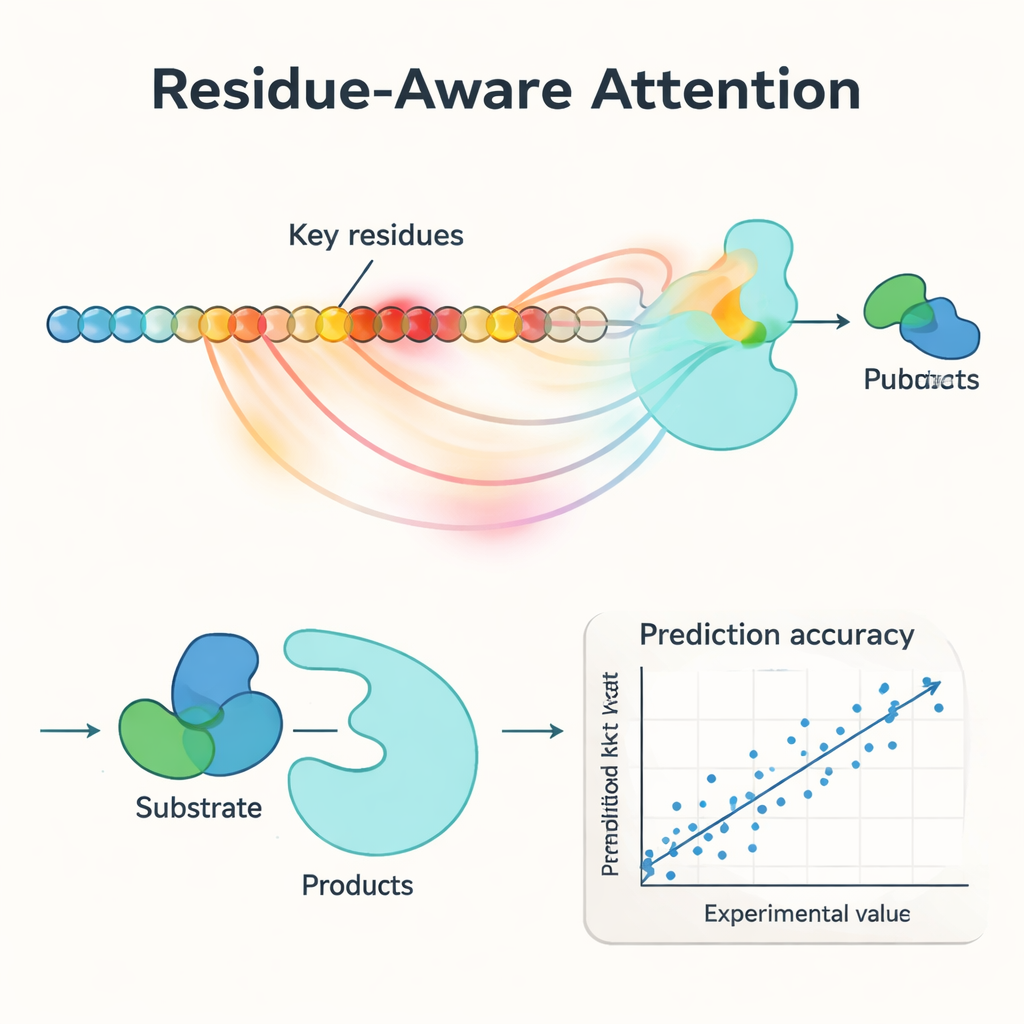
أداء جيد على إنزيمات جديدة وتفاعلات جديدة وطفرات
اختبر المؤلفون PMAK بدقّة على مجموعة بيانات مُنقّحة تضم أكثر من 4000 قيمة kcat تغطي ما يقرب من 3000 إنزيم و2800 تفاعل. تحت ظروف "البدء الدافئ" — حيث تظهر إنزيمات وتفاعلات مشابهة في مجموعتي التدريب والاختبار — طابق PMAK أو تفوّق على أفضل النماذج الموجودة. والأكثر إثارة للإعجاب، في اختبارات "البدء البارد" حيث كان أحد الإنزيمات أو التفاعلات في مجموعة الاختبار لم يُرَ من قبل، تفوّق PMAK على مجموعة من الطرق الرائدة. ظل مفيدًا حتى للإنزيمات ذات تشابه التسلسل المنخفض جدًا مع بيانات التدريب وللتفاعلات التي اختلفت إلى حد كبير عن تلك التي تعلّم منها. كما حسّن PMAK التوقعات في تطبيقات واقعية، مثل تقدير كيفية تخصيص الخلايا لمواردها البروتينية المحدودة وتوقُّع آثار الطفرات في مجموعات بيانات هندسة الإنزيم.
ماذا يعني هذا لعلم الأحياء والتقنية الحيوية
بالنسبة لغير الاختصاصيين، يمكن اعتبار PMAK مساعدًا ذكيًا يتعلّم من مكتبات ضخمة من البروتينات والتفاعلات ليخمن مدى سرعة أي إنزيم في تفاعل معين — ولشرح أي الأحماض الأمينية تُسيّر هذا السلوك. من خلال الجمع بين دقة أعلى والبصيرة على مستوى البقايا، يمكن أن يساعد هذا النهج الباحثين على تصميم إنزيمات أفضل، وبناء نماذج أيضية أكثر موثوقية، واستكشاف كيف تؤثر الطفرات على الوظيفة دون إجراء كل تجربة في المختبر. ومع توسّع نماذج مماثلة لتغطي خصائص حركية أخرى، فقد تصبح أدوات أساسية لتصميم عمليات صناعية أنظف، وتحسين الميكروبات للإنتاج المستدام، وتعميق فهمنا لكيفية تحقيق آلات الحياة الجزيئية لهذه السرعة الملحوظة.
الاستشهاد: Cai, Y., Ge, F., Zhang, C. et al. Enhancing kcat prediction through residue-aware attention mechanism and pre-trained representations. Commun Biol 9, 273 (2026). https://doi.org/10.1038/s42003-026-09551-9
الكلمات المفتاحية: حركية الإنزيم, التعلّم العميق, توقّع kcat, هندسة البروتين, نمذجة الأيض