Clear Sky Science · ar
الجلّيكوفاجي هو مسار قديم في ثنائيات الجذع يدعم التكيُّف الأيضي عبر تطور بنية STBD1
كيف يكشف المحار حيل الطاقة الخفية
تنجو الحيوانات في فترات الضيق من خلال الاستفادة من الوقود المخزون، لكن ليس جميعها تعتمد على النوع نفسه من “البطارية”. تدرس هذه الدراسة محار الباسيفيك وتظهر أنه، على خلاف العديد من الحيوانات الأخرى التي تعتمد على الدهون، يعتمد المحار بشدة على السكر المخزون على شكل غليكوجين. تكشف الدراسة عن مسار خلوي لإعادة التدوير قليل المعرفة — يُسمى الجلّيكوفاجي — يساعد المحار على تفريغ وإعادة ملء مخزون السكر بسرعة، وتتبّع كيف تطوّر هذا النظام عبر مملكة الحيوان.
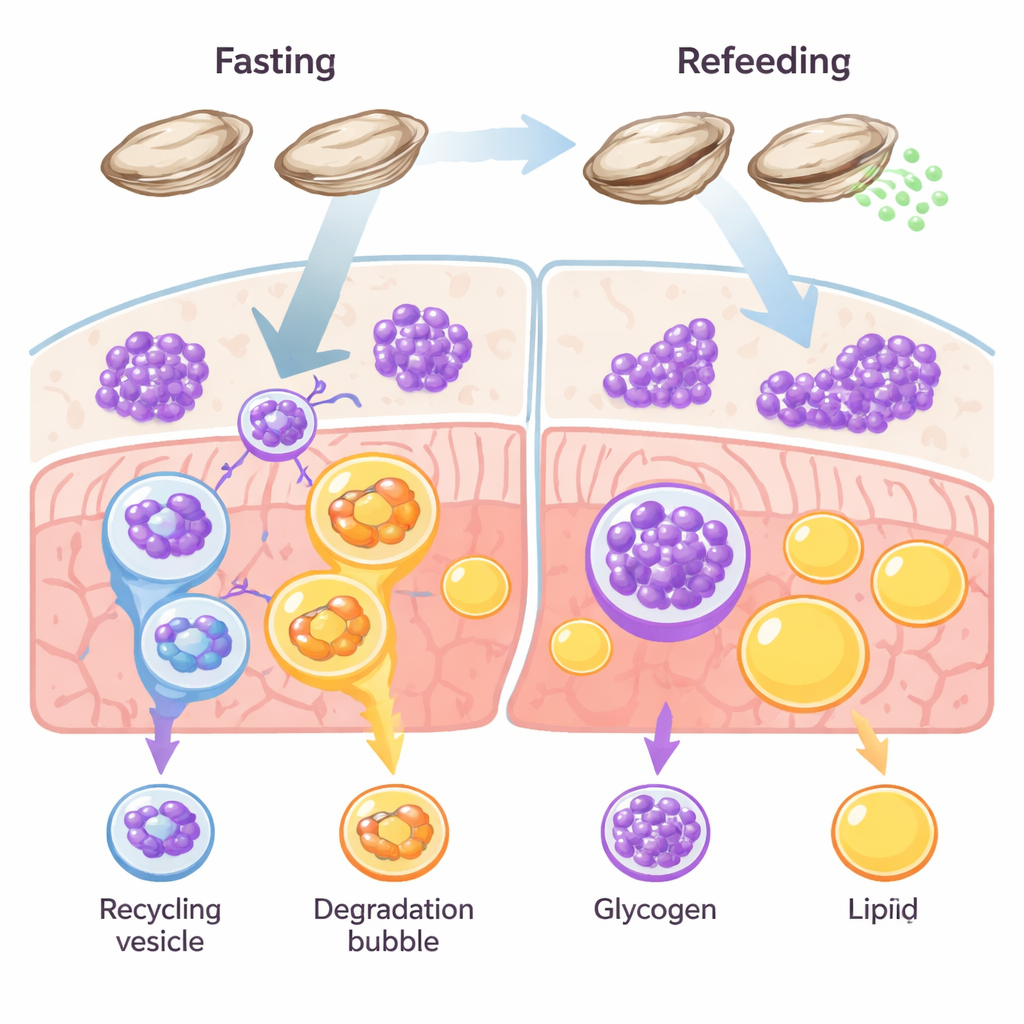
استراتيجية البقاء المعتمدة على السكر أولاً
تدير معظم الحيوانات عدة مخازن للطاقة، أساساً الدهون والغليكوجين. في الفقاريات مثل الأسماك والثدييات، تهيمن الدهون عادة كمخزون طويل الأجل. ينكسر هذا القاعدة لدى المحار؛ أنسجته مليئة بالغليكوجين، وبحوث سابقة أشارت إلى أن هذه الرخويات تحرق السكر بدلاً من الدهون عندما يندر الطعام أو عند إنتاجها للبويضات والحيوانات المنوية. سعى الباحثون إلى اختبار ما إذا كان الجلّيكوفاجي — تكسير مستهدف للغليكوجين داخل الخلايا — يعمل كمسار بقاء أساسي لدى المحار أثناء الجوع والتعافي.
مراقبة تحول الخلايا من التخزين إلى الإنفاق
جاع الفريق محار الباسيفيك لمدة أسبوعين ثم أعادوا تغذيته، متتبعين استجابة أنسجته عبر الزمن. أثناء الصيام، أظهرت الصبغات المجهرية ارتفاعاً في علامات الالتهام الذاتي — إشارات «تنظيف» خلوي — في المكان نفسه حيث كان الغليكوجين مخزوناً، بينما انخفض الغليكوجين نفسه. أما مخازن الدهون فلم تتغير تقريباً. عندما أعيد إطعام المحار، عاد الغليكوجين بسرعة وهبطت إشارات الالتهام الذاتي. وفي الوقت نفسه، ارتفعت وانخفضت مستويات بروتين مستقبل رئيسي يُدعى STBD1، الذي يربط الغليكوجين خصيصاً بآلية الالتهام الذاتي، تزامناً مع استخدام الغليكوجين. بقى مستقبل آخر مربوط بإعادة تدوير الدهون، p62، مستقراً إلى حد كبير. تشير هذه الأنماط مجتمعة إلى وجود مسار مكرّس يركز على السكر: الجلّيكوفاجي، لا التكسير الدهني (الليبوفاجي)، هو الذي يقوم بالعمل الشاق في توازن طاقة المحار.
الخطاف الجزيئي الذي يمسك بالغليكوجين
يعتمد الجلّيكوفاجي على عمل STBD1 كخطاف جزيئي: يلتصق بالغليكوجين ويسلمه إلى بروتينات مُكيِّفة صغيرة تُكوّن حويصلات إعادة التدوير. في المحار، تبين أن STBD1 مرتب بشكل مختلف عن نظيره في الفقاريات. يحمل بروتين المحار منطقة التقاط الغليكوجين المعروفة باسم مجال CBM20 عند الطرف الأمامي (نهاية N)، بينما يضع STBD1 في الفقاريات نفس الوحدة عند الطرف الخلفي (نهاية C) ويشمل ذيلاً دهنيّاً إضافياً يرسخه في أغشية الخلية. أشارت نماذج الحاسوب والمحاكاة إلى أن ترتيب المحار بنهاية N يمنح CBM20 قبضة أقوى وأكثر مرونة على سلاسل السكر المتفرعة. دعمت التجارب المخبرية هذا الاستنتاج: ارتبطت نسخة STBD1 المنقاة من المحار بالغليكوجين بقوة أكبر من نظيراتها في السمك أو الفأر، وعندما عُبِّرت جميع النسخ في خلايا بشرية، أدت نسخة المحار إلى انخفاض أشد في الغليكوجين أثناء الالتهام الذاتي المحفَّز.
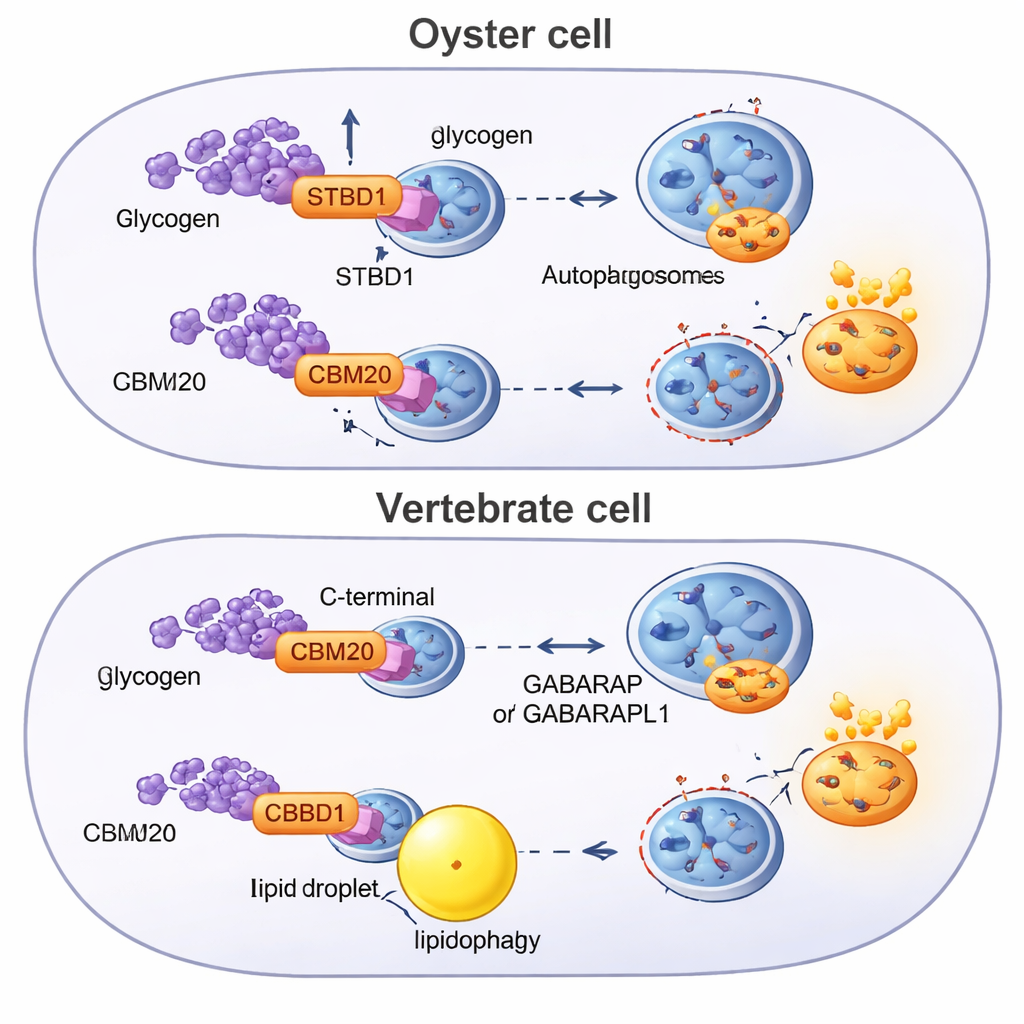
إعادة توصيل مسار قديم عبر الحيوانات
لفهم مصدر هذا النظام، مسح الباحثون جينومات عشرات الحيوانات بحثاً عن البروتينات الحاملة لمجال CBM20 وبنوا أشجاراً تطورية. وجدوا أن STBD1 هو اختراع ثنائيات الجذع — ظهر في السلف المشترك للحيوانات ذات المخططات الجسمانية ثنائية الجانب — لكن بنيته أعيد ترتيبها في فروع مختلفة. يميل المحار وغيره من اللوفتروتوزوان إلى الاحتفاظ بتصميم CBM20 الأثري عند نهاية N، وفي بعض الأحيان حتى تكرار وحدة التقاط السكر. تظهر الحبليات، المجموعة التي تضم الفقاريات، نسخة مميزة تحوّل فيها CBM20 إلى ذيل البروتين. يرتبط هذا التغيير بضعف ارتباط الغليكوجين وباستراتيجية أيضية تميل أكثر إلى تكسير الدهون عبر الليبوفاجي، مدعومة بمستقبلات الالتهام الذاتي وبروتينات مُكيِّفة أخرى يفتقر إليها المحار.
ماذا يعني هذا لخيارات الطاقة في الحياة
لغير المختصين، الخلاصة هي أن الحيوانات طوّرت أكثر من طريقة لعبور فترات نقص الطاقة. يبرز المحار استراتيجية قديمة متمحورة حول السكر: نسخة عالية الألفة من STBD1 تمسك بالغليكوجين بسرعة وتغذيه إلى وحدات إعادة التدوير الخلوية، ما يجعل الجلّيكوفاجي مصدر قوة رئيسي أثناء الإجهاد. على النقيض، يبدو أن الفقاريات قد ضحت جزئياً بتلك القبضة القوية على السكر من أجل نهج أكثر توازناً أو مائل إلى الدهون، مدعوم بشركاء بروتينيين وتراكيب مجالية مختلفة. من خلال ربط بنية البروتين التفصيلية بخيارات وقود الكائن الحي ككل، توضح هذه الدراسة كيف يمكن لـ«إعادة توصيل» جزيئية صغيرة أن تساعد فروعاً مختلفة في شجرة الحيوان على التكيّف مع بيئاتها وأنماط حياتها الخاصة.
الاستشهاد: Ren, L., Bai, Y., Shi, C. et al. Glycophagy is an ancient bilaterian pathway supporting metabolic adaptation through STBD1 structural evolution. Commun Biol 9, 268 (2026). https://doi.org/10.1038/s42003-026-09546-6
الكلمات المفتاحية: الجلّيكوفاجي, تمثيل الغليكوجين, بيولوجيا المحار, الالتهام الذاتي, تطور الأيض