Clear Sky Science · ar
يعطّل الفلوفاستاتين بداية وتقدّم سرطان الثدي عبر استهداف CYP4Z1
لماذا يهم دواء خافض للكوليسترول في سرطان الثدي
تطوّر العديد من النساء المعالَجات من سرطان الثدي اضطرابات في دهون الدم ويواجهن تهديداً مستمراً بعودة المرض أو انتشاره. تستكشف هذه الدراسة فكرة مثيرة: هل يمكن إعادة توظيف حبة شائعة لخفض الكوليسترول، الفلوفاستاتين، لإبطاء أو منع سرطان الثدي عن طريق تعطيل بروتين يغذي الخلايا الورمية الشبيهة بالخلايا الجذعية، والتي تعدّ أكثر خطورة؟
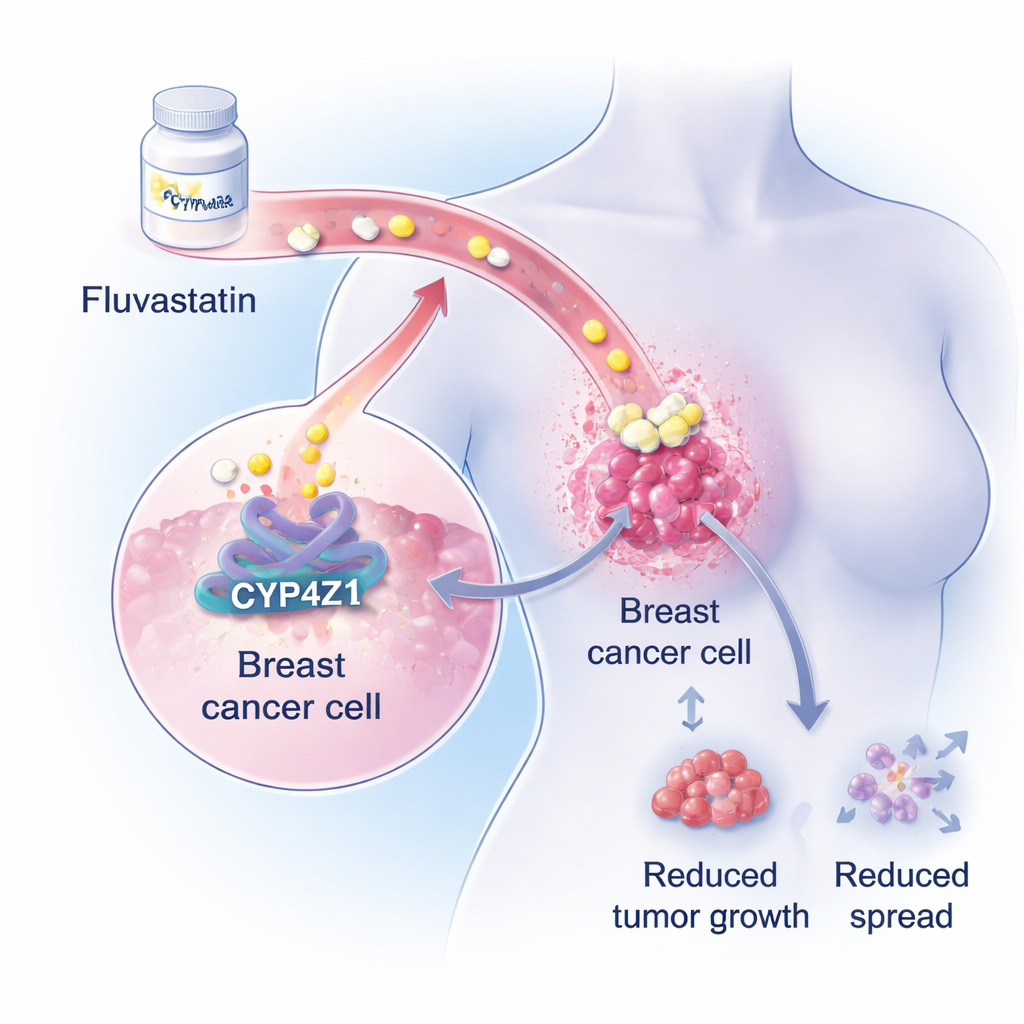
محفّز مخفي داخل أورام الثدي
يركّز الباحثون على بروتين غير معروف كثيراً يُدعى CYP4Z1، يوجد بمستويات عالية في خلايا سرطان الثدي لكنه غير موجود بوضوح في نسيج الثدي السليم. أظهرت أعمال سابقة أن CYP4Z1 يساعد الخلايا السرطانية على التصرف بشكل أقرب إلى الخلايا الجذعية—خلايا قادرة على التجدد المستمر، ومقاومة العلاج الكيميائي، وإعادة بدء الأورام بعد المعالجة. في تحليلات جينية وكيميائية حيوية واسعة، تُظهر الفريق الآن أن اضطراب نشاط CYP4Z1 يعزّز بشكل قوي مسارات بناء الدهون داخل خلايا سرطان الثدي، خصوصاً إنتاج ثلاثي الغليسريد، وهو دهون تخزينية رئيسية. وبما أن العديد من مرضى سرطان الثدي يتطوّر لديهم بالفعل اضطراب في دهون الدم أثناء العلاج الكيميائي، اقتُرح دور CYP4Z1 المحفّز للدهون كنقطة انطلاق لاستخدام أدوية خافضة للدهون موجودة.
إعادة توظيف الفلوفاستاتين من صحة القلب إلى علاج السرطان
لاختبار هذه الفكرة، فحص العلماء مكتبة صغيرة مكونة من 23 دواءً معتمداً من إدارة الغذاء والدواء يُستخدم لخفض دهون الدم. برز الفلوفاستاتين، وهو أقراص ستاتين موصوفة على نطاق واسع لارتفاع الكوليسترول، كخيار مميز: فقد أعاق مباشرة نشاط إنزيم CYP4Z1 بطريقة تعتمد على الجرعة. عند جرعات كانت أقل بكثير ضراً للخلايا الثديية السليمة مقارنة بالخلايا السرطانية، خفّض الفلوفاستاتين بشكل حاد علامات الجذعية الأساسية، وقدرة خلايا سرطان الثدي على تكوين "كرات ورمية" طافية، وقدرتها على الهجرة والغزو عبر حواجز شبيهة بالنسيج في الاختبارات المخبرية. كما جعل خلايا الورم أكثر حساسية لدواء العلاج الكيميائي الأدريامايسين، مما يوحي بأنه قد يعزّز العلاجات الحالية.
اختبار الدواء في حيوانات حية
قيّم الفريق بعد ذلك الفلوفاستاتين في نماذج فئران. في فئران زُرعت فيها خلايا سرطان ثدي بشرية، أبطأ العلاج الدوري بالفلوفاستاتين نمو الورم، وخفّض مستويات علامة الجذعية (ALDH1A1) وعلامة انقسام الخلايا Ki67 في الأورام، وقلّل عدد العقيدات النقيلية التي ظهرت في الرئتين. والأهم من ذلك، حافظت الفئران التي تلقت الفلوفاستاتين على وزنها ولم تُظهر شذوذات دموية أو في نخاع العظم كبيرة، مما يدعم ملف سلامة ملائم عند الجرعة المختبرة. في نموذج وراثي أكثر واقعية—فئران مُهندَسة لتطوير أورام ثدي مدفوعة بجين مسبب للسرطان—أدخل الباحثون أيضاً CYP4Z1 البشري إلى نسيج الثدي. طورت هذه الفئران آفات قبل سرطانية وسرطانية أكثر، ومزيداً من النقائل إلى الكبد والرئتين، مقارنة بالحيوانات الضابطة. خفّض علاج الفلوفاستاتين بشكل كبير عدد آفات الثدي والنقائل البعيدة، خصوصاً في الفئران الحاملة للجين الإضافي CYP4Z1.
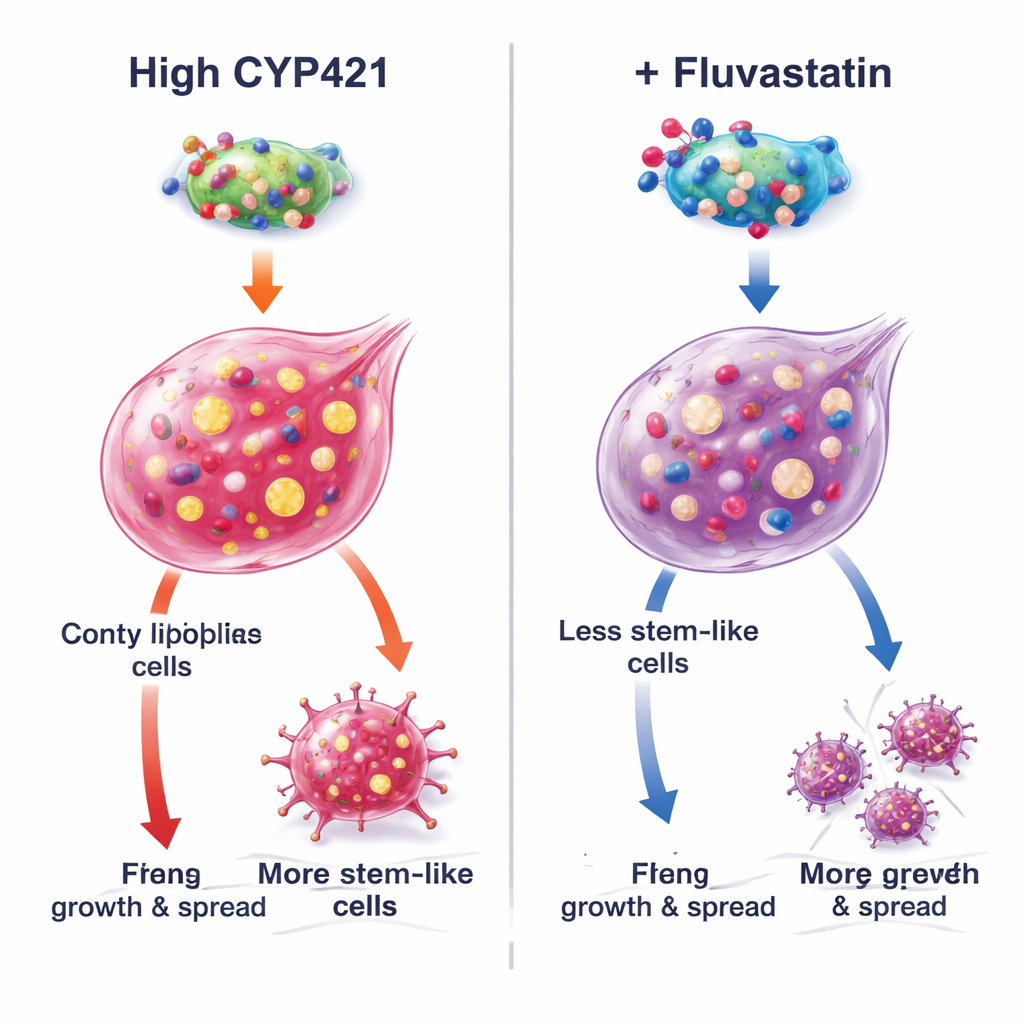
كيف يعطّل الفلوفاستاتين بروتيناً محفّزاً للسرطان
لفهم الآلية، جمع المؤلفون النمذجة الحاسوبية مع هندسة بروتينية دقيقة. تنبأوا بأن الفلوفاستاتين يندفع إلى الموقع النشط في CYP4Z1 عند ثلاثة أحماض أمينية حاسمة (Lys109 وPro444 وArg450). عندما طُفّرت تلك المواقع، انخفض نشاط CYP4Z1 ولم يعد الفلوفاستاتين قادراً على تثبيطه أكثر، مؤكداً أن هذه المواضع تعمل كنقاط ارتكاز. في خلايا تفتقر طبيعياً إلى CYP4Z1، أدى إضافة البروتين الطبيعي إلى زيادة الجذعية وتنشيط إشارة النمو PI3K/AKT، بينما قلّب الفلوفاستاتين هذه التأثيرات. كانت النسخ المطفّرة من CYP4Z1 أقل فعالية وأقل استجابة للدواء. أظهرت تجارب إضافية أن تأثير الفلوفاستاتين ضعُف عندما زاد إنتاج ثلاثي الغليسريد اصطناعياً، أو عندما نُقصَّ CYP4Z1، مما يؤكد أن أقوى تأثيرات الدواء تنشأ من حجب هذا البروتين المحدد وعواقب بناء الدهون المرتبطة به بدلاً من تحريض موت الخلايا عبر "الفِرُوبرُّوس" المعتمد على الحديد.
ماذا يعني هذا للمرضى
بشكل عام، تشير الدراسة إلى أن الفلوفاستاتين، إلى جانب خفضه للكوليسترول، يمكن أن يحدّ من المراحل المبكرة والانتشار اللاحق لسرطان الثدي في نماذج تجريبية عبر استهداف CYP4Z1، وهو بروتين يدفع استقلاب الدهون وسلوكاً شبيهاً بالخلايا الجذعية في الأورام. ونظراً لأن الفلوفاستاتين معتمد بالفعل وسلامته موصوفة جيداً، فإن هذه النتائج تفتح طريقاً واعداً نحو اختبار سريري أسرع كعلاج إضافي، لا سيما لدى المرضى الذين تعبر أورامهم بقوة عن CYP4Z1. ومع حاجتنا إلى مزيد من العمل لاختبار هذا المنهج في البشر ولتحديد أي أهداف إضافية للدواء، تفتح الأبحاث الباب لاستخدام دواء مألوف للقلب كجزء من استراتيجية جديدة ضد سرطانات الثدي العدوانية والمعرضة للانتكاس.
الاستشهاد: Li, H., Chen, Y., Shi, W. et al. Fluvastatin suppresses breast cancer initiation and progression via targeting CYP4Z1. Commun Biol 9, 254 (2026). https://doi.org/10.1038/s42003-026-09532-y
الكلمات المفتاحية: سرطان الثدي, فلوفاستاتين, الخلايا الجذعية السرطانية, استقلاب الدهون, إعادة استخدام الأدوية