Clear Sky Science · ar
النيبوموليد يخفف متلازمة الضائقة التنفسية الحادة والتهاب القولون التقرحي عن طريق تعطيل تنشيط مركب إنفلاماسوم NLRP3
لماذا يهم تهدئة الالتهاب الجامح
العديد من الأمراض الخطيرة، من فشل الرئتين المهدد للحياة إلى أمراض الأمعاء المؤلمة، لا تُسبِّبها الميكروبات أو الإصابات فقط، بل يساهم فيها جهاز المناعة الذي يدخل في حالة فرط استجابة. تستقصي هذه الدراسة ما إذا كان مركب طبيعي يُدعى النيبوموليد، والمستخلص من شجرة النييم، يمكن أن يعمل كـ"مكبح" دقيق لآلة التهابية قوية داخل خلايا المناعة لدينا، مما يفتح طريقًا أكثر أمانًا لعلاج حالات مثل متلازمة الضائقة التنفسية الحادة (ARDS) والتهاب القولون التقرحي.
منبه مزعج داخل خلايا المناعة
في جوهر القصة يوجد نظام إنذار جزيئي يُسمى مركب إنفلاماسوم NLRP3. عندما تَشعر خلايا المناعة بالخطر—إشارات من عدوى، أنسجة تالفة، أو بلورات—يمكن أن يتجمع المركب مثل هيكل ليغو مؤلف من ثلاثة أجزاء: المستشعر NLRP3، المُوَصِل ASC، والإنزيم كاسبيز‑1. بعد تجميعه، ينشط هذا المركب رسائل قوية مثل IL‑1β وIL‑18 ويمكن أن يُحدث شكلًا ناريًا من موت الخلية يُسمى البيروبتوزيس. بينما تساعد هذه الاستجابة في إزالة التهديدات، فإن فرط تنشيطها يساهم في أمراض مزمنة وحادة، بما في ذلك التهاب المفاصل، ومضاعفات السكري، ومرض ألزهايمر، وARDS، وداء الأمعاء الالتهابي. حاولت شركات الأدوية تهدئة NLRP3 بمركبات صناعية، لكن العديد من المرشحين تعثروا بسبب السمية، أو الآثار الجانبية، أو السلوك غير الملائم داخل الجسم، مما يبرز الحاجة إلى مثبطات أكثر أمانًا وانتقائية.
اكتشاف مثبط نباتي قوي
فحص الباحثون 126 مركبًا طبيعيًا لمعرفة أيها يعيق أفضل إفراز IL‑1β من خلايا مناعية ماوسية. برز النيبوموليد، حيث خفّض إفراز IL‑1β بأكثر من 80% عند الجرعات الاختبارية. أظهرت تجارب إضافية أن النيبوموليد قلّل بقوة من تنشيط كاسبيز‑1، وإطلاق IL‑1β، وموت الخلايا بالبيروبتوزيس في البلّعميات المستمدة من نخاع العظم للفئران، بفعالية مماثلة لدواء معياري يُدعى MCC950. والأهم أن النيبوموليد لم يثبط إفراز مراسلين مناعيين آخرين مثل IL‑6، مما يشير إلى أنه يعمل بشكل مركز بدلاً من إيقاف الجهاز المناعي بأكمله. عند اختباره عبر محفزات مختلفة تُفعّل NLRP3—مثل ATP، النيجرسين، بلورات الألوم، والايماكيميود—قلّل النيبوموليد نشاط الإنفلاماسوم باستمرار، بما في ذلك في خلايا بشرية من نوع THP‑1. وبالمقابل، لم يمنع اثنين من الإنفلاماسومات ذات الصلة، AIM2 وNLRC4، مما يبرز خصوصيته تجاه NLRP3.
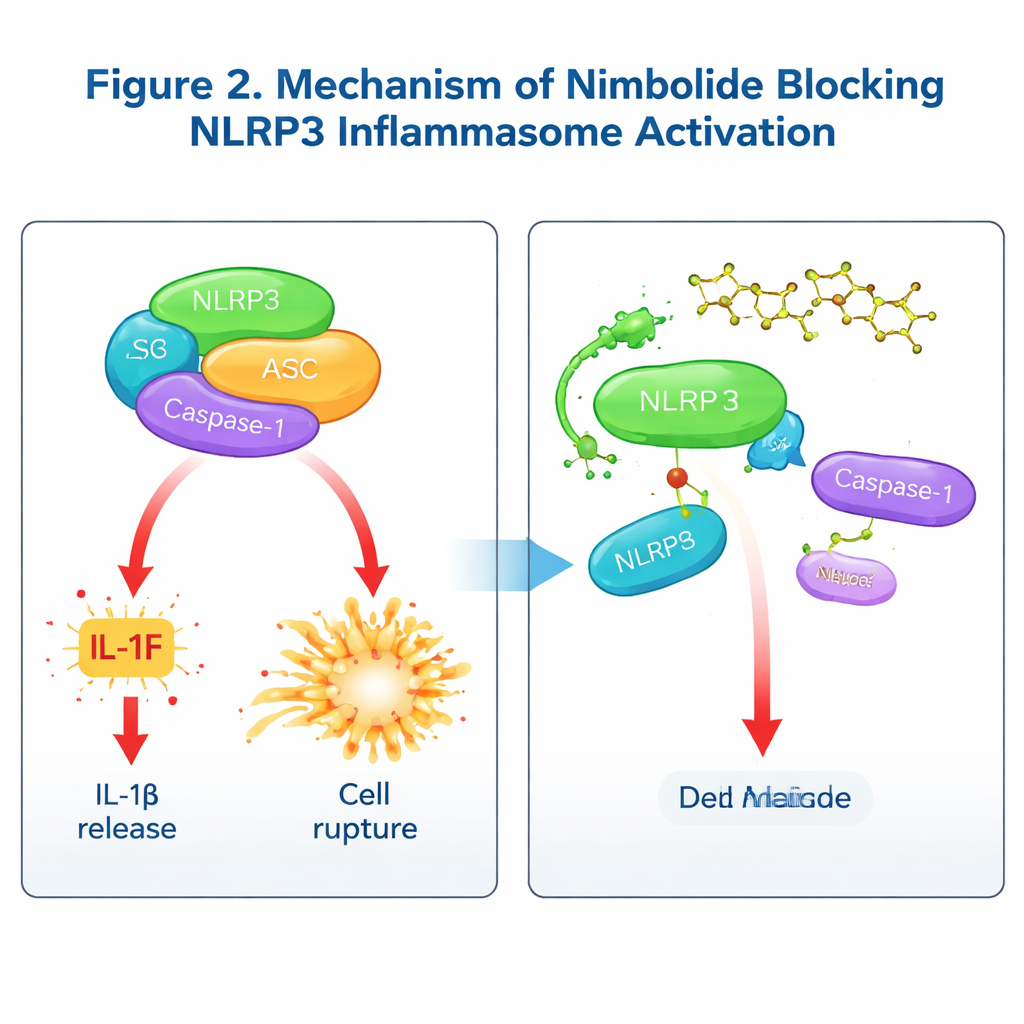
كيف يوقف النيبوموليد الآلة الالتهابية
لفهم آلية عمل النيبوموليد، سأل الفريق ما إذا كان يتداخل مع خطوات "التهيئة" المبكرة التي تتحكم فيها مسار NF‑κB، أو مع المراحل اللاحقة عند تجميع الإنفلاماسوم فعليًا. العلاج قصير الأمد بعد التهيئة ترك إشارات التهيئة وتعبير الجينات الرئيسية دون تغيير لكنه ما زال يقلل IL‑1β وتنشيط كاسبيز‑1، مما يدل على أن النيبوموليد يعمل بشكل أساسي على مرحلة التجميع. كشفت الاختبارات الكيميائية الحيوية التفصيلية أن النيبوموليد لا يغيّر تدفّق البوتاسيوم أو الكالسيوم، أو تلف الميتوكوندريا، أو تفاعل NLRP3 مع بروتينه المساعد NEK7. بدلاً من ذلك، يعطل المصافحة الحاسمة بين NLRP3 وASC، ويقلل تجمع ASC إلى بقع، ويمنع NLRP3 من تشكيل أوлигومرات ذات ترتيب أعلى. باستخدام تجارب الارتباط والنمذجة الجزيئية، أظهر المؤلفون أن النيبوموليد يرتبط مباشرة بمنطقة NACHT من NLRP3 عند حمض أميني محدد، ليسين 565. عندما طُورت طفرة في هذا الموقع، لم يعد النيبوموليد قادرًا على حماية NLRP3 من التحلل أو قطع صلته بـASC، مؤكدًا أن ليسين565 هو نقطة الارتباط الأساسية. ومن الجدير بالذكر أنه بينما تستهدف أدوية أخرى غالبًا نشاط ATPase في NLRP3، يمنع النيبوموليد التجميع دون التأثير على استخدام ATP، ما يقدم آلية عمل متميزة.
اختبار النيبوموليد في أمراض الرئة والأمعاء
تساءل الفريق بعد ذلك عما إذا كان هذا التأثير الجزيئي يترجم إلى حماية حقيقية في نماذج مرضية. في الفئران المعطاة سمًا بكتيريًا لتحريض ARDS، قلّل علاج النيبوموليد قبل التعرض من تلف نسيج الرئة وتراكم السوائل وتسرب البروتين إلى المساحات الهوائية. كانت هناك خلايا مناعية غازية أقل في الرئتين ومستويات أقل من IL‑1β في كل من نسيج الرئة والدم. لوحظت فوائد مشابهة في نموذج حيث تم توصيل السم مباشرة إلى الممرات الهوائية. في نموذج منفصل لالتهاب القولون التقرحي، حيث شربت الفئران مادة كيميائية تُتلف القولون، قيد النيبوموليد فقدان الوزن، وحسّن قوام البراز ودرجات النزف، وحافظ على طول القولون، وقلّل العلامات المجهرية للالتهاب وتآكل النسيج، إلى جانب خفض IL‑1β في القولون. والأهم من ذلك، في فئران مهندسة وراثيًا تفتقر إلى NLRP3، كان المرض أخف بالفعل ولم يوفر النيبوموليد فائدة إضافية، مما يؤكد أن تأثيراته الوقائية تعتمد على حجب NLRP3.
ماذا قد يعني هذا للعلاجات المستقبلية
لغير المتخصصين، الدرس الأساسي هو أن النيبوموليد يعمل كمكبح ذكي لأحد أقوى مفاتيح الالتهاب في الجسم. عن طريق التعلق بموقع دقيق على NLRP3 ومنع الإنفلاماسوم من التجمع، يهدئ الالتهاب المفرط في كل من الرئتين والأمعاء دون إيقاف الدفاعات المناعية على نطاق واسع. بينما سيحتاج النيبوموليد نفسه إلى تحسينات في جوانب مثل الثبات وطرق الإعطاء قبل أن يصبح دواءً، تضع هذه الدراسة النيبوموليد كنقطة انطلاق واعدة—ونموذج—لتصميم أدوية الجيل القادم ضد الأمراض المدفوعة بـNLRP3 مثل ARDS والتهاب القولون التقرحي.
الاستشهاد: Xu, H., Lin, Y., Luo, W. et al. Nimbolide ameliorates ARDS and ulcerative colitis by disrupting NLRP3 inflammasome activation. Commun Biol 9, 246 (2026). https://doi.org/10.1038/s42003-026-09524-y
الكلمات المفتاحية: نيبوموليد, مركب إنفلاماسوم NLRP3, الالتهاب, متلازمة الضائقة التنفسية الحادة, التهاب القولون التقرحي