Clear Sky Science · ar
تعزيز MAT2A لنسخ PARN عبر SRF لتسريع التحلل السكري ودفع التقدم الخبيث في الساركوما العظمية
لماذا تهم هذه الدراسة عن سرطان العظام
الساركوما العظمية هي أكثر أنواع سرطانات العظام شيوعاً لدى الأطفال والمراهقين، والعلاجات بالكاد تغيرت على مدى عقود. لا يزال العديد من المرضى الصغار يواجهون نتائج سيئة، لا سيما إذا انتشر السرطان أو أصبح مقاومًا للعلاج الكيميائي. تكشف هذه الدراسة عن بروتين "مفتاح تحكم" مخفي يسمى MAT2A يساعد خلايا الساركوما العظمية على النمو، وإعادة تهيئة استخدامها للطاقة، وتكوين أورام عدوانية—وتوضح أن دواءً يستهدف MAT2A يمكنه إبطاء هذه الأورام أو تصغيرها في نماذج مخبرية.
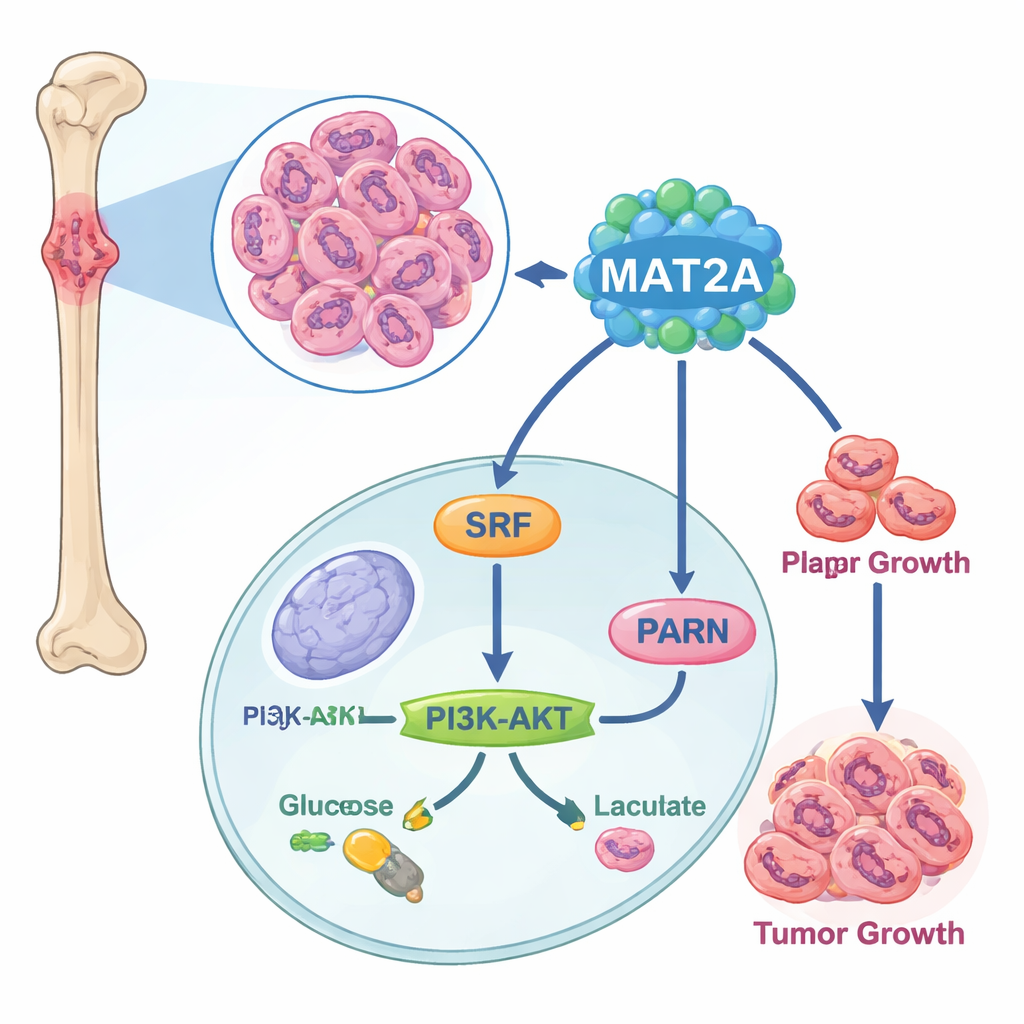
محرك خفي داخل خلايا الورم
بدأ الباحثون بمقارنة عينات سرطان العظام بنسيج العظام الطبيعي على مستوى الخلايا المفردة. وجدوا أن نسيج الساركوما العظمية يحتوي على مزيد من الخلايا البانية للورم وأعدادًا أقل من الخلايا المناعية، وأن جينًا واحدًا على وجه الخصوص—MAT2A—كان نشطًا بشكل غير اعتيادي في الخلايا السرطانية. أكدت تحليلات قواعد بيانات السرطان العامة وخطوط الخلايا المزروعة في المختبر أن مستويات MAT2A كانت أعلى بكثير في الساركوما العظمية مقارنة بخلايا العظام السليمة، وأن المرضى الذين لديهم مستويات أعلى من MAT2A كانوا ميالين إلى مرض أكثر تقدمًا وانتشارًا إلى العقد الليمفاوية. وضع هذا MAT2A في مركز الاهتمام كدافع محتمل للمرض بدلًا من كونه مجرد مرافق سلبي.
خفض MAT2A يبطئ نمو السرطان
لاختبار مدى أهمية MAT2A فعلاً في سلوك الورم، استخدم الفريق أدوات جينية لخفض مستويات MAT2A في خطوط خلايا الساركوما العظمية. عندما تم إسكات MAT2A، انقسمت الخلايا السرطانية بمعدل أبطأ وكانت أكثر عرضة للدخول في الموت المبرمج. في الفئران المزروعة بهذه الخلايا المعدلة، نمت الأورام بشكل أبطأ بكثير وانتهت أصغر حجمًا بشكل ملحوظ، على الرغم من استقرار وزن أجسام الحيوانات. أظهرت هذه التجارب أن خلايا الساركوما العظمية تعتمد بشدة على MAT2A من أجل البقاء والقدرة على تكوين الأورام.
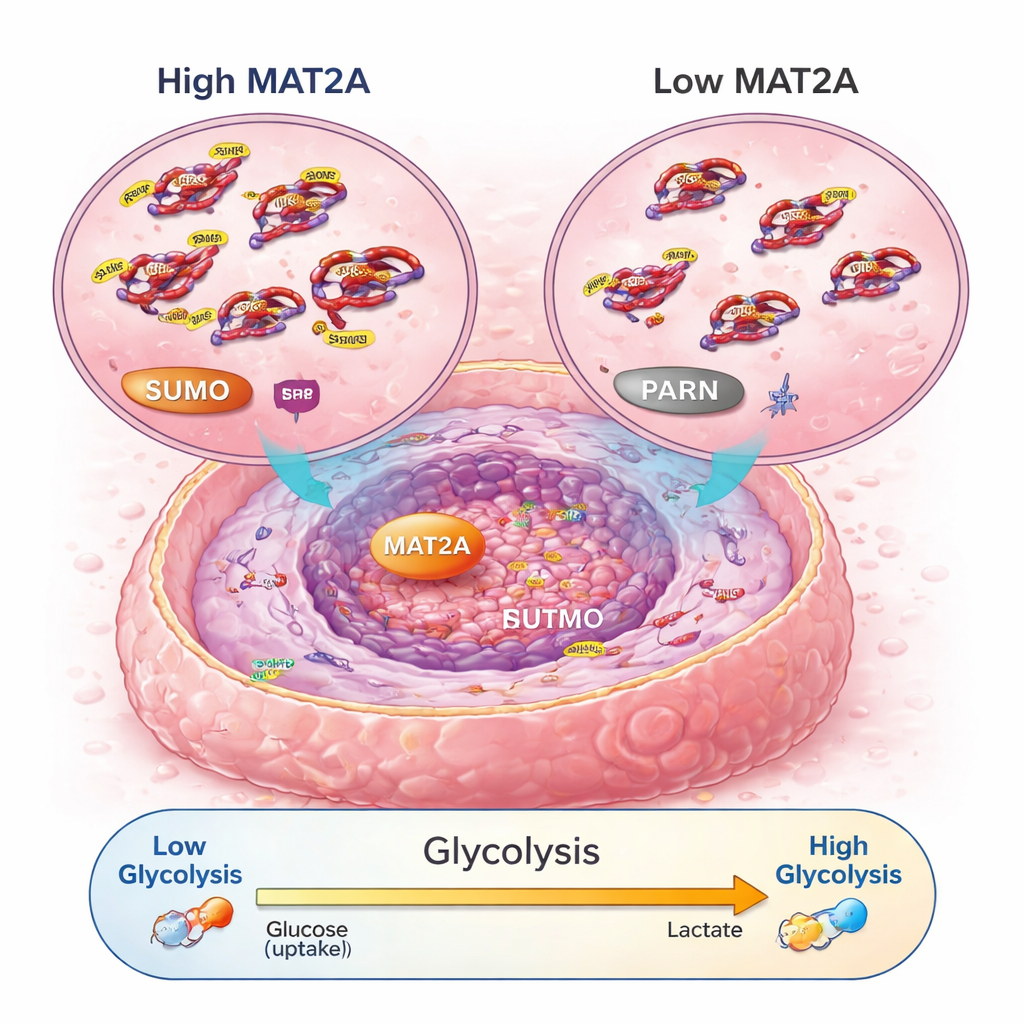
تتابع إشارية يعزز استخدام الخلايا للوقود
بتعمق أكبر، اكتشف العلماء أن MAT2A يفعل أكثر من أداء وظيفته الأيضية المعتادة. داخل النواة، يرتبط بعامل نسخ يُدعى SRF، مما يساعد على إبقاء SRF مستقرًا ونشطًا عبر تعزيز وسم كيميائي يعرف بـSUMO. بالمقابل، يقوم SRF بتشغيل جين يدعى PARN، الذي ينشط بدوره المسار المعروف PI3K–AKT ويعلي من آلية التحلل السكري الهوائي—طريقة سريعة ولكن غير فعّالة للخلايا لصنع الطاقة تفضلها الخلايا السرطانية. عندما انخفضت مستويات MAT2A، أنتجت الخلايا السرطانية كمية أقل من ATP (عملة طاقتها)، وامتصاصًا أقل للجلوكوز، وإنتاجًا أقل لحمض اللاكتيك، وتحولت مرة أخرى نحو التنفس الهادىء القائم على الأكسجين. كان تعطيل PARN أو AKT قادرًا على قلب تأثيرات MAT2A المحفزة للنمو والتحلل السكري، مؤكداً أن هذا التتابع—من MAT2A إلى SRF إلى PARN إلى PI3K–AKT—يعمل كدائرة أساسية للطاقة والنمو في الساركوما العظمية.
دور غير تقليدي وهدف قابل للعقار
من اللافت أن نسخة من MAT2A تفتقر إلى نشاطها الإنزيمي الطبيعي لا تزال تدعم استقرار SRF وتنشيط PARN، ما يعني أن هذا الدور المحفز للسرطان لا يعتمد على تفاعله الكيميائي المعتاد. بدلًا من ذلك، يعمل MAT2A أكثر كهيكل داعم ينظم بروتينات أخرى. لهذا آثار عملية: لا تحتاج الأدوية بالضرورة إلى إعاقة مركزه التحفيزي لإضعاف الأورام. اختبر الباحثون مثبطًا جزيئيًا صغيرًا يسمى FIDAS-5، مصممًا لاستهداف MAT2A، في كل من زُرعات الخلايا ونماذج الفئران. قلّل العلاج من SRF النووي، وخفض إشارات PARN وPI3K–AKT، وكبح التحلل السكري، وأبطأ نمو الخلايا، وأحدث موتًا خلويًا سرطانيًا. في الفئران، قلّص FIDAS-5 الأورام أو أبطأ نموها دون فقدان وزني ملحوظ، مما يشير إلى آثار جانبية محتملة مقبولة في هذا السياق.
ماذا يعني هذا للمرضى والعلاجات المستقبلية
لغير المتخصصين، الرسالة الأساسية هي أن خلايا الساركوما العظمية تعتمد على MAT2A للحفاظ على برامج نموها ومحركات حرق السكر تعمل بأقصى طاقة. من خلال تثبيت بروتينات التحكم الرئيسية وتعزيز سلسلة من الإشارات، يساعد MAT2A الأورام على النمو بشكل أسرع وتصبح أكثر عدوانية. إن حجب هذا البروتين—سواء بأساليب تعتمد على الجينات أو بدواء مثل FIDAS-5—يقطع ذلك الدعم، مما يجبر الخلايا السرطانية على الإبطاء، وحرق الطاقة بشكل أقل هستيرية، وفي نهاية المطاف الموت. بينما لا يزال أمامنا عمل كبير قبل أن تصل مثل هذه العلاجات إلى العيادة، تضع هذه الدراسة MAT2A كهدف واعد جديد في مكافحة سرطان العظام، فاتحة طريقًا محتملاً لعلاجات أكثر دقة وأقل سمية لدى المرضى الصغار.
الاستشهاد: Ren, Z., Chen, H., Qiao, Q. et al. MAT2A enhances PARN transcription via SRF to accelerate glycolysis and drive malignant progression in osteosarcoma. Commun Biol 9, 241 (2026). https://doi.org/10.1038/s42003-026-09518-w
الكلمات المفتاحية: الساركوما العظمية, MAT2A, أيض السرطان, مسار PI3K AKT, العلاج المستهدف