Clear Sky Science · ar
تقدمات استراتيجية لدراسات الهيكل الجزيئي بواسطة الكريو-إلكترون المجهري لبروتينات GPCR الصغيرة (<100 kDa)
لماذا تهم هذه المفاتيح الصغيرة للطب
تعمل أجزاء كبيرة من الطب الحديث عبر دفع خفي لمفاتيح صغيرة تقع في أغشيتنا الخلوية تُعرف بمستقبلات بروتين‑جي المقترنة (GPCR). تستشعر هذه المفاتيح الهرمونات والروائح والأدوية، ويستهدفها نحو ثلث الأدوية المعتمدة. ولتصميم أدوية أكثر أماناً وذكاءً، يحتاج العلماء إلى صور ثلاثية الأبعاد مفصلة لهذه المستقبلات، لا سيما في حالتها «المطفأة» أو غير النشطة، التي تستهدفها الكثير من الأدوية تحديداً. تشرح هذه المقالة كيف يتعلم الباحثون رؤية بعض أصغر مستقبلات GPCR باستخدام المجهر الإلكتروني بالتبريد (كريو‑إم)، وهو أسلوب تصوير قوي يمكنه النظر إلى الجزيئات المجمدة في حالة قريبة من الطبيعية.
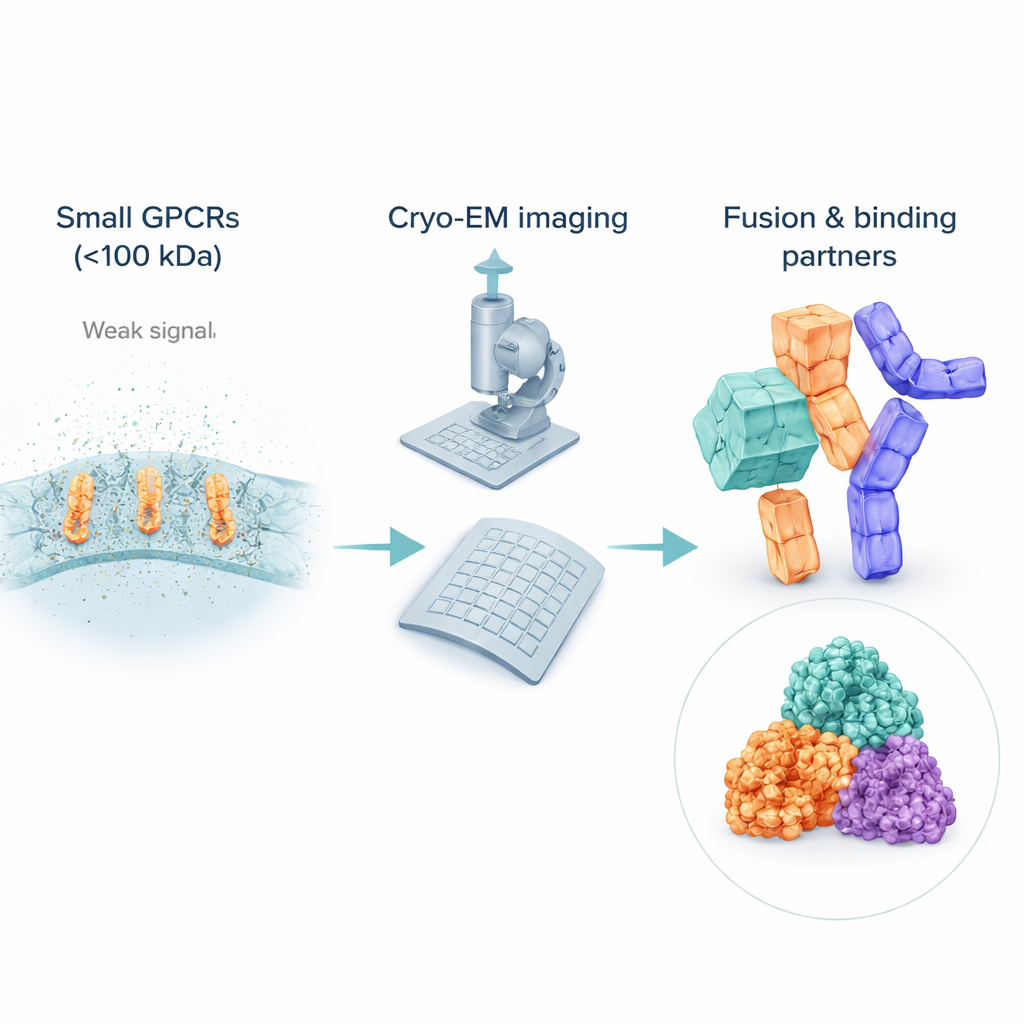
تحدي رؤية المستقبلات الصغيرة جداً
على الرغم من أن الكريو‑إم أحدث ثورة في علم الأحياء الهيكلي، إلا أنه لا يزال يواجه صعوبة مع الجزيئات الصغيرة والمرنة. فالكثير من مستقبلات GPCR غير النشطة تزن أقل بكثير من 100 كيلو دالتون، مما يجعل من الصعب اكتشافها ومحاذاتها في صور ضوضائية. للحفاظ على ذوبانها، يحيط العلماء بهذه المستقبلات وفقاعات منظفة أو محاكيات دهنية، والتي قد تبدو في الواقع «أكبر» لحزمة الإلكترونات من البروتين نفسه، مما يغمر الإشارة القادمة من البنية المراد دراستها. وعلى خلاف المستقبلات النشطة المرتبطة بشركاء ضخمين مثل بروتينات G، غالباً ما تفتقر المستقبلات غير النشطة إلى ميزات خارجية بارزة، لذا تجد الحواسيب صعوبة في متوسط العديد من الصور إلى رؤية ثلاثية الأبعاد حادة. ونتيجة لذلك، لا تزال معظم هياكل GPCR غير النشطة تُستمد من طرق الأشعة السينية الأقدم، تاركة فراغاً في تغطية الكريو‑إم تحديداً حيث تعمل العديد من الأدوية.
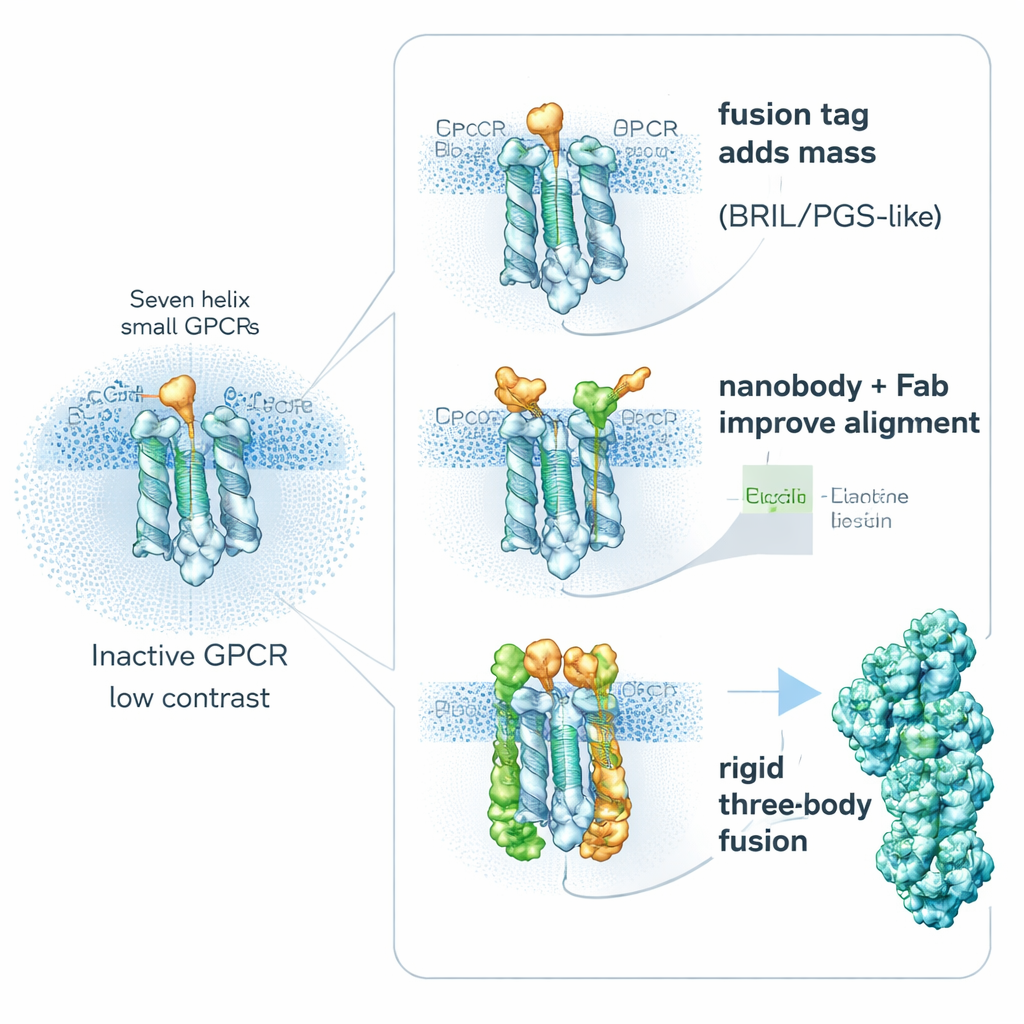
زيادة كتلة المستقبلات بمساعدين مدمجين
أحد الاستراتيجيات الأساسية بسيط إلى حد ما: جعل المستقبل «أثقل» عن قصد. يربط الباحثون جينياً بروتينات مساعدة صغيرة ومستقرة بأجزاء مرنة من مستقبلات GPCR لزيادة حجمها وصلابتها، من دون حجب مناطق ربط الدواء المهمة. من المساعدين الشائعين BRIL (حزمة من أربع حلزونات ألفا)، وPGS (مقطع من إنزيم مستقر حرارياً)، وبروتين أكبر يشبه المشبك اسمه calcineurin. تُدرج هذه الشركاء الاندماجية غالباً في حلقة داخلية متحركة تربط بين حلزونيْن. عبر تقوية هذه المنطقة، تقلل من الضبابية الناتجة عن الحركة الجزيئية وتوفر أشكالاً معروفة تساعد الحواسيب على محاذاة الجسيمات. تُظهر الدراسات أن الموضع والاتجاه الدقيقان لقطعة الاندماج يمكن أن يحددان نجاح المشروع: ففي أحد المستقبلات، حسن وضع علامة PGS مختلفة الدقة من نحو 6 أنغستروم ضبابية إلى 3.7 أنغستروم أوضح بكثير.
استعارة الأجسام المضادة والروابط المصممة كمقابض
مسار ثانٍ يتجنب إدخال اندماجات كبيرة في المستقبل وبدلاً من ذلك يربط «مقابض» عالية التقارب من الخارج. يمكن تربية شظايا الأجسام المضادة الصغيرة المسماة النانوبودي والروابط ذات الصلة للتعرف على مستقبلات GPCR غير النشطة والتشبث بالحلقة الداخلية المرنة. مثال بارز هو Nanobody‑6، الذي صُمم أولاً كمستشعر لأحد مستقبلات الأفيون ثم أعيد استخدامه، مع تعديلات طفيفة، لتثبيت عدة مستقبلات GPCR أخرى في حالاتها غير النشطة. وبما أنه يرتبط بعيداً عن المركز، فإنه يمنح كل جسيم دليل اتجاه واضح، مما يجعل متوسط الصور أكثر موثوقية. كثيراً ما يوسع الباحثون هذه الفكرة بإضافة طبقة ثانية—شظية جسم مضاد عادية تتعرف على النانوبودي نفسه—مشكّلة مركباً أكبر وأكثر صلابة يظهر بوضوح في الكريو‑إم. ويمكن استخدام روابط مهندسة أخرى، مثل DARPins، كفواصل معيارية أو كموصلات لأقفاص بروتينية أكبر، معزِّزةً الإشارة من الأهداف الصغيرة جداً.
تصميم عيّنات أذكى ومعالجة صور مدعومة بالذكاء الاصطناعي
ليس إدخال المساعدين أو إضافة الروابط سوى جزء من القصة. تؤكد المراجعة أن الهياكل الجيدة تبدأ ببُنى مستقبلات مُهندَسة بعناية: تقليم المناطق الذيلية المرنة، إدخال طفرات مثبتة، واستخدام أدوات التنبؤ بالهياكل الحديثة لتحديد الأجزاء التي قد تسبب مشاكل. وعلى جانب التصوير، تُكمل أو حتى تحل أدوات الذكاء الاصطناعي الحديثة حيلاً أقدم مثل صفائح الطور التي تزيد التباين للجسيمات الباهتة. يمكن لبرامج التعلم العميق انتقاء الجسيمات الصغيرة المختبئة في الميكروغرافات المليئة بالضوضاء، والخوارزميات الجديدة يمكنها فرز الصور إلى أشكال مختلفة عندما تتأرجح المستقبلات بين توافقات متعددة. مع المساعدين المرجعيين، تدفع هذه التقدّمات الكريو‑إم نحو حلّ موثوق لبروتينات الغشاء التي كانت تُعتبر ذات يوم صغيرة جداً أو ديناميكية للغاية للدراسة.
ما الذي يعنيه ذلك للأدوية المستقبلية
تخلص المقالة إلى أنه لا يوجد مساعد «سحري» واحد يصلح لكل المستقبلات، لكن صندوق أدوات متنامٍ من شركاء الاندماج، والروابط الشبيهة بالأجسام المضادة، والأساليب المدفوعة بالذكاء الاصطناعي يفتح تدريجياً المشهد غير النشط لمستقبلات GPCR أمام الكريو‑إم. ولغير المتخصصين، الخلاصة الأساسية هي أنه بجعل المستقبلات الصغيرة تبدو أكبر وأكثر انتظاماً للمجهر، يمكن للعلماء أخيراً الحصول على لقطات مفصّلة للأشكال الدقيقة التي تفضّل العديد من الأدوية ربطها. يجب أن تسرّع هذه المخططات الهيكلية تصميم أدوية تطفئ هذه المفتاحات الخلوية بدقة أكبر—أو تضبط نشاطها بدقة—مع آثار جانبية أقل.
الاستشهاد: Singh, S.K., Agrawal, M., Pattanayak, A. et al. Strategic advances for cryo-EM structural studies of small (<100 kDa) GPCRs. Commun Biol 9, 237 (2026). https://doi.org/10.1038/s42003-026-09516-y
الكلمات المفتاحية: مستقبلات بروتين-جي المقترنة, التصوير المجهري الإلكتروني بالتبريد, اكتشاف الأدوية, علم الأحياء الهيكلي, هياكل النانوبودي