Clear Sky Science · ar
الديناميكيات الزمنية لتقطيع الحمض النووي الريبي العرضي بواسطة LbuCas13a في خلايا الإنسان
تحويل دفاع بكتيري إلى قاطعة خلايا دقيقة
اكتشف الباحثون طريقة لتحويل بروتين مناعِي بكتيري إلى مفتاح "تدمير ذاتي" انتقائي للغاية للخلايا البشرية. باستخدام إنزيم CRISPR يسمى LbuCas13a، يمكنهم التعرف على رسالة ريبية محددة داخل الخلية ثم تمزيق معظم الحمض النووي الريبي الآخر في تلك الخلية. بالنسبة للقارئ العام، هذا مثير للاهتمام لأن الرسائل الريبية تتحكم في البروتينات التي تُنتَج داخل الخلية؛ وإتقان محوها عند الطلب يفتح أبواباً لعلاجات جديدة للسرطان، واستراتيجيات مضادة للفيروسات، وأدوات بحثية قوية.
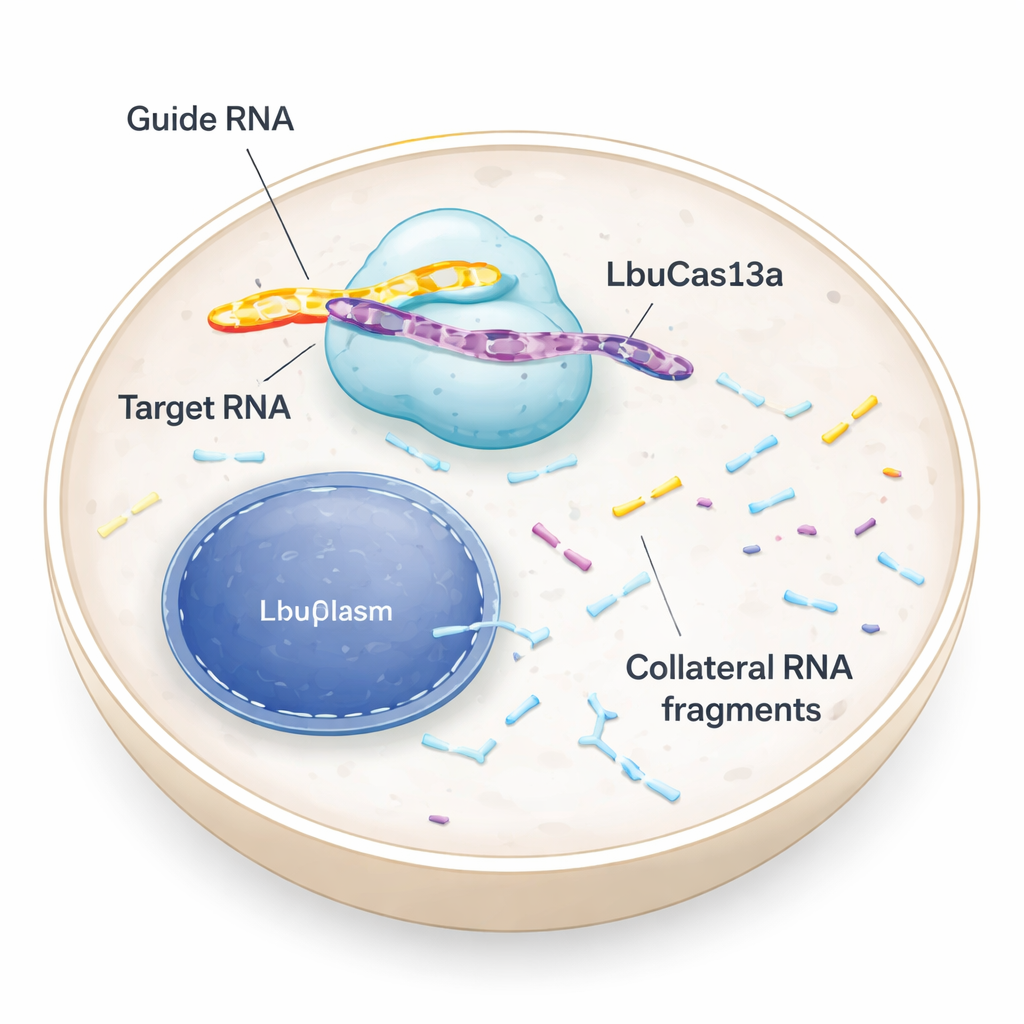
مقص جزيئي يستهدف الحمض النووي الريبي لا الحمض النووي
معظم الناس سمعوا عن أدوات CRISPR التي تقطع الحمض النووي، وتعيد كتابة الشفرة الجينية. LbuCas13a مختلف: فهو يتعرف على الحمض النووي الريبي ويقطعه، وهي الرسائل المؤقتة التي تنقل التعليمات من الحمض النووي إلى مصانع البروتين داخل الخلية. في البكتيريا، تشكل إنزيمات Cas13 جزءاً من الدفاع المضاد للفيروسات. عند رصدها لحمض ريبوي فيروسي، لا تقتصر على تقطيع ذلك الغزو فحسب، بل تبدأ أيضاً في تقطيع العديد من الحمضيات الريبية الأخرى المجاورة. يمكن لهذا النشاط "العَرَضِي" أن يدفع الخلايا المصابة إلى السكون أو الموت، مما يساعد على حماية المجتمع البكتيري. أشارت الاختبارات المبكرة في خلايا حيوانية وبشرية إلى أن التقطيع العرضي بواسطة Cas13 كان ضعيفاً أو مفقوداً، فاستُخدم الإنزيم أساساً كمفتاح "إيقاف" دقيق للحمض النووي الريبي. تعيد الدراسة الجديدة فحص هذا الافتراض وتُظهر أنه، تحت ظروف مناسبة، يمكن أن يكون النشاط العرضي في الخلايا البشرية قوياً ومفيداً.
إطلاق التقطيع العرضي في خلايا الإنسان
قارن الفريق عدة متغيرات من Cas13 ووجدوا أن LbuCas13a كان ذا قوة خاصة. سلَّموا بروتين LbuCas13a المنقَّى المحمَّل مسبقاً بإرشاد ريبوي قصير مباشرة إلى الخلايا البشرية، وهو شكل من أشكال "حقن البروتين" الجزيئي يُسمى توصيل ريبونوكليوبروتين (RNP). عندما طابقت الإرشاد حمضاً ريبياً مستهدفاً — مثل جين علامة فلورية أو رسائل طبيعية وفيرة مثل GAPDH و18S ribosomal RNA — قام الإنزيم أولاً بتقطيع ذلك الهدف ثم بدأ في التهام العديد من الأحماض الريبية الأخرى. خلال نحو 50 دقيقة، تغيَّر الملف العام للحمض الريبي في الخلية بشكل كبير، مع ظهور شظايا تقطيع مميزة. لوحظ هذا التأثير العرضي مع طرق توصيل مختلفة وفي مجموعة من أنواع الخلايا، مما يدل على أنه لم يكن سلوكاً خاصاً بخط خلوي واحد أو هدف صناعي وحيد.
من تمزيق الحمض الريبي إلى موت الخلية والانتقاء
ماذا يحدث لخلية تختفي رسائلها الريبية فجأة؟ باستخدام تصوير الخلايا الحية، رصد الباحثون أن الخلايا التي تُعبِّر عن الحمض الريبي الهدف دخلت تدريجياً في حالة الاستماتة (apoptosis)، وهي شكل منظم من موت الخلايا المبرمج تتميز بإشارات "التحذير المبكر" قبل تفتت الخلية. ومن المهم أن الخلايا المجاورة التي لم تُعبِّر عن الحمض الريبي الهدف ظلت في الغالب غير متأثرة، مما يبرهن أن التدمير الذاتي محدد. ثم استغل الفريق هذه الخاصية كأداة انتقائية. عندما خلطوا خلايا حاملة للهدف مع خلايا طبيعية ونشطوا LbuCas13a، تم استنفاد الخلايا الحاملة للهدف انتقائياً على مدى عدة أيام. وتكرار العلاج عدة مرات خفَّض نسبتها أكثر. أظهروا أن هذا يمكن أن يثري الخلايا التي تم تعديلها بنجاح وراثياً، ويمكن أيضاً ضبطه لمهاجمة الخلايا السرطانية التي تُفرِز مقداراً زائداً من جين مسرطن، هنا CDK4، مع تجنُّب الخلايا المرتبطة التي تصنع كمية أقل بكثير من ذلك الحمض الريبي.
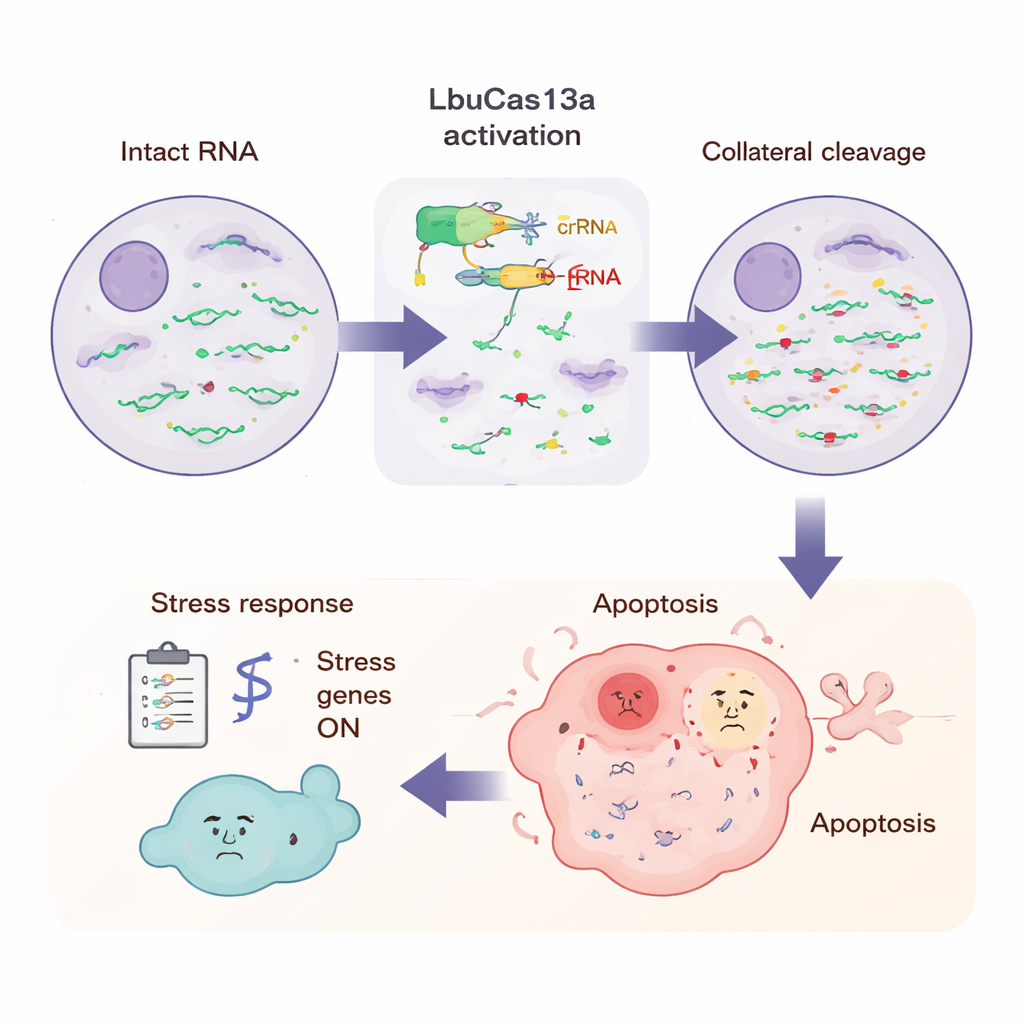
ما الذي تختبره الخلية أثناء الهجوم
لرصد الصورة الأوسع، قاس العلماء جميع الأحماض الريبية في الخلية عند عدة نقاط زمنية بعد تفعيل LbuCas13a. من خلال إضافة معايير ريبية معروفة (spike‑in)، تمكنوا من معرفة أن معظم الأحماض الريبية المرمزة للبروتين في السيتوبلازم انخفضت بأكثر من النصف خلال بضع ساعات، بينما نُفِقت أنواع معينة من الأحماض الريبية — مثل رسائل الميتوكوندريا وبعض الأحماض الريبية غير المشفرة النَوية — إلى حد كبير. كشفت تقنية التسلسل الطويل الأمد أن التقطيع حدث عند مواقع نوكليوتيدية مكررة ومحددة، غالباً في مناطق حلقية مرنة من الحمض الريبي غنية باليوراسيل، بما يتوافق مع الأنماط المرصودة في التجارب المختبرية. في نقاط زمنية لاحقة، شُغِّلت العديد من جينات الإجهاد والمناعة الفطرية، بما في ذلك تلك المرتبطة بالإشارات الالتهابية والدفاعات المضادة للفيروسات. يشير هذا النمط إلى أن الخلية تستشعر سيل النهايات الريبية المكسورة فجأة بطريقة تشبه اكتشافها لعدوى فيروسية، مما يطلق برنامج إنذار ينتهي بالاستماتة.
لماذا هذا مهم وإلى أين قد يقودنا
بعبارات بسيطة، تُظهر الدراسة أن LbuCas13a يمكن تحويله إلى "مفتاح قتل" موجه بالحمض الريبي للخلايا: إذا كانت الخلية تصنع كثيراً من حمض ريبوي معين، فإن تفعيل LbuCas13a ضد ذلك الحمض يسبب فقداناً شبه شامل للحمض الريبي، واستجابة مناعية شبيهة بالإنذار، ثم موتاً خلوياً منظماً. وبما أن العملية تعتمد بقوة على مقدار وفرة الحمض الريبي الهدف، فيمكن استخدامها لإزالة الخلايا التي تُفرِز جينات ضارة بكثرة — مثل بعض الخلايا السرطانية — أو لتنظيف خلايا غير مرغوب فيها في مزروعات مختلطة أثناء البحث أو تصنيع علاجات خلوية. وفي نفس الوقت، العمل تحذيري: أدوات CRISPR الموجهة للحمض الريبي قد تسبب آثاراً جانبية قوية يجب إدارتها بحذر. إن فهم متى وكيف يحدث التقطيع العرضي للحمض الريبي أمر ضروري لاستخدام تقنيات Cas13 بأمان في الطب والتكنولوجيا الحيوية.
الاستشهاد: Bot, J.F., Zhao, Z., Li, M. et al. Temporal dynamics of collateral RNA cleavage by LbuCas13a in human cells. Commun Biol 9, 233 (2026). https://doi.org/10.1038/s42003-026-09511-3
الكلمات المفتاحية: CRISPR-Cas13, تقطيع الحمض النووي الريبي, موت الخلايا, استهداف السرطان, أدوات تعديل الجينات