Clear Sky Science · ar
فك شفرة محور التنظيم المناعي ERS–CAF عبر ذكاء اصطناعي متعدد النماذج وقيمته التنبؤية النِّسيجية والعلاجية عبر أنواع السرطان
التطلع إلى الأورام دون مشرط
يعترف أطباء السرطان بشكل متزايد بأن ما يحيط بالورم قد يكون له نفس أهمية الورم نفسه. لكن أخذ عينات متكررة من هذا الحي المخفي عبر خزعات أمر تدخلي وغالباً غير عملي. تُظهر هذه الدراسة كيف يمكن للذكاء الاصطناعي أن يقرأ الفحوص الروتينية بالأشعة والصور الميكروسكوبية لاستنتاج عمليات مناعية ونسيجية تشبه الندبة، والتي يصعب قياسها، داخل الأورام، محوِّلاً صور التصوير الطبي اليومية إلى نوع من «الخزعة الرقمية» القابلة للتطبيق عبر سرطانات متعددة.
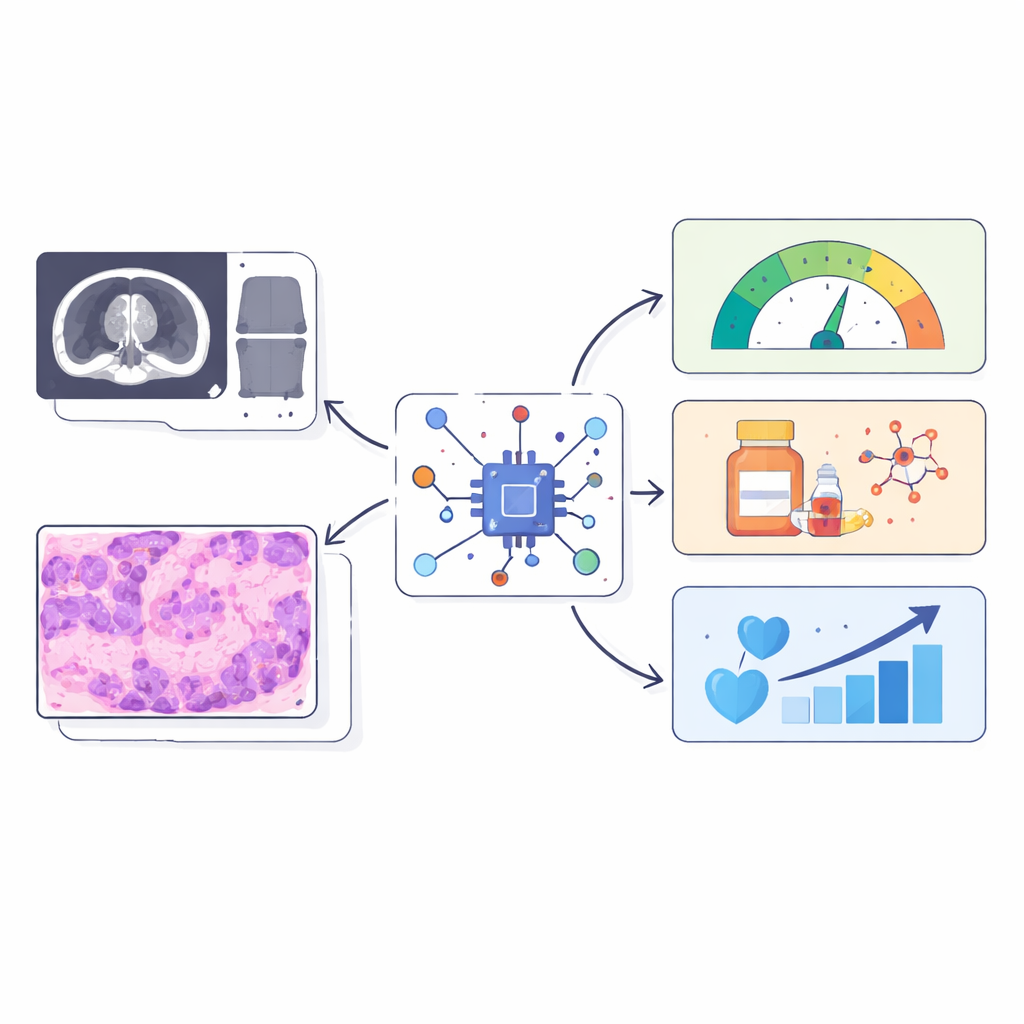
الخلايا الداعمة الخفيّة التي تشكّل السرطان
العديد من الأورام الصلبة ملفوفة بقشرة ليفية صلبة يصنعها خلايا داعمة متخصّصة تُسمى الخلايا الليفية. عندما تكون هذه الخلايا تحت ضغوط داخل مصنع البروتين في الخلية (الشبكة الإندوبلازمية)، تتبنّى حالة عدوانية تُساعد السرطان. في الورم الحبلوي، وهو سرطان عظمي نادر، تبني هذه الخلايا الليفية المتوترة مصفوفة كثيفة وتساهم في إبعاد خلايا الجهاز المناعي، مما يجعل العلاجات أقل فعالية. تظهر بيئات ليفية وفقيرة بالمناعة مشابهة في سرطانات أخرى مثل البنكرياس والقولون والمستقيم، مما يشير إلى أن هذه البيولوجيا ليست مقتصرة على مرض واحد. التحدي هو أن الطرق الحالية لقياس هذه الخلايا الليفية المتوترة وسلوكها المعيق للمناعة تعتمد على عينات الأنسجة والاختبارات الجزيئية المعقدة، والتي يصعب تكرارها وقد تفوت مناطق مهمّة من الورم.
تعليم الذكاء الاصطناعي لرؤية البيولوجيا غير المرئية
تساءل الباحثون عما إذا كانت صور الرنين المغناطيسي القياسية قبل الجراحة وشروحات الهيئة المصبوغة الروتينية H&E تحتوي بالفعل على دلائل بصرية حول حاجز الخلايا الليفية المتوترة والمستبعدة للمناعة. أنشأوا ثلاثة «درجات مرجعية» رقمية من تسلسل الحمض النووي الريبوزي للورم: واحدة تلتقط مدى نشاط برنامج الضغوط في الخلايا الليفية، وأخرى تلخّص مدى قوة إشارات هذه الخلايا إلى خلايا الجهاز المناعي، وثالثة تصف تنوّع مجموعات الخلايا المناعية والداعمة المحيطة. بدلاً من التنبؤ بآلاف الجينات، تدرب الذكاء الاصطناعي على التنبؤ بهذه الدرجات الثلاث ذات المعنى البيولوجي من الصور وحدها. لتحقيق ذلك، جمع الفريق بين فرعين: أحدهما يحلّل نسيج وملامح الشكل من الرنين المغناطيسي، والآخر يفحص آلاف المناطق الصغيرة في الشريحة الرقمية ويستخدم آلية انتباه موجهة باللغة للتركيز على المناطق التي تتطابق مع أوصاف الخبراء للأنسجة الليفية الفقيرة بالمناعة.
مزج الفحوص والشرايح لإشارات أقوى
في 126 مريضاً بالورم الحبلوي لديهم رنين مغناطيسي مطابق وشرائح باثولوجية وبيانات RNA ومتابعة، تفوق النموذج الذكي المندمج على النماذج التي استخدمت الرنين المغناطيسي فقط أو الشرائح فقط. اتفقت توقعاته للدرجات الجزيئية الثلاث بشكل وثيق مع القياسات المستندة إلى الحمض النووي الريبوزي وبقت جيدة المعايرة عبر مستشفيات وأجهزة تصوير مختلفة. عندما وضع الأطباء العلامات بشكل مستقل على المناطق الليفية والمستبعدة مناعياً، كانت «نقاط السخونة» لدى الذكاء الاصطناعي تميل إلى الاشتغال في تلك المناطق نفسها، مما يوحي بأنه يتتبع بيولوجيا حقيقية بدلاً من حجم الورم فقط. كما التقط النموذج القيم التنبؤية: فدرجات الضغوط الليفية وإشاراتها الأعلى المتوقعة ارتبطت ببقاء أسوأ، في حين أن تنوع البيئة الدقيقة المتوقع الأعلى وفر حماية جزئية. أضافت هذه الدرجات المستمدة من الذكاء الاصطناعي إلى عوامل سريرية روتينية حسناً القدرة على تمييز المرضى ذوي المخاطر العالية والمنخفضة مع مرور الوقت.
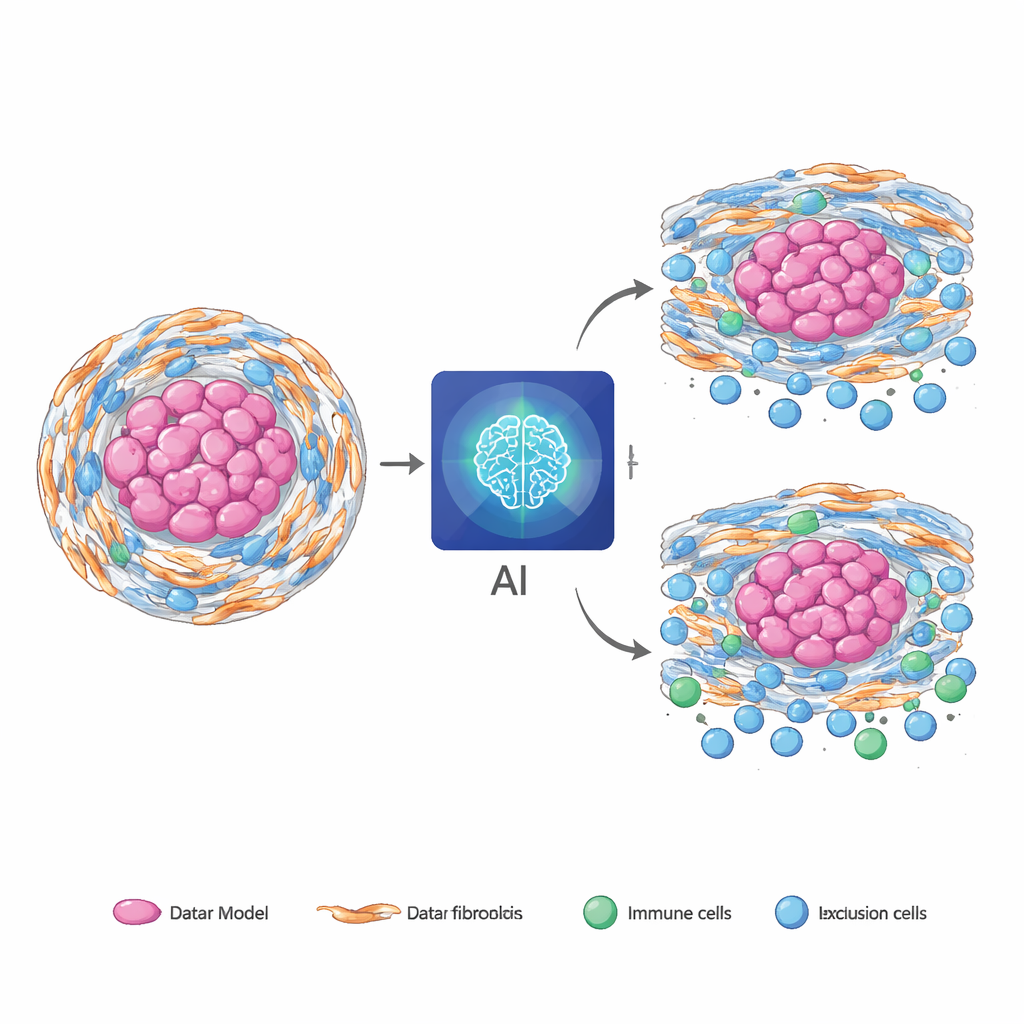
من أورام نادرة إلى سرطانات شائعة
كان اختبار رئيسي ما إذا كان النموذج المدرب كلياً على الورم الحبلوي يمكن استخدامه «كما هو» في سرطانات أخرى أكثر شيوعاً. عند تطبيقه بدون إعادة تدريب على سرطانات البنكرياس والمعدة والقولون/المستقيم من مجموعات بيانات عامة كبيرة، أظهر إصدار الشريحة فقط من النموذج توافقاً ذا دلالة بين توقعاته القائمة على الصور والدرجات المستخرجة حديثاً من RNA. في بعض هذه السرطانات حسّنّت درجات الذكاء الاصطناعي تنبؤ بقاء المرضى متجاوزةً المعلومات السريرية القياسية وساعدت في التمييز بين المرضى الأكثر احتمالية للاستفادة من العلاج الكيميائي. ولتسهيل نشر النهج في أماكن تفتقر إلى الباثولوجيا الرقمية، كوّن الفريق نسخة تعتمد على الرنين المغناطيسي فقط من النموذج متعدد النماذج احتفظت بمعظم القدرة التنبؤية مع تشغيل أسرع واستخدام قدرة حوسبة أقل.
ما الذي قد يعنيه هذا للمرضى
تدعم النتائج مجتمعة الفكرة القائلة بأن الصور الطبية الروتينية تخزن بهدوء معلومات حول الخلايا الداعمة المتوترة، والاستبعاد المناعي، وتنوّع البيئة الدقيقة — وهي ميزات تتطلب عادة اختبارات جزيئية مكلفة. وبينما العمل الحالي رجعي ويحتاج إلى تحقق استباقي، فإنه يشير إلى مستقبل يمكن فيه للمسح والشريحة القياسية أن تشير غير جراحياً إلى الأورام التي تمتلك حاجزاً ليفياً معادياً للمناعة، وتوجيه من قد يستفيد من اختبارات إضافية أو علاجات مصممة خصيصاً، وكل ذلك عبر أنواع متعددة من السرطان دون عبء إضافي على المرضى.
الاستشهاد: Zheng, BW., Xia, C., Tang, M. et al. Decoding the ERS–CAF immunoregulatory axis via multimodal AI and its pan-cancer prognostic and therapeutic predictive value. npj Digit. Med. 9, 199 (2026). https://doi.org/10.1038/s41746-026-02388-w
الكلمات المفتاحية: البيئة الدقيقة للورم, تصوير السرطان, الذكاء الاصطناعي, الخلايـا الليفيـة, العلاج المناعي