Clear Sky Science · ar
DARE-FUSE: تعلم موجه بالأدلة ومتوافق مع المجال لتجزئة وتصنيف صور الرنين المغناطيسي لأورام الدماغ المشتركة
لماذا تهم فحوصات الدماغ الأكثر ذكاءً
تُعد أورام الدماغ من أكثر التشخيصات إثارة للقلق في الطب، ويُعد التصوير بالرنين المغناطيسي الأداة الأساسية التي يستخدمها الأطباء لرؤية مكان بدء الورم وانتهائه. ومع ذلك، قد يجد أخصائيو الأشعة حتى الخبراء صعوبة في تحديد محيط الورم بدقة وتقييم كيفية تغيُّره مع الزمن، لا سيما عندما تمتد حوافه لتندمج مع نسيج دماغ متورم. تقدم هذه الورقة DARE-FUSE، نظام ذكاء اصطناعي جديد مصمم لقراءة صور رنين الدماغ بشكل أكثر موثوقية، يرسم حدودًا أدق للورم ويقدم تفسيرات أوضح لقراراته لدعم الجراحين وأطباء الأورام والمرضى.
حواف ضبابية وعيادات مزدحمة
في المستشفيات الواقعية، تكون صور رنين الدماغ فوضوية. غالبًا ما يندمج الورم مع التورم المحيط، ويمكن للزرعات المعدنية أن تُشوه الصورة، كما تستخدم المستشفيات إعدادات مسح مختلفة قليلاً. يتعين على أخصائيي الأشعة تمرير مئات الصور يدويًا، وتحديد الورم شريحة بشريحة، ثم تقرير كيفية تصرفه. هذا العمل يستغرق وقتًا ويُجهد ويخضع لاختلاف الآراء بين الخبراء. الأدوات الحالية للذكاء الاصطناعي يمكنها المساعدة في تحديد أورام أو تصنيف الصور إلى «ورم» أو «لا ورم»، لكن معظم الأنظمة تتعامل مع هذه المهام بشكل منفصل، وكثير منها يضعف أداؤه عندما تأتي الصور من مراكز جديدة أو تحتوي على نمو هامشي طفيف وغير منتظم.
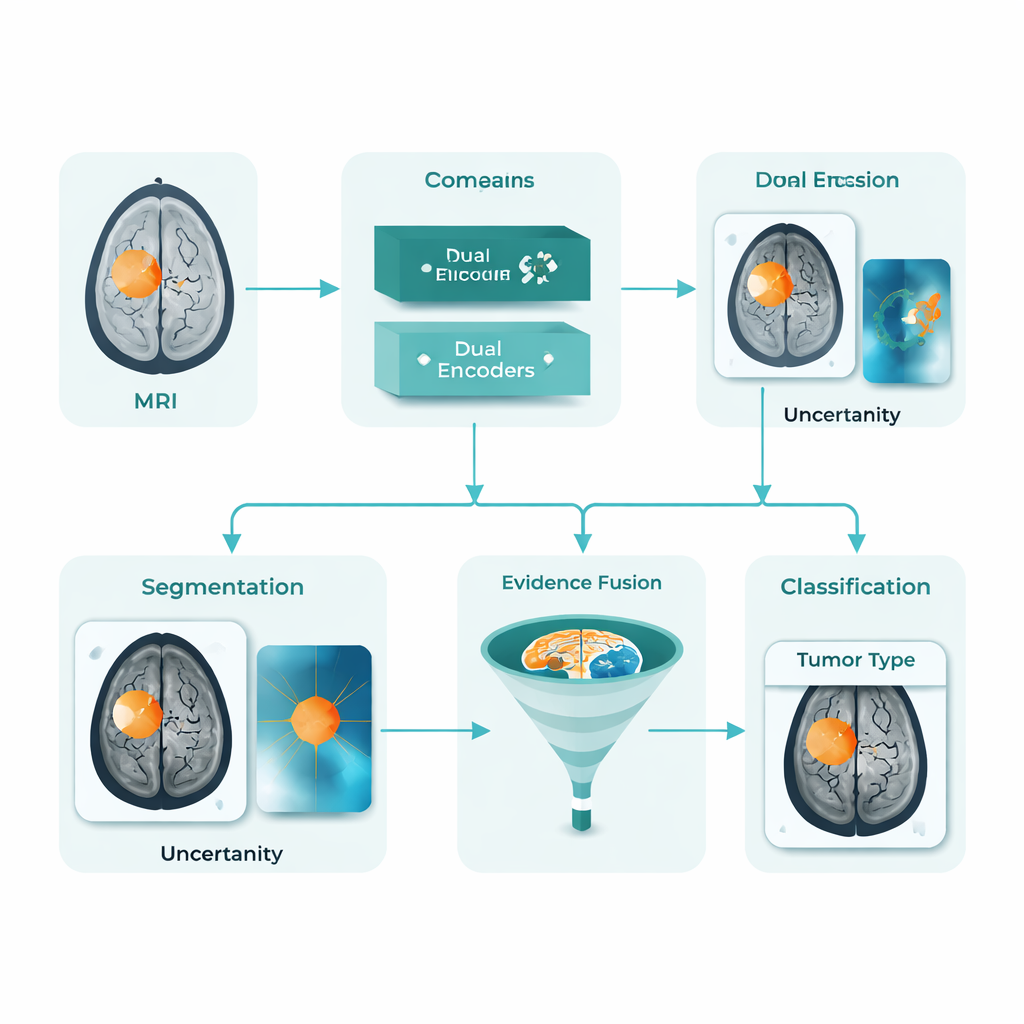
مساعد ذكاء اصطناعي موحَّد لخريطة الورم والتسميات
يعالج DARE-FUSE عدة عقبات في وقت واحد. بُني كنظام واحد يقوم بكل من تتبع الورم في كل شريحة رنين (التجزئة) وتصنيف الصور الكاملة إلى مجموعات تشخيصية (التصنيف). في جوهره يعمل جانبان متعاونان: شبكة مخصصة للأشكال والتجاويف التفصيلية، وأخرى موجهة للنمطيات العالمية التي تميّز بين أنواع الأورام المختلفة. وحدة محاذاة خاصة تبقي هذين الجانبين متزامنين عبر المستشفيات وأجهزة المسح، بحيث لا تؤثر الميزات المتعلمة من مجموعة بيانات واحدة سلبًا على الأداء في أخرى. كما يقدر النظام مستوى اليقين الخاص به، مما يوسم المناطق التي يكون فيها أقل تأكدًا بالنسبة لمحيط الورم الدقيق—وهو أمر حيوي للاستخدام السريري الآمن.
استخدام دلائل من خرائط الحرارة وإعادة بناء «خالية من الورم»
بدلاً من الاعتماد على إشارة واحدة، يتعلم DARE-FUSE من أنواع متعددة من الأدلة. ينتج أحد الفروع خرائط حرارة توضح أي أجزاء الدماغ تدعم قرار التصنيف بقوة. يستخدم فرع آخر نموذجًا توليديًا لتخيل كيف قد تبدو نفس الصورة لو تمت إزالة الورم، ثم يقارن نسخة «خالية من الورم» مع الأصلية. الاختلافات بين النسختين تبرز تغيُّرات هيكلية دقيقة وحواف قد لا تظهر بقوة في خريطة الحرارة الاعتيادية. ثم يجمع وحدة الدمج هذه الدلائل في «خريطة أولوية للورم» مستمرة: تُعامل المناطق التي تتفق فيها عدة مصادر كجزء مركزي من الورم، بينما تُضاف المناطق الأقل يقينًا بحذر وتُخفَّض أهميتها عندما يكون اليقين منخفضًا. هذا الأساس المدمج يوجّه المحيط النهائي، مما يساعد على تجنب كل من جيوب الورم الفائتة والجزر الخاطئة في الأنسجة السليمة.
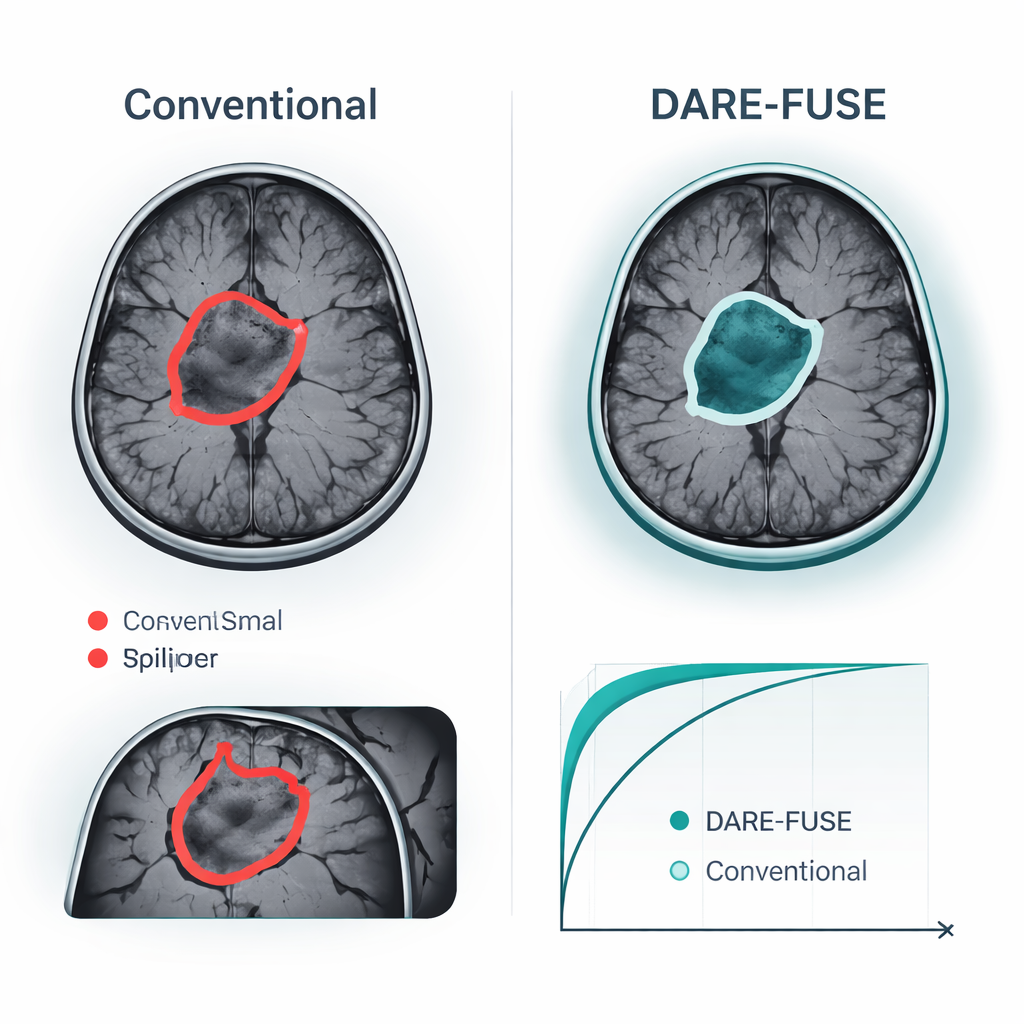
مكاسب مثبتة على مجموعات بيانات أورام الدماغ العامة
اختبر المؤلفون DARE-FUSE على ست تحديات كبيرة ومتعددة المراكز لأورام الدماغ (سلسلة BraTS) وأربع مجموعات رنين عامة مستخدمة لتصنيف مستوى الصورة. عبر جميع إصدارات BraTS، طابقت المنظومة أو تجاوزت أفضل النماذج الحديثة للتعلم العميق، محققة تراكبًا أعلى قليلًا بين أقنعة الورم المتوقعة ورسومات الخبراء، وأخطاء أصغر باستمرار في قياس سطح الورم. كانت هذه المكاسب بارزة بشكل خاص في الحالات الصعبة: الأورام الصغيرة، الحواف منخفضة التباين، والأشكال المعقدة وغير المنتظمة. في مهام التصنيف—تحديدًا، على سبيل المثال، ما إذا كانت الصورة تُظهر غليوما أو سحائيّة أو ورم النخامية أو لا ورم—تفوقت DARE-FUSE أيضًا على قواعد قوية تعتمد على المحوِّلات والتحكيم الضعيف من حيث الدقة ومقياس التمييز القياسي (AUC). والأهم من ذلك، عندما قلل الباحثون عمدًا عدد التعليقات التفصيلية، تدهور أداء النظام الجديد بشكل تدريجي وحافظ على ميزة مقارنة بالطرق شبه الموجهة والضعيفة الإشراف.
ماذا قد يعني هذا للمرضى
بالنسبة للمرضى والسريريين، الوعد الرئيسي لـ DARE-FUSE ليس خوارزمية جديدة لافتة فقط، بل دعم تصويري أكثر اعتمادية وتفسيرًا. على أرض الواقع، يمكن للنظام اقتراح محيط الورم، تمييز المناطق التي يكون فيها أقل ثقة، وعرض خرائط حرارة تشرح أي مناطق الصورة تقود تصنيفه. قد يقبل الأطباء المناطق ذات اليقين المنخفض كنقطة انطلاق، ثم يوجّهون انتباههم إلى المناطق الموسومة بدلًا من إعادة رسم كل شيء من الصفر. قياسات أكثر دقة واتساقًا لحجم وشكل الورم يمكن أن تحسن تخطيط العلاج، استهداف العلاج الإشعاعي، ومتابعة الاستجابة مع الزمن. وبينما يؤكد المؤلفون أن أداتهم مساعد—وليس بديلاً—لحكم الخبراء، تشير نتائجهم إلى أن أنظمة الذكاء الاصطناعي يمكنها رؤية الأورام بوضوح أكبر والتواصل بشأن مستوى ثقتها بطرق يمكن للأطباء العمل بناءً عليها.
الاستشهاد: Liu, Y., Sun, C., Niu, Y. et al. DARE-FUSE: domain aligned evidence guided learning for joint brain tumor MRI segmentation and classification. npj Digit. Med. 9, 178 (2026). https://doi.org/10.1038/s41746-026-02365-3
الكلمات المفتاحية: تصوير بالرنين المغناطيسي لأورام الدماغ, تجزئة الصور الطبية, التعلم العميق في الأشعة, دعم القرار السريري, الذكاء الاصطناعي الواعي بعدم اليقين