Clear Sky Science · ar
إطار عمل تعاوني مدعوم بنماذج لغة كبيرة لتقييم وإدارة ألم السرطان معزَّز بالمعرفة
لماذا يهم توفير رعاية ألم أكثر ذكاءً
ألم السرطان ليس مجرد أثر جانبي مزعج—بل يمكن أن يهيمن على الأشهر أو السنوات الأخيرة من حياة الشخص، مما يجعل النوم والحركة وحتى المحادثات البسيطة صعبة. رغم وجود مسكنات قوية، فإن استخدامها بشكل آمن وفعّال أمر معقَّد، خاصة مع اختلاف كل مريض في نوع السرطان والأمراض الأخرى والأدوية. تصف هذه المقالة OncoPainBot، إطار عمل جديداً للذكاء الاصطناعي قائمًا على نماذج لغة كبيرة يهدف إلى مساعدة الأطباء في تحليل الملفات المعقدة، والالتزام بالإرشادات المحدثة، وتصميم خطط ألم أكثر أمانًا وتخصيصًا للأشخاص المصابين بالسرطان.
مشكلة صعبة في رعاية السرطان اليومية
ينشأ ألم السرطان من مصادر متعددة: أورام تضغط على العظام أو الأعصاب، عمليات جراحية، العلاج الكيميائي، والعلاج الإشعاعي. يعيش ما يصل إلى 70% من مرضى السرطان المتقدم مع ألم شديد، ومع ذلك غالبًا ما تكون التخفيفات غير كاملة. يجب على الأطباء الموازنة بين الأفيونات، والأدوية غير الأفيونية، والعلاجات المرافقة مع مراقبة الآثار الجانبية الخطرة، لا سيما لدى المرضى ذوي وظائف الكبد أو الكلى الهشة. تعتمد أدوات تقييم الألم الحالية بشدة على مقاييس موجزة وملاحظات نصية حرة، والتي قد تختلف من طبيب لآخر ومن مستشفى لآخر. ونتيجة لذلك، قد تتباين قرارات العلاج بشكل واسع، وقد تُفوت فرص لتحسين راحة المرضى.
تحويل النص الطبي إلى رؤى قابلة للتنفيذ
نماذج اللغة الكبيرة مثل ChatGPT وClaude قادرة على قراءة وتلخيص وثائق طويلة ومبعثرة، مما يجعلها جذابة للعمل الطبي. لكن «الدردشات» العادية غير آمنة لتقييم ألم السرطان لأنها قد تختلق تفاصيل، أو تفوّت تداخلات دوائية، أو تتجاهل الإرشادات الأحدث. يتعامل OncoPainBot مع هذه المشاكل بدمج نماذج اللغة الكبيرة مع قاعدة معرفة مُنقّحة مبنية من إرشادات ألم من منظمات سرطانية رئيسية، وعن طريق تقسيم العمل إلى أربعة «وكلاء» متعاونين، كل واحد منهم يعكس دورًا سريريًا حقيقيًا. يستخرج وكيل المعلومات حقائق رئيسية عن ألم المريض من السجلات الإلكترونية، ويستدل وكيل آخر على نوع الألم، ويصوغ وكيل ثالث خطة علاج، ويجري وكيل رابع فحصًا أمنيًا يركز على تداخلات الأدوية ووظيفة الأعضاء واحتياجات المراقبة.
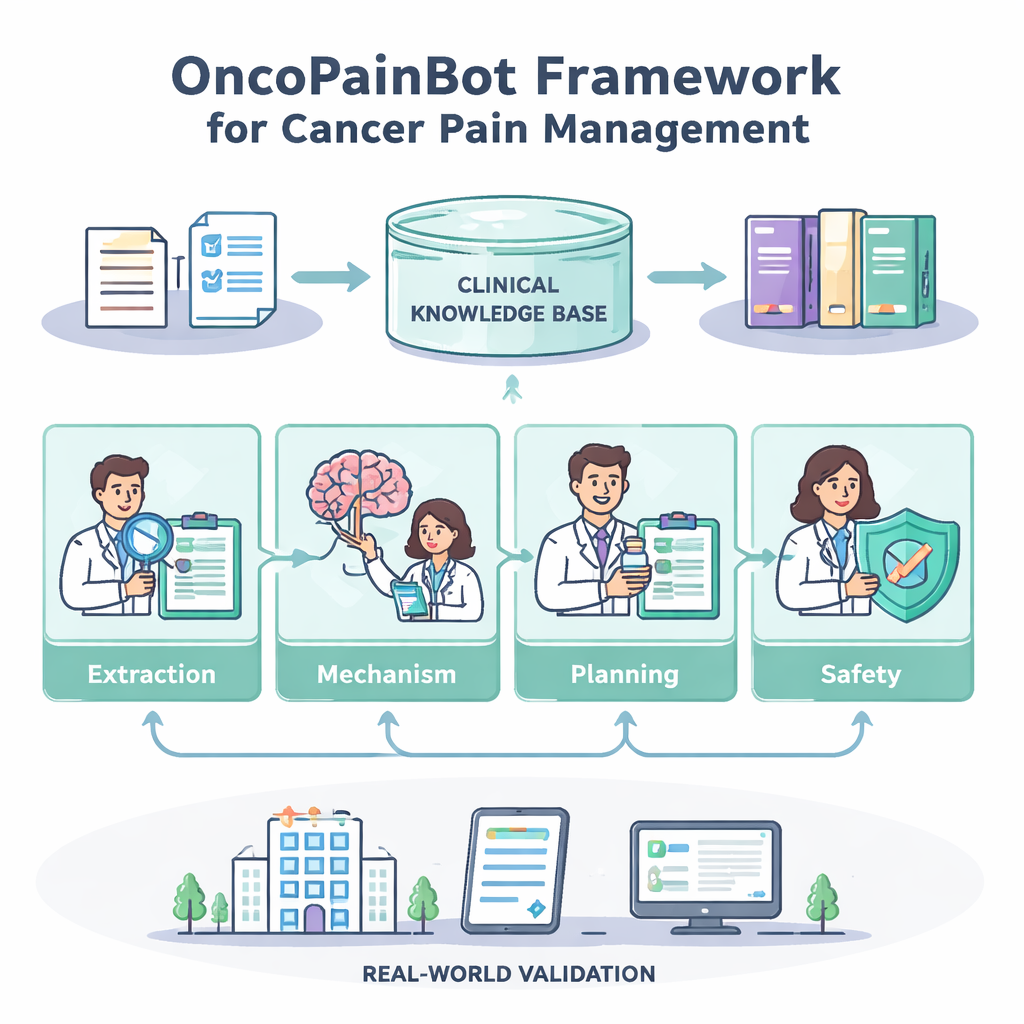
كيف يعمل فريق الوكلاء الأربعة
يقرأ وكيل استخراج الألم الملاحظات النصية الحرة ويحوّلها إلى صورة منظمة: موضع الألم، وشدته، وما الذي يخففه أو يزيده، والأدوية التي جُربت بالفعل. ثم يستخدم وكيل استدلال آلية الألم تلك الصورة للاستنتاج ما إذا كان الألم ناتجًا أساسًا عن تلف في الأنسجة، أو تلف عصبي، أو مزيج—وهو مؤشر مهم لاختيار الأدوية المناسبة. بعد ذلك، يستعين وكيل تخطيط العلاج بقاعدة المعرفة المستندة إلى الإرشادات عبر تقنية تُسمى التوليد المعزز بالاسترجاع، التي تسمح للنموذج بجلب مقاطع محددة ومحدثة بدل الاعتماد على الذاكرة فقط. يقترح خططًا تدريجية—عادة مستندة إلى «سلم الألم» لمنظمة الصحة العالمية—بما في ذلك جرعات بداية، وطرق تعديلها، وجرعات إنقاذ لنوبات الألم المفاجئة. أخيرًا، يعمل وكيل فحص السلامة كصيدلي حذر، يفحص مشاكل الجرعات، والتراكيب الخطرة، والمعلومات المخبرية المفقودة، ويعلّم على الحالات التي تكون فيها البيانات رقيقة جدًا بحيث لا تدعم توصية قاطعة.
وضع النظام قيد الاختبار
لاختيار أفضل نموذج لغة أساسي، قارن الباحثون بين سبعة أنظمة رائدة على عدة اختبارات للإجابة على الأسئلة الطبية. برز Claude 4 كالأدق، وإن لم يكن الأسرع، ولذلك اختير ليكون «عقل» OncoPainBot. ثم قيّموا طرقًا مختلفة لربط هذا العقل بمكتبة الإرشادات ووجدوا أن استراتيجية «هجينة» للاسترجاع—باستخدام مطابقة الكلمات المفتاحية والبحث الدلالي الأعمق معًا—أعطت الإجابات الأكثر موثوقية. مع إعداد هذا النظام، شغّل الفريق OncoPainBot على 516 سجل ألم سرطان حقيقي من مستشفى صيني كبير. طابقت تقارير النظام المكتوبة ملاحظات الأطباء في اللغة والمحتوى عن قرب، واتّفقت اقتراحات علاج الألم مع وصفات الأطباء الحقيقية في نحو 84% من الحالات. ومن المهم أن معظم الاختلافات ناتجة عن فروق دقيقة خاصة بكل مريض—مثل التحمل غير الموثق للأفيونات أو فشل عضوي معقد—بدلاً من اختيارات دوائية خاطئة بوضوح.
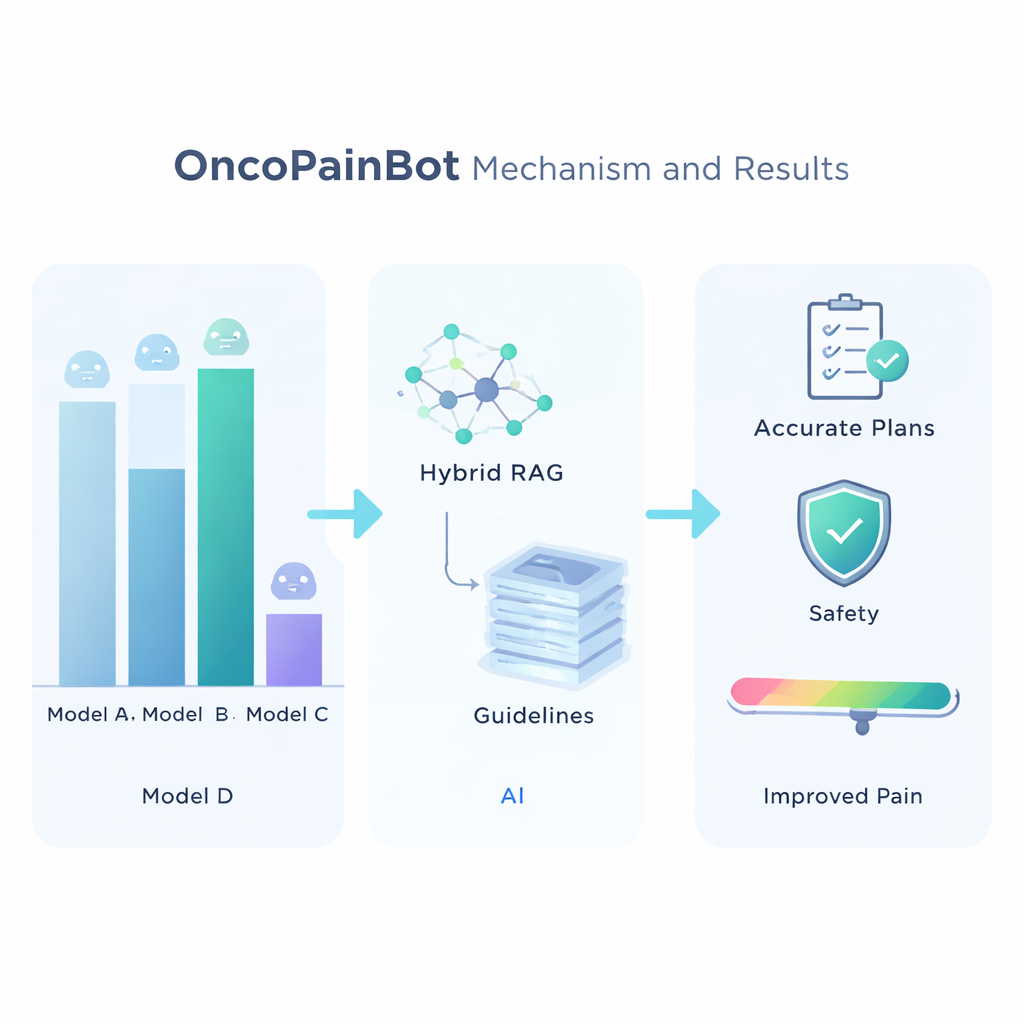
ماذا قد يعني هذا للمرضى
بالنسبة للأشخاص المصابين بالسرطان، فإن وعد OncoPainBot ليس أن تتولى آلة علاجهم، بل أن تمنح فريق الرعاية رأيًا ثانويًا أدق وأكثر اتساقًا. صُمم الإطار كأداة «الطبيب في الحلقة»: يبرز سمات الألم التي قد تكون مدفونة في الملاحظات، يقترح خيارات متوافقة مع الإرشادات، وينبه إلى مخاوف السلامة، مع ترك القرارات النهائية للأطباء البشر. يؤكد المؤلفون أن عملهم لا يزال في مرحلة مبكرة استعادية وقد جُرّب في مركز واحد فقط؛ لا تزال هناك حاجة إلى تجارب في الوقت الفعلي عبر مستشفيات متعددة. ومع ذلك، تشير نتائجهم إلى أن الذكاء الاصطناعي المصمم بعناية—المرتبط بأدلة متينة ومنطق شفاف—قد يساعد على توحيد رعاية ألم السرطان، وتقليل أخطاء الجرعات الخطرة، والأهم من ذلك، زيادة احتمال أن يقضي المرضى وقتًا أقل في المعاناة ووقتًا أكثر في عيش حياتهم.
الاستشهاد: Liu, H., Hu, Y., Li, D. et al. LLM-driven collaborative framework for knowledge-enhanced cancer pain assessment and management. npj Digit. Med. 9, 180 (2026). https://doi.org/10.1038/s41746-026-02362-6
الكلمات المفتاحية: إدارة ألم السرطان, دعم اتخاذ القرار السريري, نماذج اللغة الكبيرة, علاج الأفيونات, التوليد المعزز باسترجاع المعلومات