Clear Sky Science · ar
HMC-transducer: ناقل هرمي mamba-CNN لتجزئة أورام الكبد القوية
لماذا تهم خرائط الأورام الأفضل
بالنسبة للمرضى المصابين بسرطان الكبد أو الكلى، يعتمد الأطباء على الأشعة المقطعية لاتخاذ قرار ما إذا كان من الممكن إجراء جراحة أو إشعاع أو علاجات أخرى. خطوة رئيسية هي رسم حدود دقيقة لكل ورم في ثلاثة أبعاد، وهي مهمة بطيئة ومتعبة وغير متسقة عند أدائها يدوياً. يقدم هذا البحث نوعاً جديداً من أنظمة الذكاء الاصطناعي القادرة على تتبع هذه الأورام تلقائياً بدقة واتساق أكبر من الطرق السابقة، ما قد يساعد الأطباء في تخطيط العلاجات بسرعة وثقة أكبر.
رؤية الصورة كاملة في مسوحات ثلاثية الأبعاد
تعد أورام الكبد صعبة التحديد لأنها تختلف كثيراً في الحجم والشكل وغالباً ما تمتزج مع الأنسجة المحيطة. أدوات التعلم العميق التقليدية المعروفة بالشبكات التلافيفية (CNNs) جيدة جداً في التقاط التفاصيل الدقيقة في الصور، لكنها تعاني في فهم العلاقات بعيدة المدى—كيف يرتبط تركيب في جزء من المسح بآخر بعيد. النماذج الأحدث المعروفة بالمحولات (Transformers) تستطيع التقاط هذا السياق الواسع لكنها تصبح مكلفة جداً عند العمل على مجلدات ثلاثية الأبعاد كبيرة من الأشعة المقطعية، مما يحد من قابلية تطبيقها في المستشفيات الحقيقية. يجادل المؤلفون بأنه لكي تنجح فعلاً، يجب أن يكون النظام دقيقاً في التفاصيل وواعياً للسياق العام في الوقت نفسه، من دون الحاجة إلى طاقة حاسوبية بمستوى الحواسيب العملاقة.
عقل هجيني جديد للصور الطبية
لتلبية هذا الاحتياج، صمم الباحثون HMC-Transducer، بنية هجينة تدمج بين الشبكات التلافيفية ونوع أحدث من النماذج يُعرف بنماذج الحالة الزمنية، وتحديداً نموذج يُدعى Mamba. تركز أجزاء الـCNN على التفاصيل المحلية الواضحة مثل حواف الأورام الحادة. تتتبع أجزاء Mamba كيفية تدفق المعلومات عبر المسح ثلاثي الأبعاد بأكمله مع تكلفة حسابية خطية فقط، متجنبة النمو الحاد الذي تسببه المحولات. كتلة "Mamba ثلاثية الأبعاد الواعية بالاتجاه" المصممة خصيصاً تعالج المسح على طول ثلاثة محاور—من الرأس إلى القدم، ومن اليسار إلى اليمين، ومن الأمام إلى الخلف—بحيث يحترم النموذج البنية التشريحية الحقيقية بدلاً من تسطيح الحجم إلى سلسلة أحادية البعد من الأرقام.
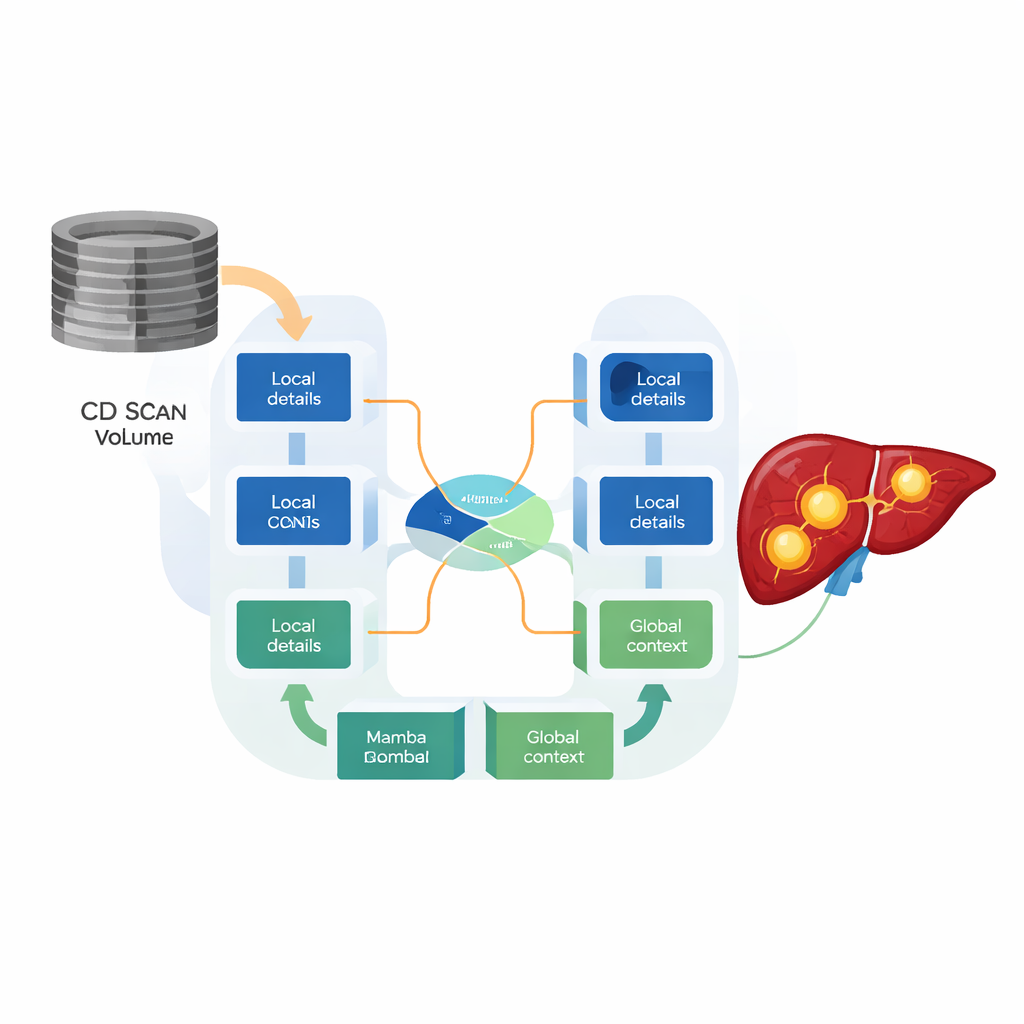
ترك النموذج يقرر ما المهم وأين
ابتكار محوري هو كيفية دمج هذين النوعين من الميزات. بدلاً من مجرد جمع أو تكديس مخرجات الـCNN وMamba، يستخدم HMC-Transducer آلية دمج بمفتاح (gated fusion) تتعلم، لكل منطقة دقيقة في المسح، مدى الثقة بالتفاصيل المحلية مقابل السياق العام. في المناطق ذات الحدود الواضحة والحادة يمكن للمفتاح الاعتماد على ميزات الـCNN؛ أما حيث تكون الأورام ضبابية أو مخترقة للأنسجة أو قريبة من أوعية دموية كبيرة، فيمكنه إعطاء وزن أكبر للرؤية الأوسع من Mamba. تظهر التجارب أن هذا المزج التكيفي ينتج تجزئات أدق وأكثر استقراراً من كلٍ من الـCNN أو نماذج Mamba بمفردها، وتحسناً واضحاً على التصميمات الهجينة السابقة التي تدمج الميزات بطريقة ثابتة غير متكيفة.
مُختبر عبر أعضاء وأجهزة ومستشفيات
قيّم الفريق منهجهم على ثلاث مجموعات بيانات عامة رئيسية: LiTS17 وMSD-Liver لأورام الكبد، وKiTS21 لأورام الكلى. عبر هذه المقاييس، حقق HMC-Transducer تراكباً أعلى باستمرار مع خرائط الأورام المرسومة من الخبراء مقارنة بالخطوط الأساسية القوية، بما في ذلك nnU-Net المستخدم على نطاق واسع ونماذج المحولات وMamba الرائدة. كما عمم النموذج أداءً أفضل عند تدريبه على مجموعة بيانات كبدية واحدة واختباره على أخرى مُجمعة في مستشفيات مختلفة—وضع يحاكي النشر الواقعي مع اختلاف الأجهزة وبروتوكولات التصوير. في اختبارات مواجهة مباشرة، تأخرت النماذج الأساسية الكبيرة مثل SAM ونسخها الطبية عند استخدامها مباشرة من دون تدريب متخصص، مما يبرز حاجة الأنظمة المصممة خصيصاً والمضبوطة بعناية لاتخاذ قرارات بكسل-ببكسل مهمة في الطب.
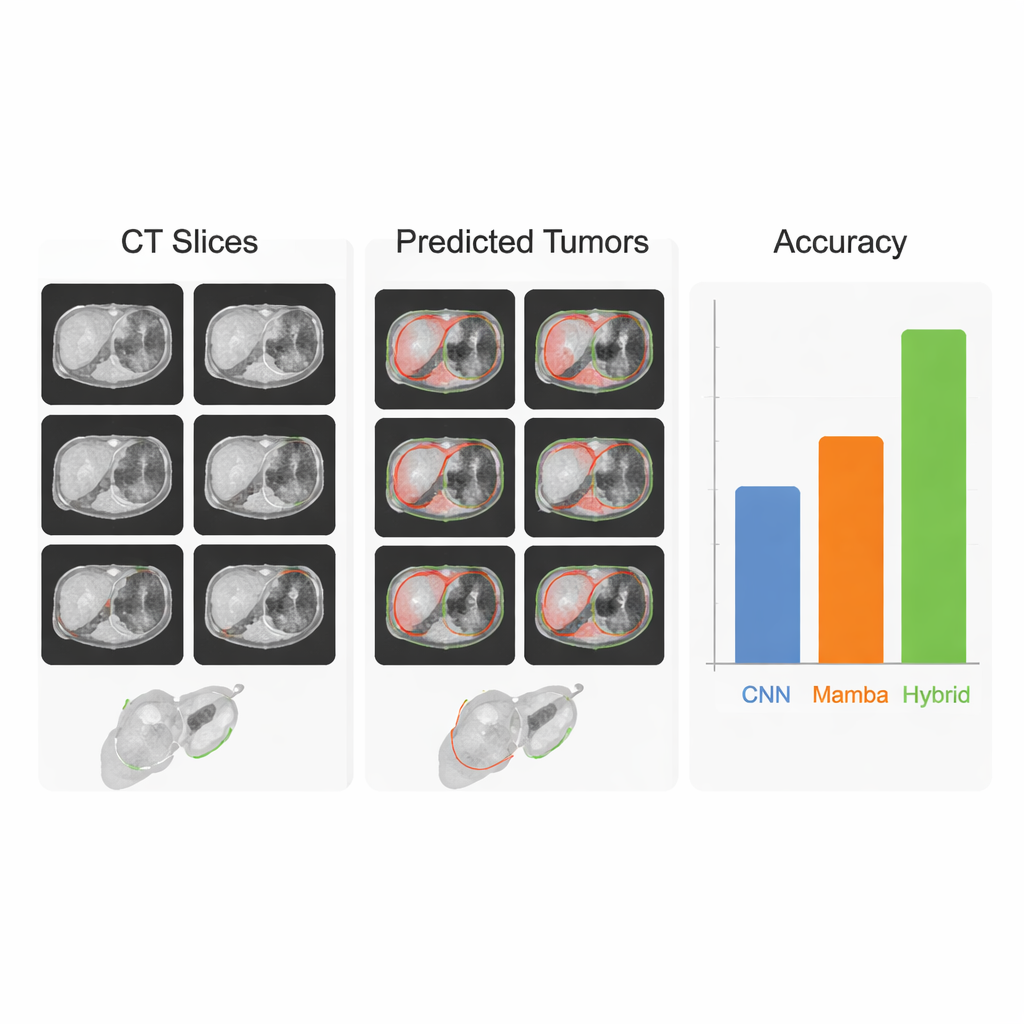
من نتائج المختبر إلى المساعدة السريرية
للغير متخصص، الخلاصة أن هذا العمل يقرب برمجيات رسم الأورام مما يحتاجه الأطباء فعلاً: أداة موثوقة وفعالة في الوقت نفسه. من خلال الجمع بين طريقتين تكميليتين للرؤية—إحداهما بارعة في التفاصيل الصغيرة، والأخرى في الصورة الكبرى—يرسم HMC-Transducer أورام الكبد والكلى بدقة وموثوقية أكبر من الأنظمة السابقة، مع القدرة على العمل على أجهزة المستشفيات المتقدمة الاعتيادية. وعلى الرغم من أن هناك خطوات إضافية لازمة قبل الاستخدام السريري الروتيني، بما في ذلك اختبارات أوسع على أعضاء وأنواع تصوير أخرى، يمثل النهج تقدماً واعداً نحو خرائط أورام ثلاثية الأبعاد آلية قد تدعم تشخيصات أسرع وعمليات جراحية أكثر دقة ورعاية سرطانية أكثر تخصيصاً.
الاستشهاد: Zhu, J., Xu, C., Lei, C. et al. HMC-transducer: hierarchical mamba-CNN transducer for robust liver tumor segmentation. npj Digit. Med. 9, 176 (2026). https://doi.org/10.1038/s41746-026-02361-7
الكلمات المفتاحية: تجزئة أورام الكبد, الذكاء الاصطناعي في التصوير الطبي, التعلم العميق, تحليل الأشعة المقطعية, الشبكات العصبية الهجينة