Clear Sky Science · ar
الترميز التلقائي المقنع، التدريب المسبق القابل للتعميم، والخبراء المتكاملون لتحسين تقسيم الأورام الدبقية
لماذا تكون الصور الأذكى مهمة لأورام الدماغ
الأورام الدماغية المعروفة بالدبقيات تُعدّ من أكثر أنواع السرطان فتكاً، ومع ذلك لا يزال الأطباء يقضون وقتاً طويلاً في تتبّع حدود الورم يدوياً على صور الرنين المغناطيسي. هذا التحديد الدقيق يوجّه الجراحة والإشعاع، لكنه قد يستغرق 15–20 دقيقة لكل مريض ويجب تكراره مع مرور الوقت. تقدّم الدراسة نظام ذكاء اصطناعي اسمه MAGPIE يتعلّم من عشرات الآلاف من صور الدماغ دون تسميات بشرية، ثم يحتاج فقط إلى عدد قليل من الحالات المصنفة بخبرة ليقدّم خرائط موثوقة للأورام الدبقية. بالنسبة للمرضى، قد يعني ذلك تخطيط علاج أسرع وأكثر اتساقاً حتى في المستشفيات التي تفتقر إلى مجموعات بيانات كبيرة ومنسقة.
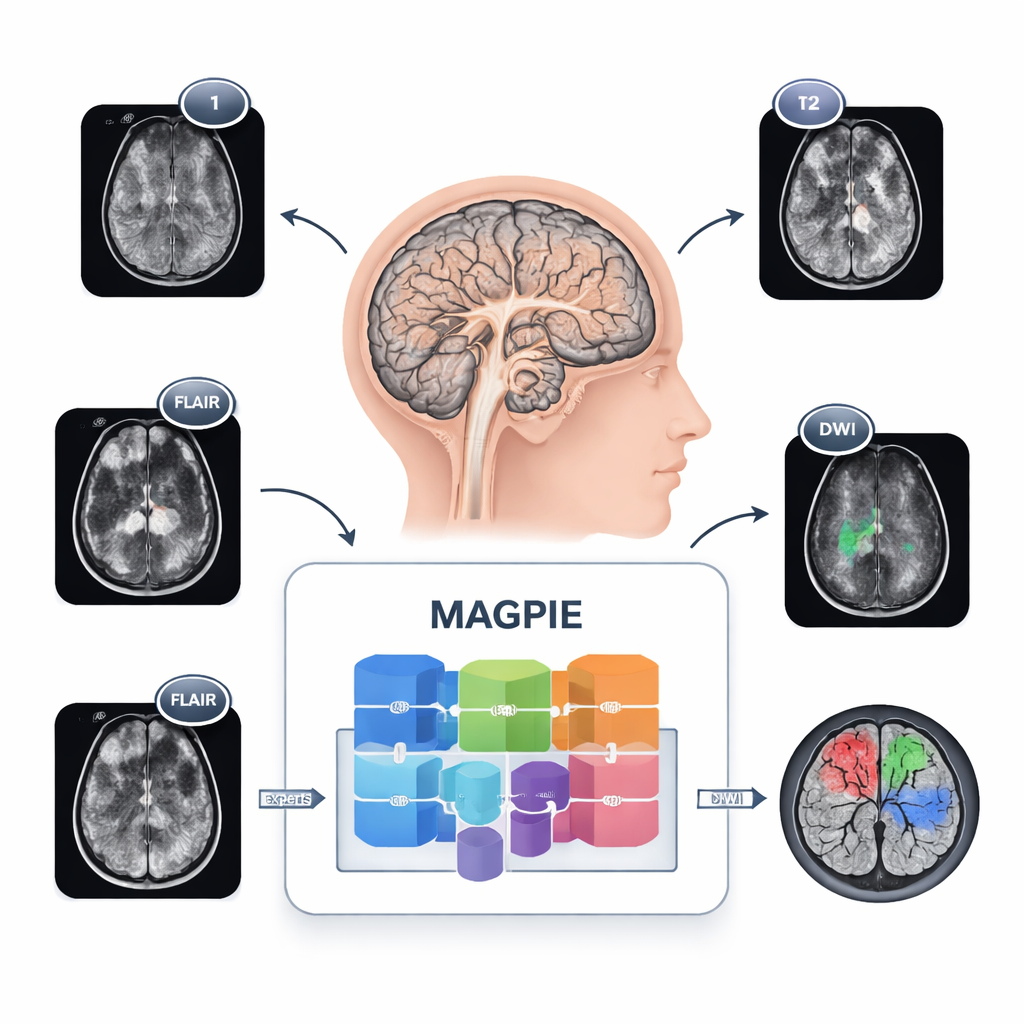
رؤية الأورام بطريقة جديدة
من الصعب رسم خرائط الأورام الدبقية لأنها لا تتكوّن على شكل كتل منتظمة. تنتشر خلايا السرطان على امتداد توصيلات الدماغ، مكوّنة حدوداً غامضة وبقعاً ساتلية صغيرة يصعب رصدها. كما أن المستشفيات تختلف في إعدادات الرنين المغناطيسي وتراكيب السلاسل المستخدمة، لذلك قد يتعثر نموذج مدرّب في مكان واحد عند تطبيقه في مكان آخر. يتعامل MAGPIE مع كل ذلك دفعة واحدة. خضع أولاً لمرحلة تعرّض شملت 43,505 صور رنين مغناطيسي للدماغ غير معنونة مأخوذة من دراسات وأنواع أجهزة مسح متعددة. خلال هذه المرحلة تعلّم أنماطاً عامة للأنسجة السليمة والمريضة بمحاولة إعادة أجزاء مفقودة من الصور ومقارنة صور معدّلة مختلفة لنفس الدماغ، مما دفعه للتركيز على ميزات مستقرة ومفيدة بدل التفاصيل الهشة على مستوى البكسل.
مشاركة العمل بين خبراء متعددين
بدلاً من أن يعمل كنموذج واحد ضخم، يحتوي MAGPIE على «خليط من الخبراء» داخله. عندما يحلل صورة جديدة، يُفعّل فقط مجموعة صغيرة من ثمانية شبكات فرعية متخصصة لكل منطقة من الصورة. مع التدريب، تتوزع هذه الخبرات تلقائياً على المهام: فبعضها يصبح حساساً للحافة المضيئة النامية للنمو؛ وبعضها يركّز على النواة الميتة؛ وبعضها يتعرّف على حلقة الوذمة المحيطة؛ وبعضها يركّز على الخلفية السليمة وحدودها. يوضّح المؤلفون ذلك بقياس مدى تداخل نشاط كل خبير مع مناطق الورم المختلفة المرسومة بواسطة أخصائيي الأشعة. هذا التقسيم للعمل يحسّن الدقة مع الحفاظ على موارد الحوسبة—فقط نحو نصف معلمات النموذج تكون نشطة لأي رقعة معينة.
التعامل مع صور العالم الواقعي الفوضوية
بروتوكولات الرنين المغناطيسي السريرية بعيدة عن التوحيد. لدى بعض المرضى أربع سلاسل، ولدى آخرين أقل؛ وأجهزة من شركات مختلفة تنتج صوراً مختلفة بفوارق دقيقة. يعامل تصميم MAGPIE كل سلسلة رنين مغناطيسي كـ «رمز» منفصل ويتعلّم مقدار الأهمية التي يمنحها لكل واحدة تلقائياً، بدلاً من توقع مجموعة ثابتة من المدخلات بترتيب ثابت. هذا النهج غير المعتمد على القنوات يمكّن النظام من التكيّف إذا، على سبيل المثال، كانت سلسلة معززة بالمادة التباينية مفقودة لكن سلسلة FLAIR متوفرة. كما يستخدم النموذج آليات انتباه متقدمة تتيح له «الرؤية البعيدة» لالتقاط الانتشار على مسافات طويلة على طول حزم المادة البيضاء و«الرؤية الدقيقة» لرصد آفات صغيرة جداً يبلغ قطرها بضعة مليمترات.
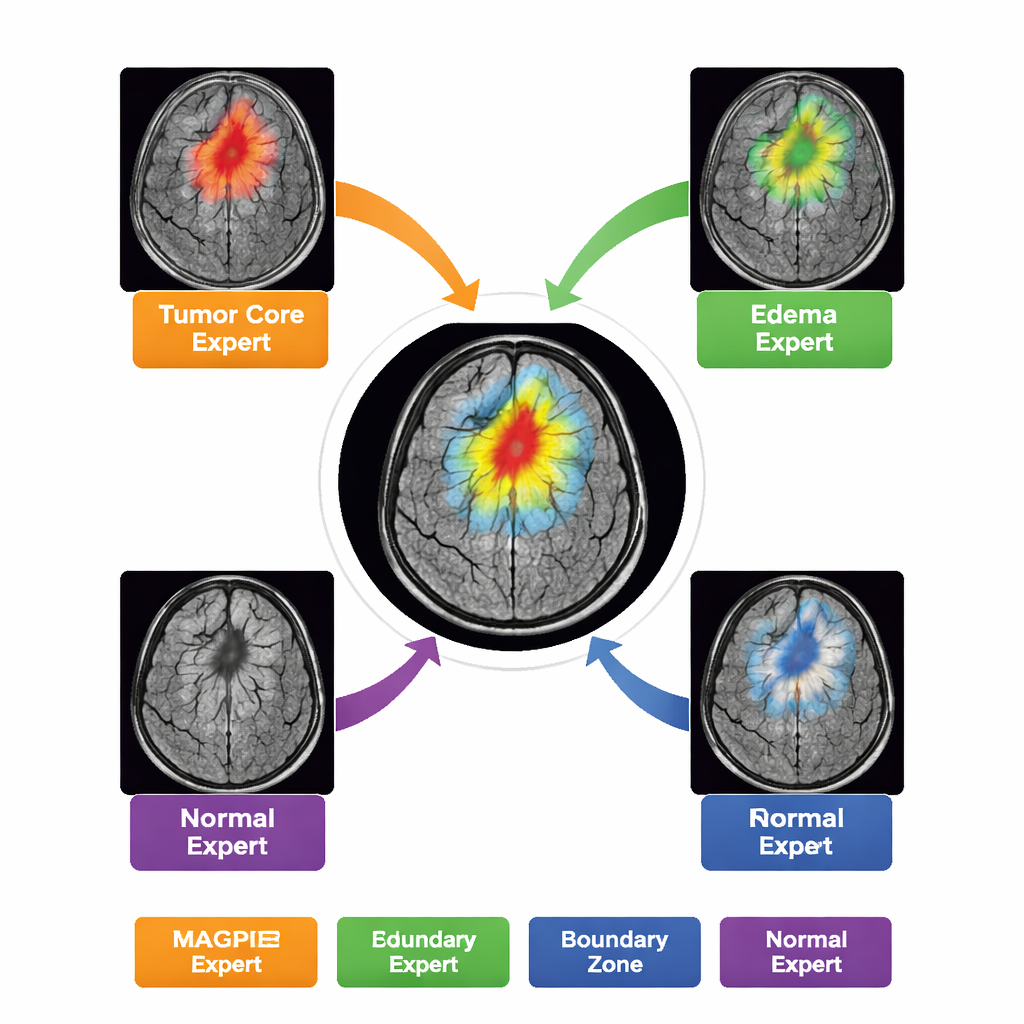
الإنجاز بالمزيد مع عدد أقل بكثير من التسميات
بعد التدريب المسبق، قام الباحثون بضبط MAGPIE بدقة على 20 حالة دبقية معنونة بالكامل فقط وقارنوها مع نماذج قياسية مدرّبة من الصفر تحت نفس الظروف. على معيار رئيسي لأورام الدماغ (BraTS21)، حقّق MAGPIE درجة Dice — مقياس شائع للتداخل في التصوير الطبي — تبلغ حوالي 61%، متفوقاً بنحو 2.6 نقطة مئوية على أفضل نسخة مُدرّبة من الصفر ومتجاوزاً طريقة قوية سابقة في التعلّم الذاتي دون إظهار أي «نقل سلبي» ضار. على بيانات صعبة خارج التوزيع—صور من أمراض وأنواع أجهزة وإعدادات صور مختلفة—صمد أيضاً بشكل أفضل، حيث بلغ أكثر من 70% Dice على مجموعة بيانات لآفات المادة البيضاء دون أي ضبط إضافي. والأهم أن هذا المستوى من الأداء عادةً ما يتطلب في العادة حوالي 400 حالة معنونة؛ يصل MAGPIE إليه بجهد يقارب 5% فقط من ذلك.
ما قد يعنيه ذلك للمرضى والعيادات
لغير المتخصصين، الرسالة الأساسية هي أن MAGPIE يحوّل جبالاً من صور الرنين المغناطيسي غير المعنونة إلى مساعد قوي يحتاج إلى تدريب خبير قليل جداً ليصبح ذا فائدة سريرية. يمكنه رسم حدود واقعية لأورام الدماغ المعقّدة، واكتشاف البقع الساتلية الصغيرة التي تفوّتها أنظمة أخرى، والاستمرار في العمل بشكل موثوق عندما تأتي الصور من أجهزة غير مألوفة أو تفتقر إلى سلاسل معينة. قد يؤدي هذا المزيج إلى تقليل وقت عنونة الأطباء الشعاعيين بحوالي 95%، وخفض الحواجز أمام المستشفيات الصغيرة لنشر ذكاء تصويري متقدم، ودعم تخطيط جراحي وإشعاعي أكثر دقة. وعلى الرغم من الحاجة إلى المزيد من التحقق على أنواع الأورام النادرة والحالات منخفضة الدرجة، تظهر هذه الدراسة كيف يمكن للتعلّم الذاتي المصمم بعناية أن يقرب تقطيع أورام الدماغ الفعّال والمقتصد في البيانات من واقع العيادات اليومية.
الاستشهاد: Xie, M., Xiao, Q., Wu, H. et al. Masked autoencoding, generalizable pretraining, and integrated experts for enhanced glioma segmentation. npj Digit. Med. 9, 163 (2026). https://doi.org/10.1038/s41746-026-02347-5
الكلمات المفتاحية: تقسيم الأورام الدبقية, تصوير بالرنين المغناطيسي للدماغ, التعلّم الذاتي المراقبة, خليط من الخبراء, الذكاء الاصطناعي في التصوير الطبي