Clear Sky Science · ar
محور الإشارات AXL–SHC1 يوسّع المقاومة التكيفية لمثبطات التيروسين كيناز الموجَّهة ضد HER2 في سرطانات الرئة والمعدة الشاذة HER2
لماذا تتفوق بعض السرطانات على الأدوية الجديدة
حوّلت الأدوية الموجَّهة للسرطان علاج العديد من المرضى عن طريق استهداف الجزيئات المحددة التي تحفّز نمو الورم. ومع ذلك، حتى مع هذه الأدوية الدقيقة، فإن تحقيق استجابة كاملة ودائمة نادر الحدوث. تطرح هذه الدراسة سؤالاً ملحاً لمرضى سرطان الرئة والمعدة الذين تحرّك الأورام لديهم بواسطة جين يُدعى HER2: لماذا البؤر الخلوية العنيدة تبقى عادة بعد تقلّص الورم المبدئي على حبوب حابسة لـ HER2 وتؤدي لاحقاً إلى الانتكاس—وكيف يمكن للأطباء غلق هذا طريق الفرار منذ البداية؟
نظرة أدق على الأورام المحركة بواسطة HER2
يُعدّ HER2 محور إشارات يساعد الخلايا على النمو والبقاء. عندما يتبدل أو يُنتَج زائدًا، يمكنه تحويل خلايا طبيعية في الثدي أو المعدة أو الرئة إلى خلايا سرطانية. تم تصميم عدة أدوية حديثة تُسمى مثبطات التيروسين كيناز (TKIs) لإيقاف عمل HER2 داخل الخلايا السرطانية. يمكن لهذه الأدوية، بما في ذلك موبوسيرتينيب وأمثالها، أن تقلّص الأورام وتؤخّر التقدم. ومع ذلك، في سرطانات الرئة والمعدة غالباً ما تكون فوائدها مؤقتة. جزء صغير من خلايا الورم ينجح في الصمود خلال الهجوم الدوائي الأولي في حالة تحمل دوائي، ثم يتطور لاحقًا إلى أورام مقاومة تمامًا. فهم ما يبقي هذه الخلايا الناجية على قيد الحياة ضروري لتصميم علاجات أولية أذكى.
حبل نجاة احتياطي يُدعى AXL
فحص الباحثون خطوط خلايا سرطانية للرئة والمعدة ذات تغيرات في HER2 ليروا أي مفاتيح إشارات أخرى تساعد الخلايا على مقاومة مثبطات HER2 الموجَّهة. حدّدوا مستقبلًا يدعى AXL كلاعب رئيسي. عندما تعرّضت الخلايا لأدوية حابسة لـ HER2، تم تنشيط AXL وبقي في حالة تشغيل حتى مع كبح إشارات HER2 الرئيسية. حافظ هذا التنشيط على مسار بقاء مهم يُعرف باسم AKT–mTOR. أدى إسكات AXL بأدوات جينية أو حظره بأدوية تجريبية إلى جعل الخلايا السرطانية أكثر حساسية بشكل ملحوظ تجاه عدة مثبطات HER2، مما أدى إلى تباطؤ نمو الخلايا ومزيد من موتها في الأطباق المخبرية.
كيف توصل البروتينات المساعدة طريق الهروب
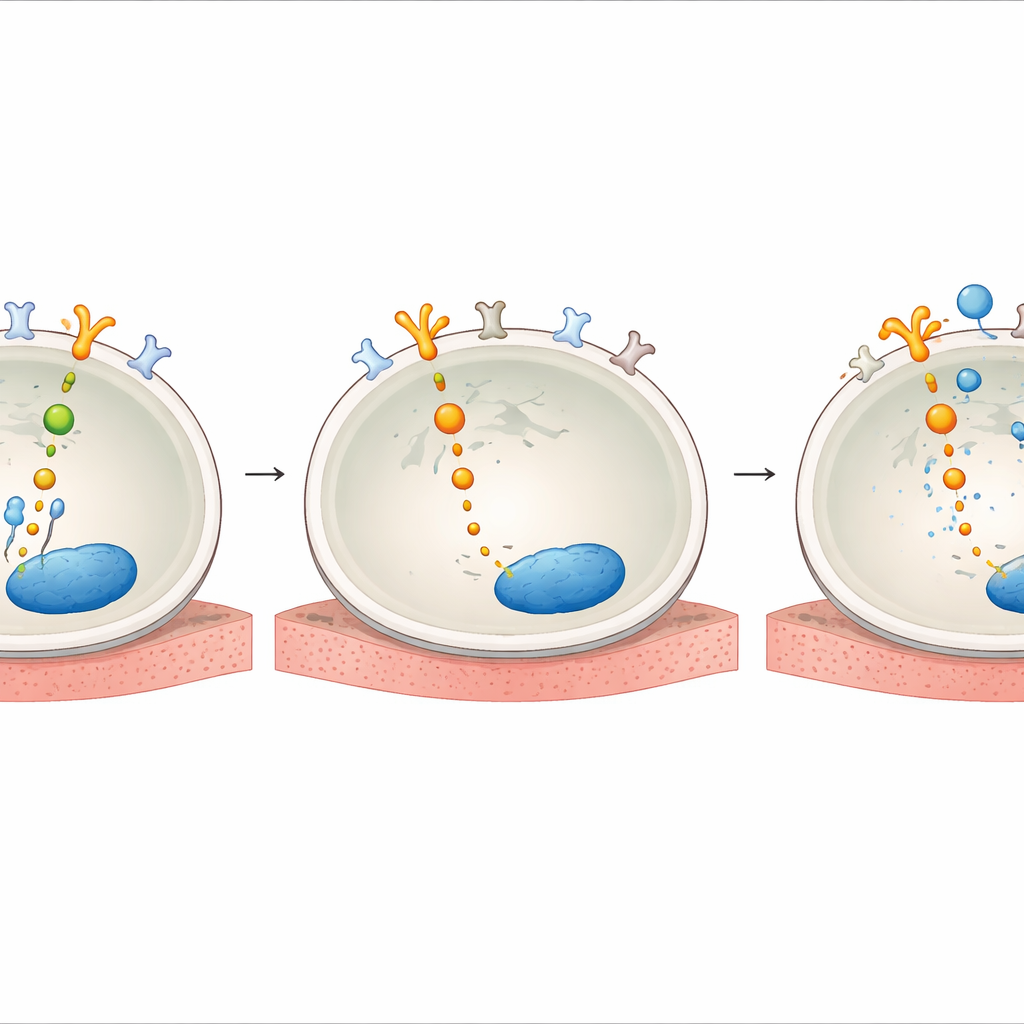
ثم تحقق الفريق في كيفية اكتساب AXL هذه الأهمية تحت ضغط الدواء. وجدوا أن المعالجة بمثبطات HER2 زادت مستويات GAS6، الجزيء الشريك الطبيعي الذي يفعل AXL على سطح الخلية. كما أظهروا أنه بعد التعرض للدواء، ارتبط AXL ماديًا بـ HER2 وذويها EGFR وHER3، مستغلاً فعليًا نفس دوائر البقاء التي يتحكم بها HER2 عادة. داخل الخلية، عملت بروتينات ماصة تُدعى SHC1 وSHCBP1 كموزعات توصيل. عندما تم حجب HER2، انفصل SHC1 عن SHCBP1 وربط بدلاً من ذلك بـ AXL، بينما انتقل SHCBP1 إلى النواة حيث ساعد في دفع تقدم دورة الخلية. أدى تثبيط SHC1 أو SHCBP1 إلى إضعاف إشارة AKT وتقليل بقاء الخلايا، كاشفًا عن محور AXL–SHC1–SHCBP1 الذي يدعم النمو عند تثبيط HER2.
إيقاف الخلايا المتحملة للدواء قبل أن تسيطر
لمحاكاة ما يحدث في المرضى، سمح العلماء للخلايا السرطانية بالنمو لأيام في وجود موبوسيرتينيب، مختارين مجموعة صغيرة تحمّلت الدواء. نمت هذه الخلايا المتحملة ببطء لكنها كانت أقل حساسية بوضوح للمثبّت الموجَّه لـ HER2 من الخلايا الأصلية. ظل بقاؤها يعتمد بدرجة كبيرة على AXL: إضافة حاجز لـ AXL قلّص نموها بشدة وخفّض نشاط AKT. في نماذج فئران تحمل أورام رئوية معدلة HER2 وموجبة لـ AXL، أدى الجمع بين موبوسيرتينيب ومثبط AXL إلى تقلّص الأورام أكثر، وتقليل الخلايا المنقسمة، وزيادة علامات الموت المبرمج مقارنةً بدواء HER2 وحده—دون سمية مضافة. كانت الأورام المصممة لإنتاج AXL بكميات زائدة أقل استجابة لموبوسيرتينيب بمفرده، لكنها استجابت مجدداً عند إضافة مثبط AXL.
ماذا قد يعني هذا للعلاج المستقبلي
من المهم أن عينات الأنسجة من مرضى سرطانات الرئة والمعدة ذات تغيرات HER2 أظهرت أن نحو ربعها كان لديه مستويات عالية من AXL، وكانت معظم العينات لديها على الأقل بعض وجود لـ AXL. يشير هذا إلى أن مجموعة كبيرة من المرضى قد تستفيد من استراتيجية علاج تجمع بين مثبط تيروسين كيناز موجه لـ HER2 ومثبط AXL من اليوم الأول، بدلاً من الانتظار لظهور المقاومة. بعبارات بسيطة، تُظهر الدراسة أن العديد من الأورام المحركة بواسطة HER2 تحتفظ بمفتاح نمو احتياطي—AXL—جاهزًا. عندما يُحجب HER2، يتولى AXL المهمة ويبقي الخلايا السرطانية على قيد الحياة. إيقاف المفتاحين معًا يؤدي إلى موت عدد أكبر بكثير من الخلايا السرطانية ويبطئ أو يمنع ظهور الناجين المتحملين للدواء. إذا أكدت التجارب السريرية ذلك، فقد تؤدي هذه المقاربة المزدوجة إلى تحكم أطول أمداً في سرطانات الرئة والمعدة ذات تغيرات HER2.
الاستشهاد: Ishida, M., Yamada, T., Katayama, Y. et al. AXL–SHC1 signaling axis mediates adaptive resistance to HER2-targeted tyrosine kinase inhibitors in HER2-aberrant lung and gastric cancers. npj Precis. Onc. 10, 142 (2026). https://doi.org/10.1038/s41698-026-01385-2
الكلمات المفتاحية: علاج موجه ضد HER2, مثبط AXL, مقاومة للأدوية, سرطان الرئة, سرطان المعدة