Clear Sky Science · ar
التحليل الكمي لنسيج وبلازما HER2 يتنبأ بنشاط تراستوزوماب ديروكسيتكان لسرطان الثدي
لماذا تهم هذه الدراسة المرضى
بالنسبة للأشخاص المصابين بسرطان الثدي النقيلي، يمكن أن تجلب الأدوية الجديدة أملاً — لكنها لا تعمل بنفس الفاعلية لدى الجميع. تطرح هذه الدراسة سؤالاً عملياً: هل يمكننا التنبؤ بشكل أفضل بمن سيستفيد أكثر ولمدة أطول من دواء مستهدف مستخدم على نطاق واسع يُدعى تراستوزوماب ديروكسيتكان (غالباً ما يُختصر إلى T-DXd)؟ من خلال فحص أدق وأكثر دقة لعينيات الورم والدم، يُظهر الباحثون أن القياس الدقيق لجزيء يُسمى HER2 — وكذلك بعض مؤشرات الحمض النووي والبروتين — يمكن أن يكشف أي الأورام هي الأكثر احتمالاً للاستجابة لهذا العلاج.
دواء مستهدف بنتائج متفاوتة
يعد T-DXd «مرتبطاً بين جسم مضاد ودواء»، وهو نوع من القذائف الموجهة التي تستهدف الخلايا التي تعرض بروتين HER2 وتوصِل حمولة شبيهة بالعلاج الكيميائي بداخلها مباشرة. استُخدم في الأصل للأورام ذات مستويات HER2 العالية جداً، وأصبح الآن معتمداً لما يقرب من تسعة من كل عشرة مرضى مصابين بسرطان الثدي النقيلي، بما في ذلك الأشخاص الذين يظهر لديهم HER2 بمستويات منخفضة أو حتى غير موجودة بحسب الاختبارات القياسية. ومع ذلك، في الممارسة اليومية، يستمتع بعض المرضى بفترات طويلة من السيطرة على المرض باستخدام T-DXd، بينما يتقدم سرطان آخرين بعد بضعة أشهر فقط. لقد فشلت الطرق المخبرية التقليدية، التي تصنف الأورام إلى إيجابية HER2 أو منخفضة HER2 أو صفر HER2، في تفسير هذه الاختلافات بشكل جيد.
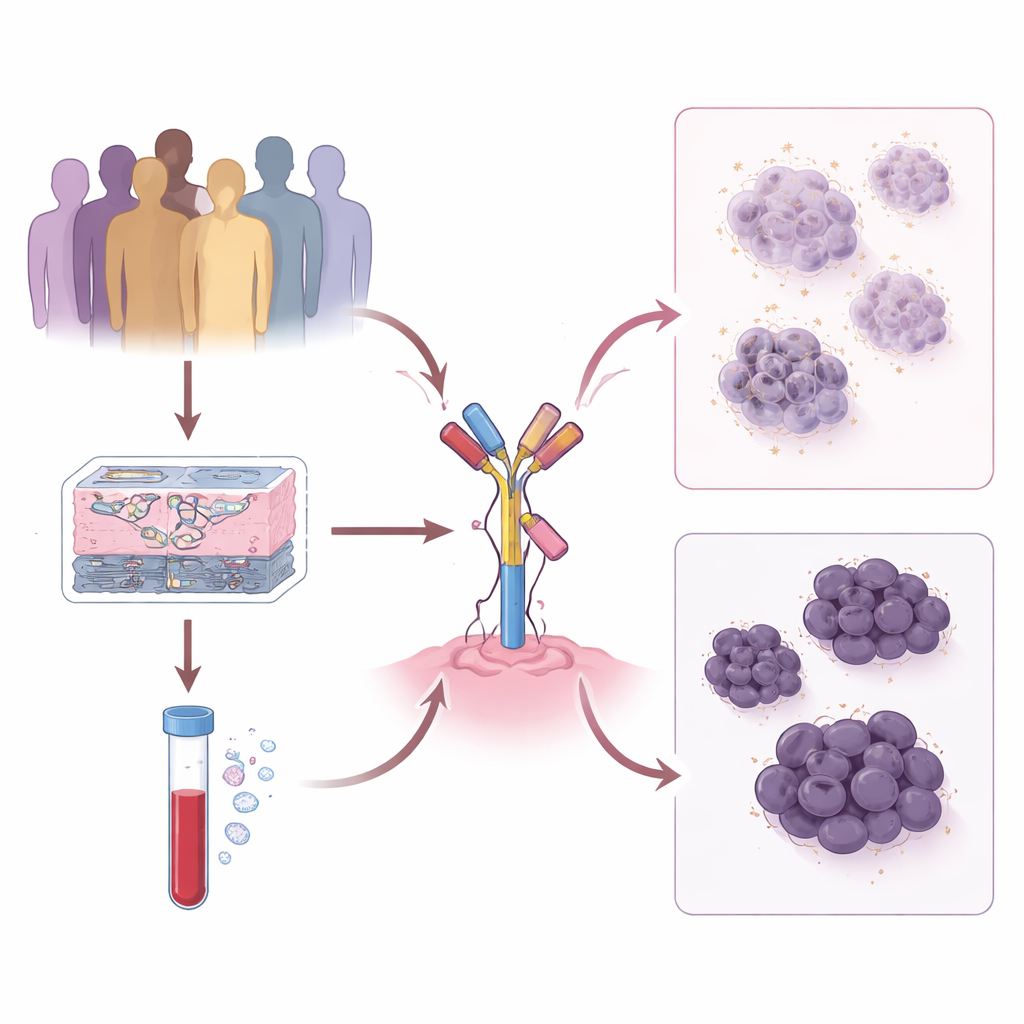
متابعة التغيرات في الورم مع مرور الوقت
فحص الفريق 191 مريضاً عولجوا بـ T-DXd في مركزين كبيرين للسرطان في الولايات المتحدة، وراجعوا كيف تصرفت أورامهم وكيف تغيرت مستويات HER2 من الورم الأصلي إلى النقائل اللاحقة. وجدوا أن تصنيف الورم لمرة واحدة على أنه منخفض HER2 أو صفر HER2 تفوّت ديناميكيات مهمة. عاش المرضى الذين ظلت أورامهم واضحة الإيجابية لـ HER2 أطول فترة على T-DXd، تلاهم أولئك الذين أظهرت أورامهم مستويات HER2 منخفضة لكن مستقرة. في المقابل، عندما تقلب HER2 بين منخفض وصفر مع مرور الوقت، كان الاستفادة من T-DXd أقصر بشكل ملحوظ. تشير هذه الأنماط إلى أنه كلما اعتمد الورم على HER2 بثبات أكبر، كانت قدرة هذا الدواء على العمل أفضل.
قياس HER2 بمقياس أدق
للانتقال أبعد من الفئات الخشنة، طبق الباحثون مجموعة من الاختبارات الحديثة على نسيج الورم. استخدم أحدها التألق المناعي الكمي لحساب بروتين HER2 بدقة؛ واستخدم آخر مصفوفة بروتينات عالية الإنتاجية؛ وقرأ ثالث نشاطات الجينات المتعلقة بمنطقة HER2 في الجينوم. عبر هذه الطرق الثلاث، كانت النتيجة متسقة: مستويات HER2 الكمية الأعلى — سواء قِيست كبروتين على سطح الخلية، أو في الأشكال المنشّطة (المفسفرة)، أو كحمض ريبونوئي الرسول — ارتبطت بزمن أطول حتى الخضوع للعلاج التالي وببقاء عام أفضل على T-DXd. وفي نفس المرضى، لم تميز قراءة علم الأمراض الاعتيادية (إيجابي HER2، منخفض، أو صفر) النتائج إلا بصعوبة، مما يؤكد أن "كمية" HER2 الموجودة أهم من الصندوق الذي يتم وضعها فيه.
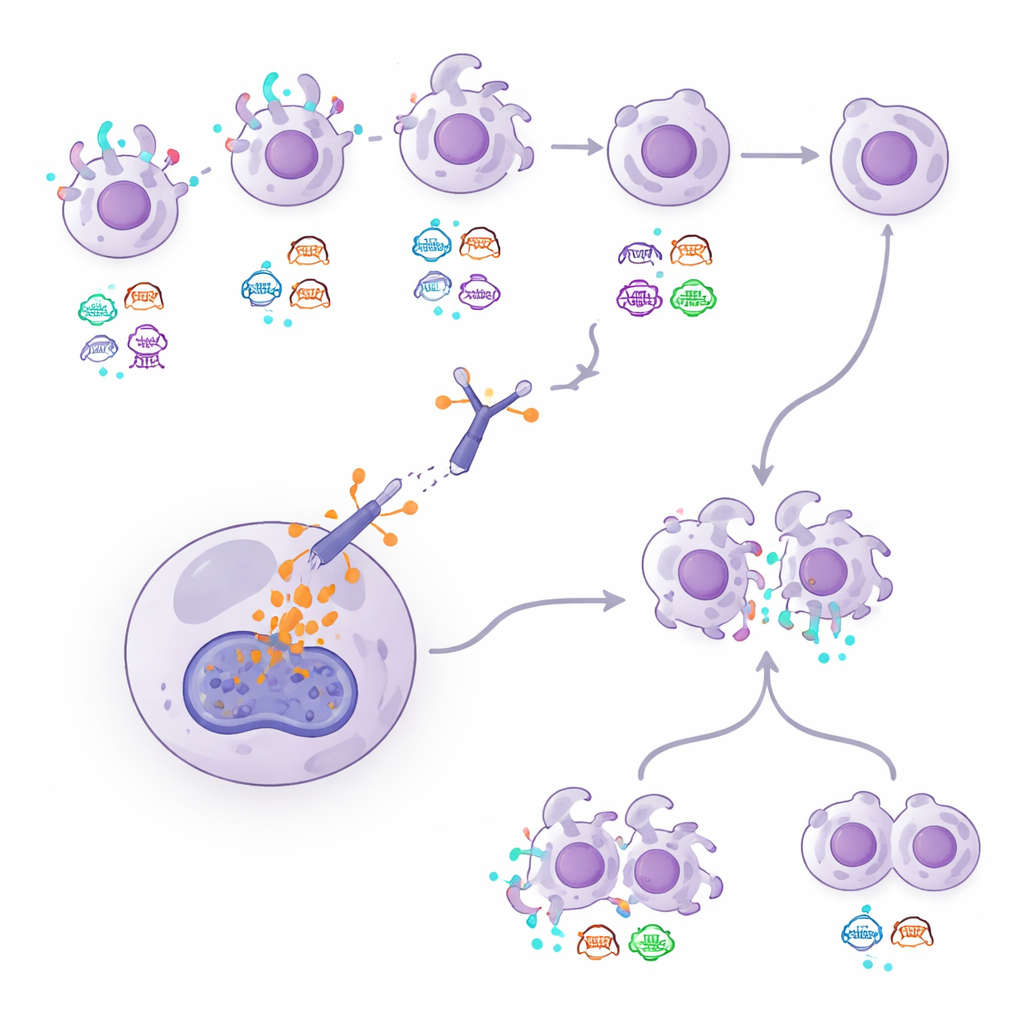
مؤشرات من اختبارات الدم وعلامات ورمية أخرى
لأن الخزعات المتكررة قد تكون غازية، اختبرت الدراسة أيضاً نهجاً معتمداً على الدم يحلل شظايا من الحمض النووي الورمي الطافية في مجرى الدم. باستخدام طريقة تُسمى DNADX، جمع الباحثون عينات دم المرضى إلى مجموعات بيولوجية وحسبوا توقيعاً وراثياً متعلقاً بـ HER2. أظهر المرضى الذين بدا أن دمهم يحمل إشارات HER2 أقوى ميلاً للبقاء على T-DXd لفترة أطول، بينما كان أولئك الذين أظهرت أنماط الحمض النووي لديهم سمات مرتبطة بمرض أكثر عدوانية ونمواً سريعاً أسوأ حظاً. لاحظ الباحثون أيضاً أن في الأورام المصنفة سلبياً لـ HER2، ارتبطت المستويات العالية لبروتين يسمى توبويزوميراز 1 داخل الخلايا الورمية بنتائج أسوأ، مما يوحي بأن طريقة تعامل الخلية مع حمولة الدواء قد تؤثر على النجاح. برزت خسارات أو طفرات جينية معينة، مثل التغيرات في جينات ERBB2 وTP53 وزيادة حدوث طفرات ARID1B بعد العلاج، كدلائل محتملة للمقاومة.
ماذا يعني هذا للمرضى والأطباء
بشكل عام، تُظهر الدراسة أن T-DXd علاج فعال في العالم الواقعي، خاصة للمرضى الذين تقود أورامهم HER2 بقوة وباستقرار. لكنها توضح أيضاً أن اختبار HER2 التقليدي أداة خشنة إلى حد لا يسمح بتوجيه هذا الدواء القوي بدقة. من خلال استخدام قياسات أكثر حساسية على النسيج والدم، قد يتمكن الأطباء في نهاية المطاف من تحديد المرضى الأكثر احتمالاً للاستفادة من T-DXd، وتوفير التعرض للعلاج غير الفعال عن غيرهم، والتخطيط بشكل أفضل لترتيب استخدام المرتبطات بين الأجسام المضادة والسموم المختلفة. وبينما هذه الاختبارات المتقدمة لم تصبح روتينية بعد وتحتاج إلى تحقق في مجموعات أكبر، فإنها تشير إلى مستقبل تُفصَّل فيه قرارات العلاج لسرطان الثدي النقيلي باستخدام صور جزيئية مفصلة، لا مجرد تسميات عامة.
الاستشهاد: Tarantino, P., Kim, SE., Hughes, M.E. et al. Quantitative HER2 tissue and plasma profiling predicts the activity of trastuzumab deruxtecan for breast cancer. npj Precis. Onc. 10, 141 (2026). https://doi.org/10.1038/s41698-026-01365-6
الكلمات المفتاحية: اختبار HER2, تراستوزوماب ديروكسيتكان, سرطان الثدي النقيلي, خزعة سائلة, المرتبطات بين الأجسام المضادة والسموم