Clear Sky Science · ar
استجابة الميدوستاورين في اللوكيميا النخاعية الحادة تتشكل بواسطة حالة خلوية شبيهة بالخلايا السلفية تستهدفها محاكيات SMAC انتقائياً
لماذا تتوقف بعض أدوية اللوكيميا عن العمل
بالنسبة لكثير من الأشخاص المصابين بنوع من سرطانات الدم يُسمى اللوكيميا النخاعية الحادة (AML)، جلبت الأدوية الموجهة الجديدة أملاً — لكن ليس الجميع يستفيدون، وغالباً ما تتضاءل الاستجابة مع الوقت. تطرح هذه الدراسة سؤالاً بسيطاً لكن حاسماً: لماذا تتجاهل بعض خلايا اللوكيميا دواءً واسع الاستخدام مثل الميدوستاورين، وهل يمكننا إيجاد تركيبة ذكية تجبر هذه الخلايا العنيدة على الموت؟
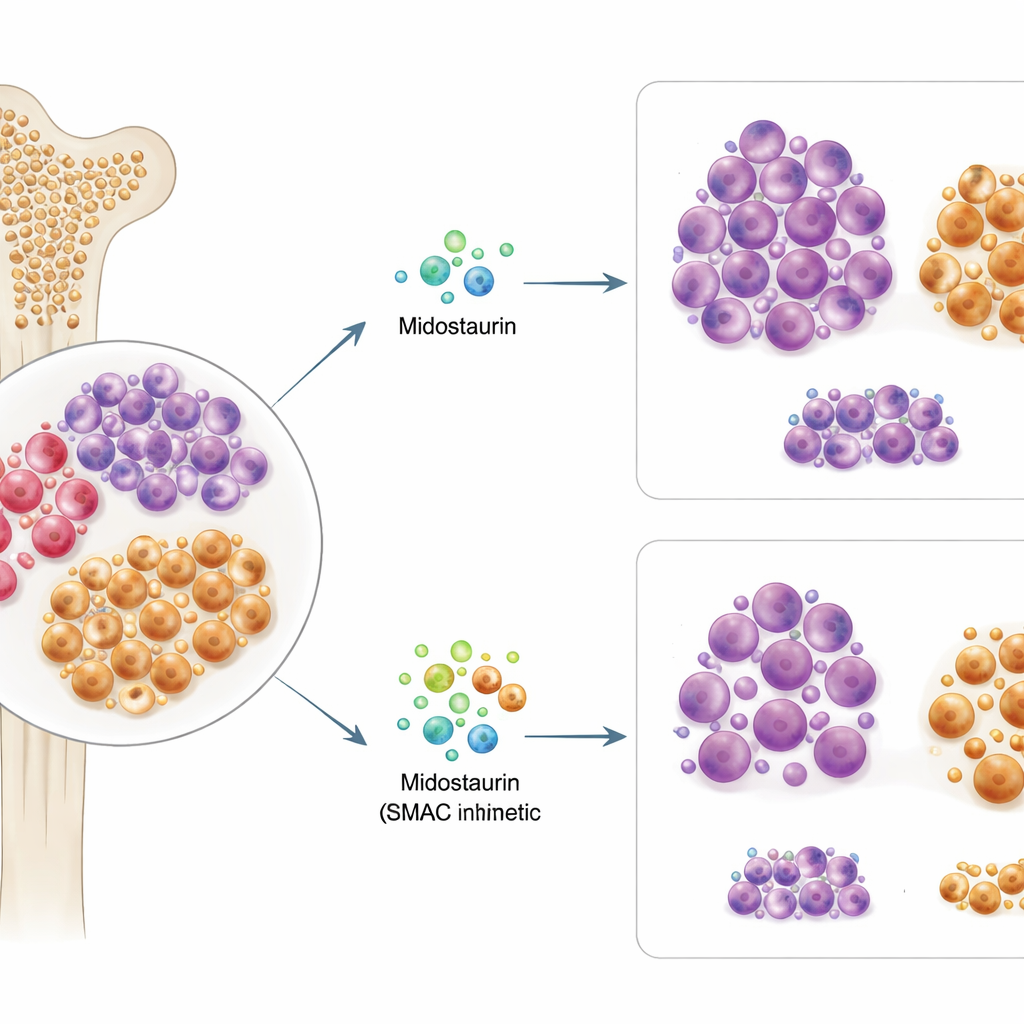
التطلع أبعد من الطفرة الرئيسية
حوالي مريض واحد من كل ثلاثة من مرضى AML يحمل تغيراً في جين يُدعى FLT3، وهو ما يدفع نمو اللوكيميا ويُعد سبب وصف الميدوستاورين. اختبر الباحثون عينات من نخاع العظم والدم من 63 مريضاً مصاباً بAML مع طفرات FLT3، وعرضوا الخلايا للميدوستاورين وأكثر من 500 دواء سرطان آخر في المختبر. وجدوا أن حساسية خلايا المريض للميدوستاورين خارج الجسم الحي طابقت عن كثب كيف استجاب ذلك المريض لاحقاً في العيادة. ومن المدهش أن نوع طفرة FLT3 بدقة أو مدى وفرتها لم يتنبأا بشكل موثوق بنجاح الميدوستاورين، ما يشير إلى أن الجينات وحدها لا تفسر من سيستفيد.
مجموعة خفية من "الخلايا البذرية" العنيدة
بالتعمق أكثر، قارن الفريق أنماط البروتين والتعبير الجيني بين الخلايا الحساسة للميدوستاورين وتلك غير المستجيبة. كانت العينات غير المستجيبة غنية بسمات خلايا سلفية غير ناضجة تشبه الجذور — خلايا أقرب إلى أصل تكوين الدم ويُعتقد أنها تعمل كـ "بذور" قادرة على إعادة تشغيل اللوكيميا. بالمقابل، بدت العينات المستجيبة أقرب إلى خلايا مناعية وميالوية جزئياً متمايزة. باستخدام طرق متقدمة على مستوى الخلية الواحدة، حدد العلماء مجموعة محددة من خلايا اللوكيميا التي تميَّزت ببروتينات سطحية CD38 وCD45RA والتي تصرفت مثل هذه الخلايا السلفية. أظهرت هذه الخلايا تنظيماً غير عادي لغشائها الخارجي، مما يوحي بأن جزيئات إشارات رئيسية مرتبة بطريقة تفضّل البقاء.
أسلاك البقاء: تبديل في مسارات الإشارة
صُمّم الميدوستاورين لوقف إشارة FLT3، التي عادة ما تغذي سلسلة إشارات تشمل جزيئاً يسمى STAT5 ويمكن أن يحفز نمو الخلايا. عندما فحص الفريق الإشارة في خطوط خلوية وعينات مرضى بعد علاج الميدوستاورين، لاحظوا نمطين مميزين. في الخلايا الحساسة للميدوستاورين، انخفض نشاط STAT5 بسرعة، بما يتفق مع إيقاف فعّال لـ FLT3. أما في الخلايا المقاومة، فقد هيمن مسار آخر: PI3K/AKT، وهو مسار بقاء كلاسيكي يساعد الخلايا على مقاومة الموت. حافظت هذه الخلايا المقاومة أو زادت من نشاط AKT بعد العلاج، وأظهرت مستويات أعلى من البروتينات التي تمنع الاستماتة (موت الخلايا المبرمج). بعبارة أخرى، بدا أن الأسلاك الداخلية في هذه الخلايا الشبيهة بالسلفية قد أعيد توجيهها لتفضيل البقاء حتى عندما يتم تثبيط FLT3.
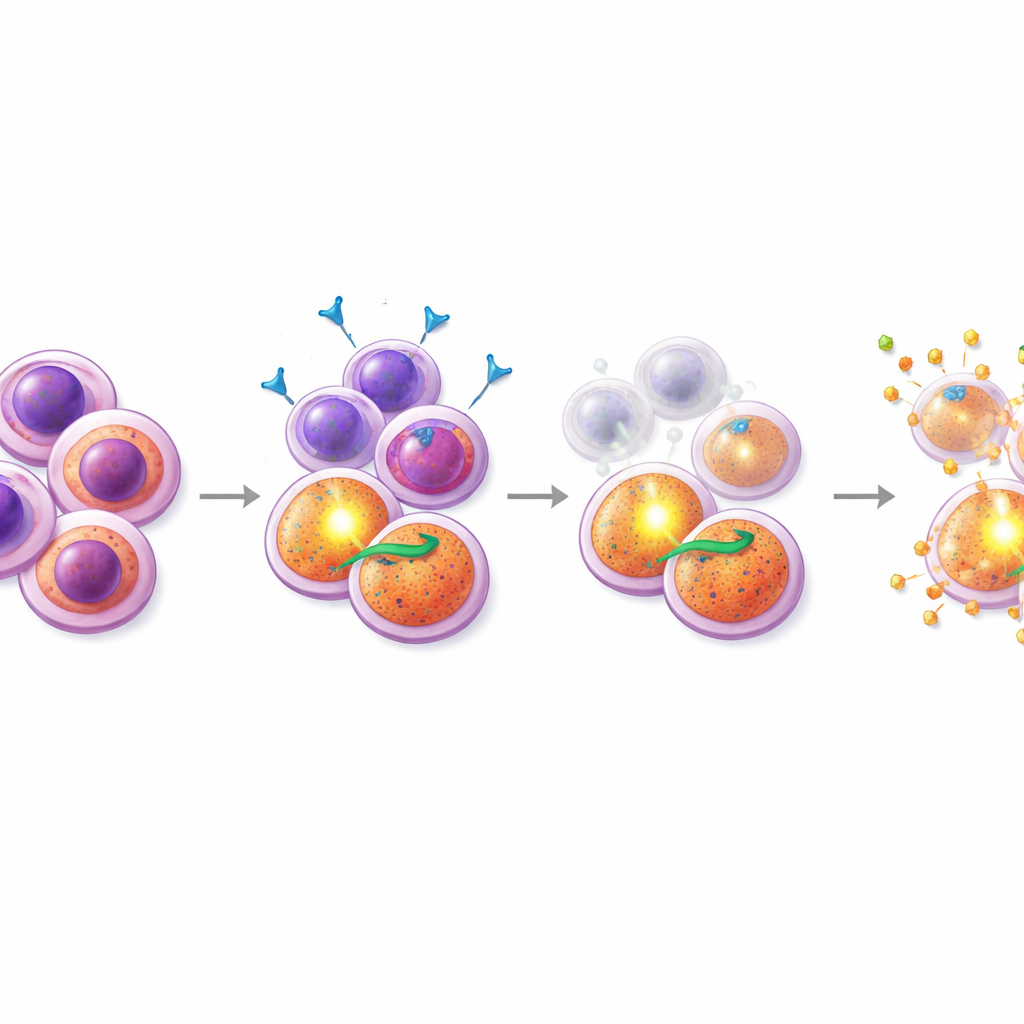
إيجاد دواء شريك يصيب النقطة الضعيفة
مسلحين بهذا الفهم، فحص الباحثون تراكيب الميدوستاورين مع مئات المركبات الأخرى، مع التركيز على الأدوية التي تؤثر على موت الخلايا. كانت إحدى المجموعات البارزة هي محاكيات SMAC، أدوية تعطل بروتينات "مثبطة الاستماتة" التي تعتمد عليها الخلايا المدفوعة بـ PI3K/AKT. في عينات مرضى مقاومة وفي خط خلوي مقاوم يحمل طفرة FLT3، أدى إضافة محاكيات SMAC مثل البيرينابانت إلى الميدوستاورين إلى تآزر قوي: معاً، قتلت الأدوية عدداً أكبر بكثير من الخلايا مقارنة بكل منهما على حدة. والأهم من ذلك، أظهرت تجارب قياس الخلايا المتقدمة أن تركيبة الميدوستاورين–محاكي SMAC استنزفت انتقائياً مجموعة الخلايا الشبيهة بالسلفية CD38+CD45RA+ وخفضت مستويات علامات السطح المميزة لها، مما يشير إلى أن هذا العلاج يستهدف خصيصاً البذور الأصعب على القتل. بالمقابل، كانت التراكيب مع مثبط BCL-2 المعتمد في العيادة فينتوكلاكس أكثر فعالية ضد مجموعة مختلفة عالية CD34 ولم تُظهر نفس التأثير المركَّز على الخلايا المقاومة.
ماذا يعني ذلك للمرضى
تشير هذه الدراسة إلى أن المقاومة للميدوستاورين ليست مسألة طفرة FLT3 وحدها، بل تتعلق أيضاً "بحالة" خلايا اللوكيميا — مستوى نضجها، تنظيم غشائها، ومسارات البقاء المفضلة لديها. يبدو أن مجموعة شبيهة بالسلفية CD38+CD45RA+ تعد مخزناً رئيسياً للمقاومة، حيث تحول إشاراتها من مسار STAT5 الاعتيادي نحو برنامج بقاء ملائم PI3K/AKT. من خلال إقران الميدوستاورين بمحاكيات SMAC، تمكن الباحثون من إعادة تحسس هذه الخلايا ودفعها نحو الموت الخلوي في المختبر. ومع أن هناك حاجة لدراسات سريرية أكبر، تشير النتائج إلى مستقبل قد يستخدم فيه الأطباء اختبارات وظيفية وتوصيف حالة الخلايا، وليس مجرد تسلسل الحمض النووي، لاختيار تراكيب موجهة ضد FLT3 تقطع كل من اللوكيميا الشاملة وبذورها الأكثر صموداً.
الاستشهاد: Struyf, N., Gezelius, H., Lundmark, A. et al. Midostaurin response in AML is shaped by a progenitor-like cell state selectively targeted by SMAC mimetics. npj Precis. Onc. 10, 117 (2026). https://doi.org/10.1038/s41698-026-01363-8
الكلمات المفتاحية: اللوكيميا النخاعية الحادة, مثبطات FLT3, مقاومة الدواء, الخلايا الجذعية اللوكيمية, محاكيات SMAC