Clear Sky Science · ar
الخلايا الليفية المرتبطة بالسرطان ذات مستوى COL3A1 العالي تنظم البيئات الأيضية والمناعية لتمنح مقاومة للعلاج الكيميائي في سرطان الثدي
لماذا بعض أورام الثدي لا تتأثر بالعلاج الكيميائي
العلاج الكيميائي يمكن أن ينقذ الأرواح في حالات سرطان الثدي، ومع ذلك يكتشف العديد من المرضى أن أورامهم تتوقف عن الاستجابة أو لم تستجب جيدًا منذ البداية. تبتعد هذه الدراسة عن خلايا السرطان نفسها لتفحص الحي الذي تعيش فيه وتسأل: أي الخلايا المجاورة تساعد الأورام على البقاء أثناء العلاج، وكيف تفعل ذلك؟ الجواب يتمحور حول مجموعة خاصة من خلايا الدعم التي تعيد برمجة تغذية الورم والمناعة المحلية لتعمل كدرع يحمي خلايا السرطان من العلاج الكيميائي.
المساعدون الخفيون حول الورم
أورام الثدي ليست مجرد خلايا سرطانية؛ إنها مجتمعات مختلطة تضم أوعية دموية وخلايا مناعية وخلايا نسيجية ربطية تُسمى خلايا ليفية. عندما تعيش الخلايا الليفية داخل الورم تُعرف بخلايا ليفية مرتبطة بالسرطان (CAFs)، ويمكن لها أن تكبح السرطان أو تعززه. من خلال دمج عدة طرق قوية لتصنيف الجينات على عينات المرضى—تحليل خلية واحدة، مكاني، وجماعي—إلى جانب تجارب مخبرية وحيوانية، حدّد الباحثون شُعبة من الخلايا الليفية التي تُعبر بكثرة عن جزيء يُدعى COL3A1، وهو مكوّن من السقالة النسيجية. المرضى الذين احتوت أورامهم على مزيد من هذه الخلايا الليفية ذات مستوى COL3A1 العالي كانوا أكثر عرضة لردود فعل ضعيفة للعلاج الكيميائي ولحظوظ بقاء أسوأ.
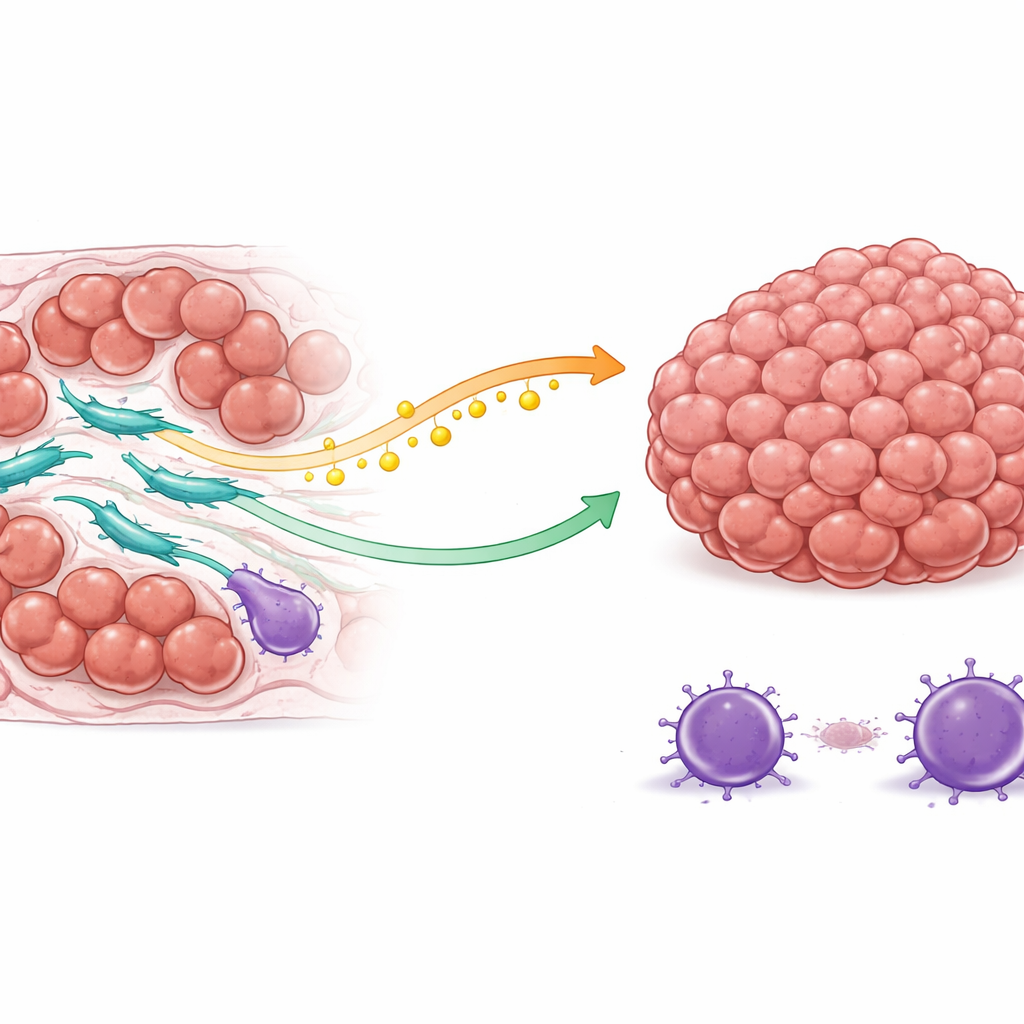
درع ذو شُقين: وقود وحماية
اكتشف الفريق أن خلايا COL3A1 العالية تحمي خلايا السرطان بطريقتين رئيسيتين. أولًا، تغيّر طريقة تعاملها مع الدهون. هذه الخلايا الليفية تزيد نشاط إنزيم يصنع حمض الأوليك، وهو نوع من الدهون. بدلًا من الاحتفاظ بهذا الوقود، تُطلقه إلى محيط الورم. تلتقط خلايا السرطان حمض الأوليك عبر بروتين سطحي، وتستجيب بتشغيل مسار داخلي للبقاء معروف بمساعدة الخلايا على مقاومة إشارات الموت. نتيجة لذلك، عندما يحاول العلاج الكيميائي تحفيز برامج الانتحار الخلوي في خلايا السرطان، تكون تلك الخلايا مجهزة بشكل أفضل للمقاومة والاستمرار في الانقسام.
تشكيل حي مناعي معادٍ
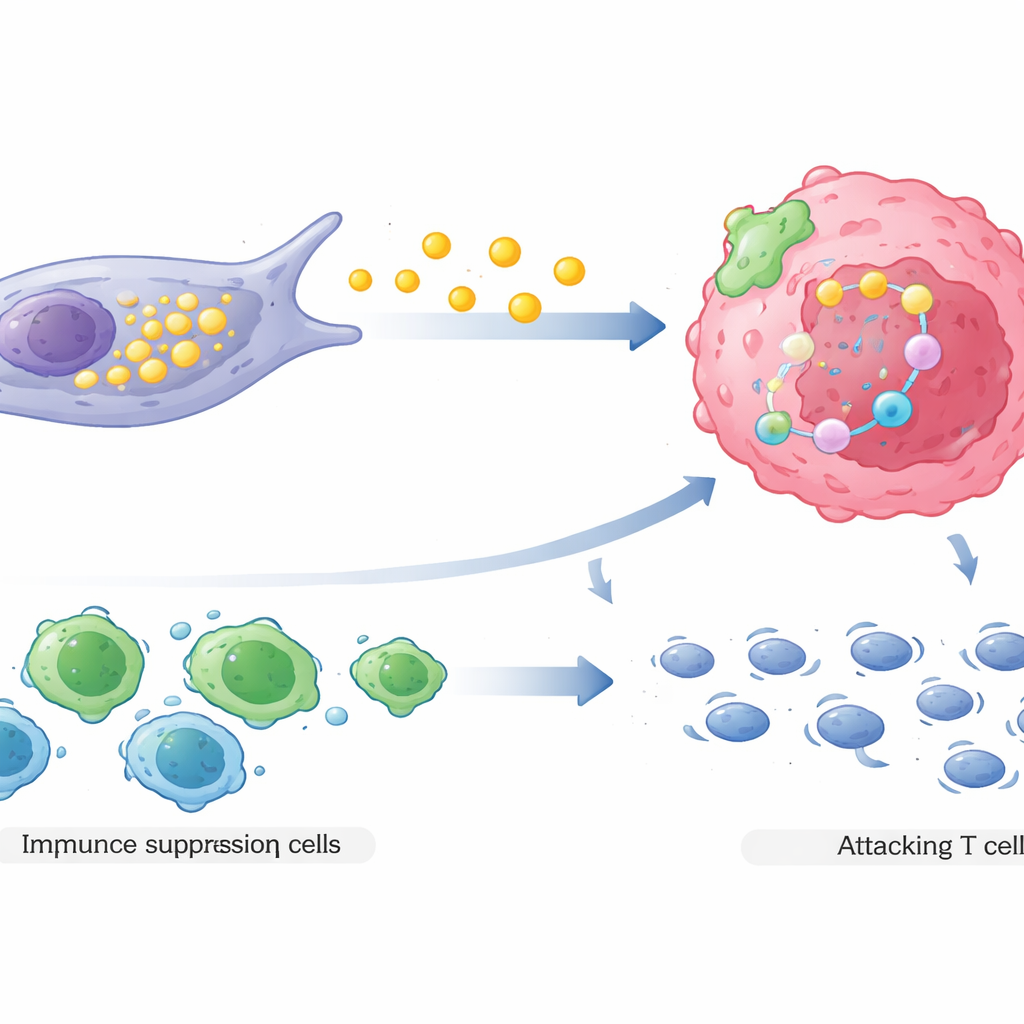
ثانيًا، تعيد خلايا COL3A1 العالية تشكيل المشهد المناعي المحلي لصالح الورم. من خلال تفاعلات إشارية معقدة، تجذب هذه الخلايا الخلايا التائية المنظمة، وهي نوع من الخلايا المناعية التي تُخمد الهجمات المناعية، وفي الوقت نفسه تُثبط أو تُضعف الخلايا التائية القاتلة التي كانت ستهاجم السرطان عادةً. أظهر التخطيط المكاني لأورام مرضى حقيقيين أن هذه الخلايا الليفية تميل إلى التمركز بالقرب من كلٍ من خلايا السرطان المقاومة للأدوية والخلايا المناعية القمعية، بينما تُبعد الخلايا التائية القاتلة الفعّالة إلى مسافات أبعد. يخلق هذا الترتيب منطقة محمية حيث تواجه خلايا السرطان تهديدات مناعية أقل بينما تصبح أصعب على القتل بالعقاقير.
دليل من الخلايا والفئران والمرضى
لاختبار السببية، قلّل الباحثون COL3A1 في الخلايا الليفية المزروعة في المختبر. عندما نمت خلايا سرطان الثدي إلى جانب هذه الخلايا الليفية المعدلة، شكلت هياكل غزوية أقل، كانت أكثر عرضة للقتل بالعقار الكيميائي باكليتاكسيل، وأظهرت المزيد من إشارات الموت المبرمج. في فئران تم زراعتها بمزائج من خلايا سرطان الثدي والخلايا الليفية، أدى حجب COL3A1 في الخلايا الليفية إلى تباطؤ نمو الورم أثناء العلاج الكيميائي وخفض مستويات إنزيم صنع الدهون والمستقبل الخلوي المرتبط بحمض الأوليك. في مجموعة مكونة من 72 مريضًا عولجوا بالعلاج الكيميائي قبل الجراحة، ارتبطت المستويات الأعلى من COL3A1 وشركائها في أيض الدهون بشدة مع استجابات علاجية أسوأ ووقت أقصر قبل تكرار السرطان.
ما يعنيه هذا للعلاج المستقبلي
ببساطة، تُظهر الدراسة أن مجموعة محددة من خلايا الدعم في أورام الثدي تعمل كوحدة حراسة: تزود خلايا السرطان بنظام غذائي قائم على الدهون يحميها وتستدعي حلفاء مناعيين يضعفون دفاعات الجسم. معًا تجعل هذه الإجراءات العلاج الكيميائي أقل فعالية. قياس وفرة الخلايا الليفية ذات مستوى COL3A1 العالي يُحسن قدرة الأطباء على التنبؤ بمن سيستجيب أو لن يستجب للعلاج، والمسارات التي تستخدمها—إنتاج الدهون، إشارات البقاء داخل خلايا السرطان، وتخميد المناعة—تقدم أهدافًا علاجية جديدة. في المستقبل، قد تُقرن علاجات تفكك أو تعيد برمجة هذه الخلايا الليفية مع العلاج الكيميائي القياسي لمنع الأورام من اكتساب المقاومة.
الاستشهاد: Jiang, P., Li, X., Wang, Z. et al. COL3A1high cancer-associated fibroblasts orchestrate metabolic and immune microenvironments to confer chemoresistance in breast cancer. npj Precis. Onc. 10, 139 (2026). https://doi.org/10.1038/s41698-026-01338-9
الكلمات المفتاحية: سرطان الثدي, مقاومة العلاج الكيميائي, البيئة الدقيقة للورم, الخلايا الليفية المرتبطة بالسرطان, استقلاب الدهون