Clear Sky Science · ar
التنبؤ بنقص إعادة التركيب المتماثل واستجابات العلاج باستخدام نموذج أساسي معتمد على التصوير المقطعي المحوسب: دراسة قبل سريرية
لماذا يهم هذا المرضى والأطباء
تستجيب بعض علاجات السرطان التي تتسبب في تلف الحمض النووي، مثل بعض أنواع العلاج الكيميائي والأدوية المستهدفة الحديثة، بشكل ملحوظ في الأورام التي تعاني مسبقًا من خلل في آليات الإصلاح. التحدي يكمن في معرفة أي الأورام تحمل هذه النقائص المستترّة دون الاعتماد على خزعات متكررة وغزوية. تبحث هذه الدراسة فيما إذا كانت فحوصات التصوير الروتينية على نمط الفحوصات الطبية في الفئران، عندما تُفسَّر بواسطة نموذج ذكاء اصطناعي قوي، قادرة على كشف مدى هشاشة الورم ومدى استجابته لدواء تجريبي جديد.
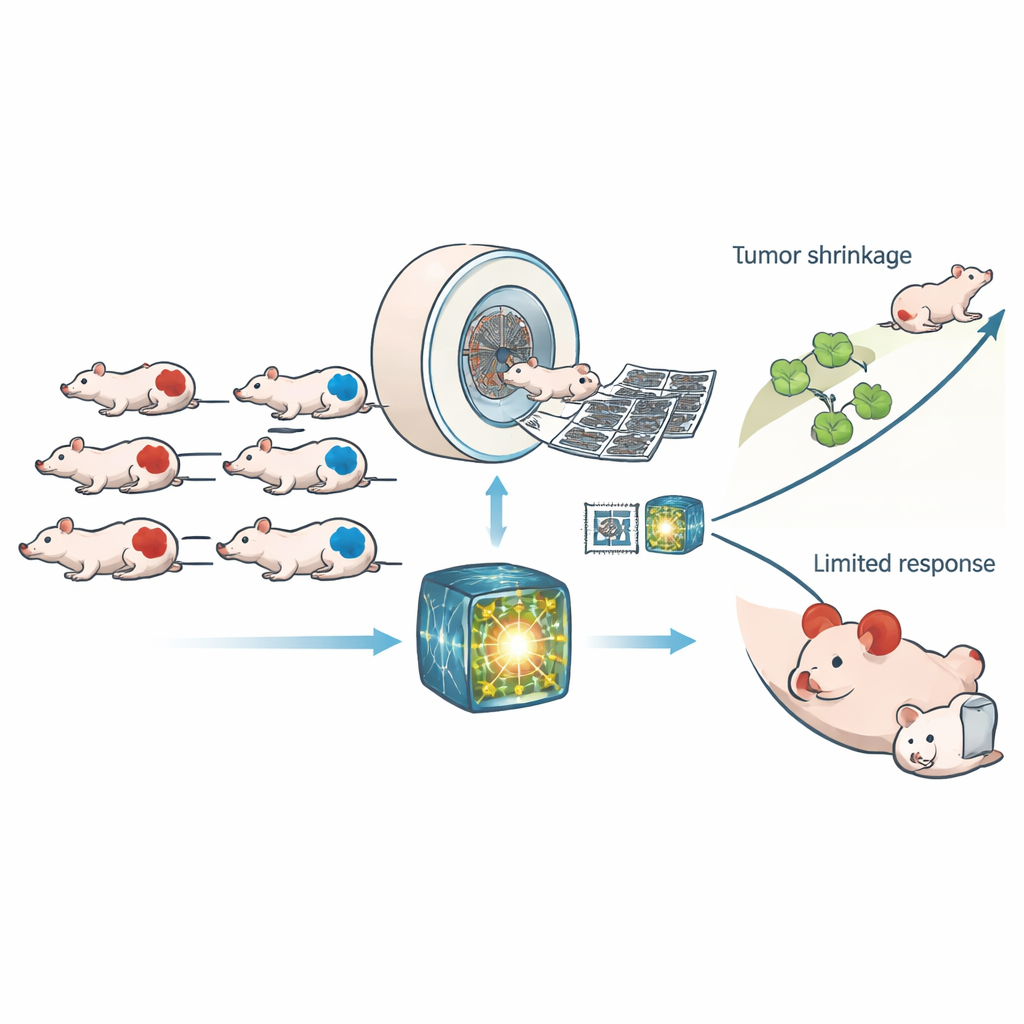
نقطة ضعف مستترة في خلايا السرطان
تحمل العديد من الأورام عيوبًا في مسار إصلاح رئيسي للحمض النووي يُسمى إعادة التركيب المتماثل. عندما يفشل هذا المسار، تتراكم الأضرار في المادة الوراثية للخلايا، وهي حالة تعرف بنقص إعادة التركيب المتماثل (HRD). قد يجعل HRD السرطانات أكثر عرضة للتكوّن، لكنه كذلك يتحول إلى نقطة ضعف: الأدوية التي تزيد من تلف الحمض النووي يمكن أن تدفع هذه الخلايا المجهدة بالفعل إلى الانهيار، مما يؤدي إلى موتها بشكل أكثر فعالية من الخلايا السليمة. حاليًا، يعتمد تحديد HRD عادةً على اختبارات جينية أو تحاليل مخبرية متخصصة مكلفة وتستغرق وقتًا وغالبًا ما تتطلب أخذ عينات من الورم. تساءل المؤلفون عما إذا كان التصوير—نفس نوع التصوير بالأشعة ثلاثية الأبعاد المستخدم على نطاق واسع في العيادات—يمكن أن يوفر نافذة سريعة وغير غازية إلى HRD.
استخدام فحوص ذكية بدلًا من المزيد من الخزعات
عمل الباحثون مع 307 فئران تحمل وزعات أورام بشرية كانت إما ناقصة في HRD أو طبيعية في قدرتها على الإصلاح. خضعت جميع الحيوانات لمسحات تصوير مقطعي محوسب (CT) عالية الدقة قبل وبعد تلقيها إما علاجًا ضابطًا أو CP‑506، وهو دواء تجريبي ينشط في مناطق منخفضة الأكسجين داخل الأورام ويكوّن وصلات متقاطعة في سلاسل الحمض النووي. بدلًا من الاعتماد على عدد قليل من قياسات الصورة المصممة يدويًا، استخدم الفريق «نموذجًا أساسيًا» حديثًا مدرَّبًا على مجموعات بيانات CT بشرية كبيرة لاستخراج آلاف الأنماط الدقيقة من كل مسح. ثم تم تدريب مصنّف بسيط على هذه الأنماط ليقرر ما إذا كان الورم يعاني HRD، وأُعيد استخدام نفس الميزات المتعلَّمة للتنبؤ بمدى تلف الحمض النووي وتأخر النمو الذي سيسببه CP‑506.
مدى أداء نموذج التصوير
تفوَّق النموذج الأساسي بوضوح على كل من الراديوميكس التقليدي وشبكة التعلم العميق القياسية التي دُربت من الصفر. على المسوح الاختبارية الجديدة، مَيّزَ بين أورام HRD وغير HRD بمساحة تحت المنحنى تقارب 0.88، وهي مستوى دقة ثبت عبر إعدادات طاقة CT المختلفة. عندما اتفقت الطريقتان المعتمِدتان على الذكاء الاصطناعي حول نوع الورم، ارتفع الأداء إلى مستوى أعلى. توافقت درجة HRD المستخرجة من الصورة مع الحالة الجينية الحقيقية في عدة خطوط أورام بروستاتية وسرطانات القولون والمستقيم، رغم أن أحد الخطوط ذات سلوك إصلاح غير المعتاد ظل أصعب في التصنيف. ومن المهم أن ميزات CT المرتبطة بـ HRD لم تكن مجرد تماثلات إحصائية: فقد تنبأت أيضًا بكمية تلف الحمض النووي الدائم التي أحدثها CP‑506 بعد 48 ساعة من العلاج وبالزمن اللازم لعودة نمو الأورام إلى أربعة أضعاف حجمها في تجربة موازية.
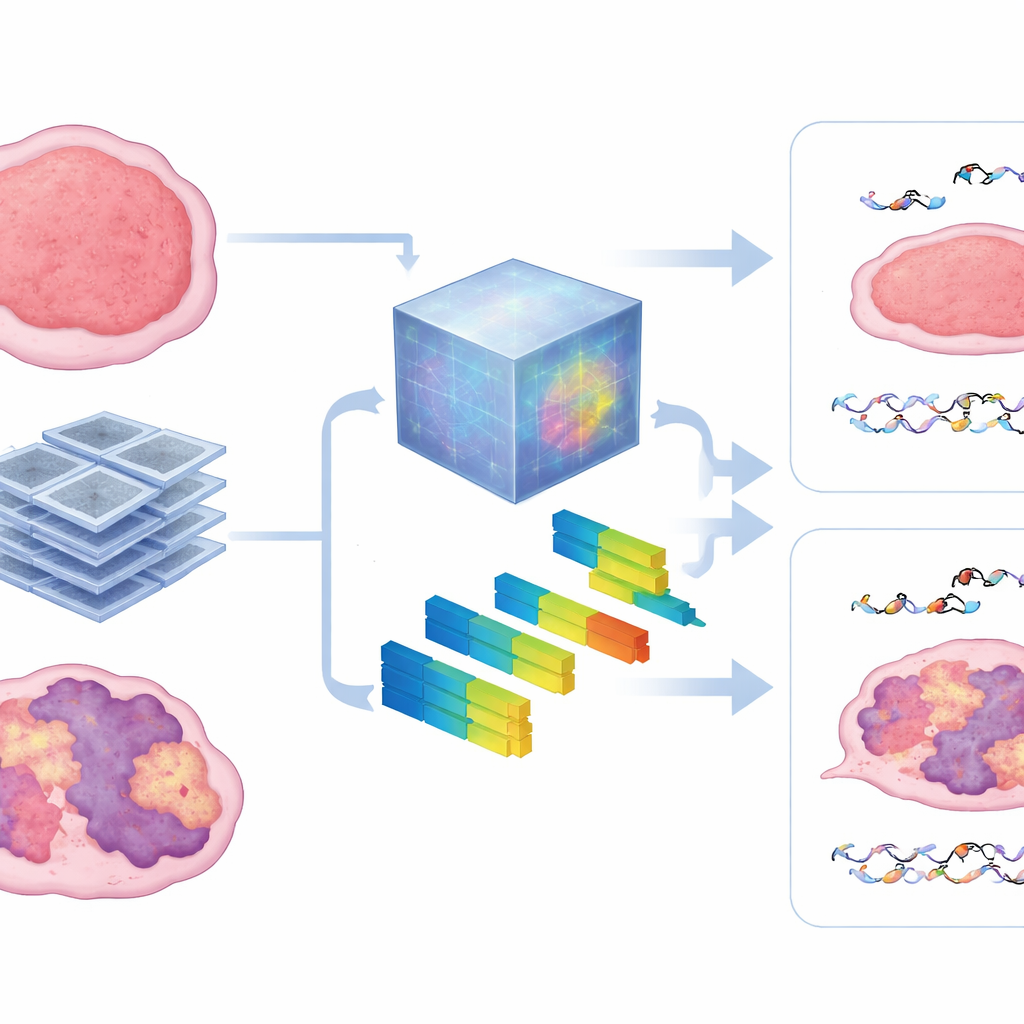
ما تكشفه المسوحات داخل الورم
لفتح نافذة على الصندوق الأسود، قارن المؤلفون الأنماط التي تعلَّمها النموذج الأساسي مع ميزات راديوميكس القياسية التي تصف نسيج الصورة وشدتها. وجدوا أن النموذج اعتمد بشكل كبير على مقاييس التغايرية—مدى تكتل، خشونة، أو عدم انتظام مظهر الورم على CT. كانت الأورام التي أظهرت توقيعات HRD أقوى تميل إلى إظهار نسيج أكثر فوضوية، وساعدت هذه الميزات نفسها في التنبؤ بكل من تلف الحمض النووي المجهرية والتحكم الظاهر في الورم. ظلت الطريقة متينة حتى عند توفر بيانات تدريب أقل، مما يشير إلى أن مثل هذه النماذج المدرَّبة مسبقًا يمكن أن تتجاوز عقبة رئيسية في الدراسات الحيوانية، حيث يصعب جمع مجموعات بيانات تصويرية كبيرة.
من تجارب الفئران إلى رعاية المرضى المستقبلية
تُظهر هذه الدراسة ما قبل السريرية أن مسح CT واحدًا، عندما يُفسَّر عبر ذكاء اصطناعي قوي ومدرَّب مسبقًا، يمكنه التقاط إشارات لخلل إصلاح الحمض النووي والتنبؤ بمدى استجابة الورم لدواء يسبب تلفًا في الحمض النووي. بالنسبة للقارئ العادي، الخلاصة أن المسوحات القياسية قد تقوم قريبًا بوظيفتين—تحديد موضع الورم وكشف هشاشته—دون إجراءات إضافية. قبل أن يصبح هذا جزءًا من الرعاية الروتينية، يجب اختبار الطريقة والتحقق من صلاحيتها في المرضى البشر. إذا نجحت تلك الجهود، فقد تساعد بصمات CT المدعومة بالذكاء الاصطناعي لنقص HRD الأطباء على توفيق العلاجات مثل CP‑506 والعلاجات المماثلة للمرضى بدقة أكبر، مما يُحسّن النتائج ويجنِّب آخرين أدوية سامة وغير فعالة.
الاستشهاد: Kuang, S., Schuitmaker, L., Wu, M. et al. Predicting homologous recombination deficiency and treatment responses using a computed tomography-based foundation model: a preclinical study. npj Precis. Onc. 10, 121 (2026). https://doi.org/10.1038/s41698-026-01322-3
الكلمات المفتاحية: نقص إعادة التركيب المتماثل, تصوير السرطان, الراديوميكس, النماذج الأساسية, العلاج المسبب لضرر في الحمض النووي