Clear Sky Science · ar
تعميم الفصل الآلي للأورام في صور الشرائح المَسلَحة المجسّمة عبر أنواع متعددة من السرطان
لماذا هذا مهم لعلاج السرطان
لا يزال تشخيص السرطان يعتمد على فحص الخبراء الدقيق لشرائح الزجاج النسيجية المصبوغة تحت المجهر — وهي مهمة تستغرق وقتًا وتزداد صعوبة مع تزايد أعداد الحالات ونقص أطباء الباثولوجيا. تطرح هذه الدراسة سؤالًا بسيطًا لكنه قوي: هل يمكن لنظام ذكاء اصطناعي واحد أن يحدد بشكل موثوق المناطق السرطانية في صور المجهر الرقمية لأنواع عديدة من الأورام، بدلًا من إنشاء أداة منفصلة لكل نوع من السرطان؟ إذا كان ذلك ممكنًا، فقد يخفف ذلك من أحمال العمل، يسرّع التشخيص، ويوسع إمكانية التحليلات المتقدمة حتى نحو السرطانات النادرة التي تندر بياناتها.
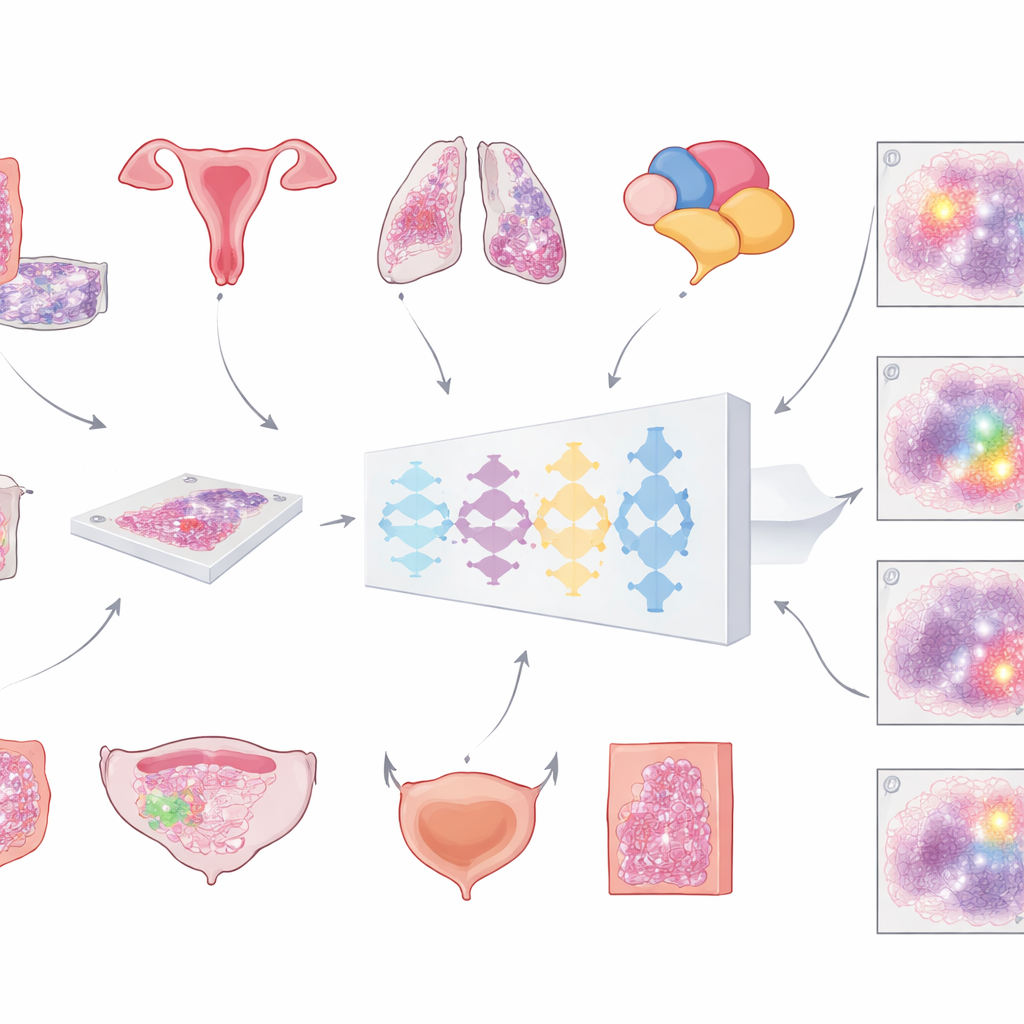
من شرائح الزجاج إلى مساعدات رقمية
تتزايد في المستشفيات الحديثة عمليات مسح شرائح المجهر لإنشاء "صور شريحة كاملة" ضخمة ومفصلة للأورام. الخطوة الأولى الحاسمة لأي تحليل محوسب هي فصل النسيج السرطاني عن بقية المكونات — الخلايا الطبيعية، والدهون، والزجاج الفارغ، والأخطاء البصرية. حتى الآن، تم تدريب معظم الأدوات الآلية على نوع واحد من السرطان فقط، مما يقيد نطاق استخدامها. سعى فريق العمل وراء هذه الدراسة لبناء نموذج واحد شامل يمكنه اكتشاف مناطق الورم عبر عدة سرطانات شائعة في شرائح مصبوغة بصبغات الهيماتوكسيلين والإيوزين الروتينية. كانت رؤيتهم أداة عامة يمكن توصيلها في العديد من سير عمل التشخيص دون إعادة تصميمها في كل مرة.
تدريب نموذج واحد لرؤية عدة سرطانات
لبناء هذا النموذج، جمع الباحثون مجموعة غير معتادة من الشرائح الرقمية من حيث الحجم والتنوّع: أكثر من 20,000 صورة شريحة كاملة من أكثر من 4,000 مريض مصابين بسرطان القولون والمستقيم، وسرطان بطانة الرحم، والرئة، والبروستاتا. جاءت جميع العينات من أنسجة مثبتة بالهكسر (الفورمالين) ومضمّنة في البارافين وتمت مسحها على جهازي مسح عالي الدقة مختلفين. قام باثولوجي بتحديد مناطق الورم بدقة على كل شريحة، موفّرًا "الحقيقة المرجعية" التي سيتعلم منها الحاسوب. اتبع النموذج خط أنابيب متعدد المراحل: تم تقسيم كل صورة ضخمة إلى بلاطات كبيرة متداخلة، مررَت عبر شبكة عصبية عميقة قدّرت، لكل بكسل، مدى احتمال كونه ورمًا، ثم أعيدت التركيب إلى خريطة ناعمة حُولت أخيرًا إلى قناع واضح يميّز الورم عن غيره.
اختبار النظام
الأهم أن الفريق لم يكتفِ بأداء التدريب. اختبروا نفس النموذج على أكثر من 3,000 مريض إضافي عبر ستة أنواع من السرطان — بما في ذلك سرطانات الثدي والمثانة التي لم تُستخدم أثناء التدريب — وعلى شرائح من مستشفيات وأجهزة مسح متعددة. قيست الدقة بشكل رئيسي بمؤشر التداخل المعياري (معامل دايس)، الذي يصل إلى 100% عندما يتطابق حد الحاسوب للورم تمامًا مع ما حدده الباثولوجي. بالنسبة لعينات الأورام الكبيرة والسليمة في سرطانات القولون والمستقيم، وبطانة الرحم، والرئة، والبروستاتا، والثدي، تجاوز متوسط التداخل 80% وغالبًا 90%. وفي مجموعات خارجية كبيرة من مشروع أطلس جينوم السرطان (TCGA)، المأخوذة من مختبرات وأجهزة مسح حول العالم، بقي الأداء فوق 80% أيضًا، ما يشير إلى أن النموذج يعمم جيدًا خارج المؤسسة التي طوّرته.
أين يواجه صعوبات وكيف يقارن
ظهر الضعف الرئيسي في سرطانات المثانة المبكرة التي تُؤخذ عبر إجراء ينتج قطع نسيجية صغيرة ومجزّأة. في هذه الحالات، غالبًا ما يفشل النموذج في تمييز أي ورم على الإطلاق، خصوصًا حين تكون مساحة الورم صغيرة جدًا. ومع ذلك، عندما كشف عن ورم، كان التداخل مع تخطيطات الباثولوجي مرتفعًا، وأدت تعديلات بسيطة على العتبات النهائية إلى تحسين النتائج — ما يوحي بأن الشبكة الأساسية تعرف النمط لكن المعالجة اللاحقة كانت صارمة جدًا. بنى الباحثون أيضًا أربعة نماذج "متخصصة"، كل واحد مدرّبًا على نوع سرطاني واحد، ووجدوا أن أيا منها لم يتفوق بشكل ملحوظ على النموذج العام في مجاله الخاص. بالمقابل، فشلت هذه النماذج المتخصصة إلى حد كبير عند تطبيقها على أنواع سرطانات أخرى، بينما ظل النموذج العام متينًا. ومقارنةً بأداة تجزئة طبية شائعة وأعمّ تتطلب تلميحات من المستخدم، أدّى النموذج الجديد عادةً بمستوى مساوي أو أفضل مع البقاء تلقائيًا بالكامل.
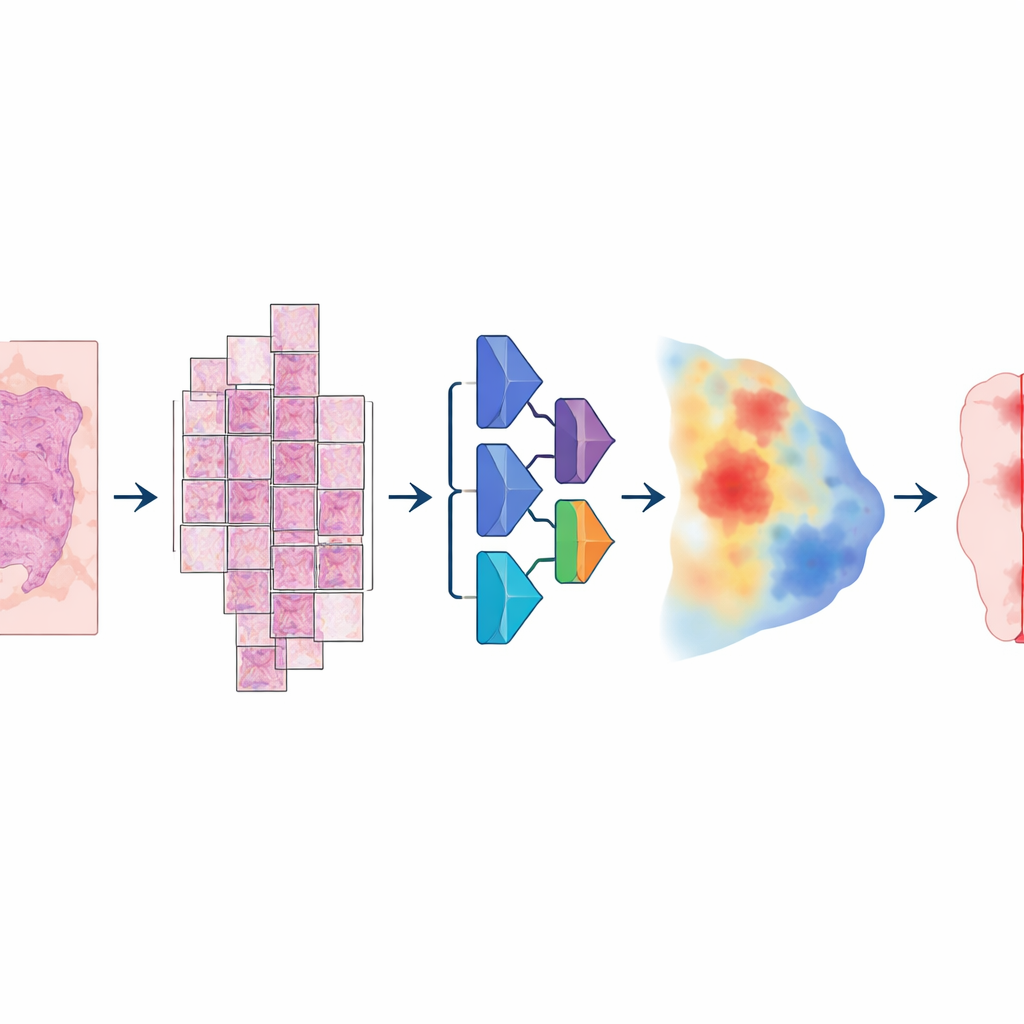
ماذا يعني ذلك للمرضى والأطباء
لغير المتخصصين، الخلاصة الأساسية هي أن نظام ذكاء اصطناعي مصمّم جيدًا واحد يمكنه تمييز النسيج السرطاني على الشرائح الرقمية عبر عدة أنواع أورام رئيسية بشكل موثوق، دون الحاجة إلى إصدارات مخصّصة لكل مرض أو جهاز مسح. لا يغيّر هذا من دور الباثولوجي، لكنه يمكن أن يعلّم مناطق الورم المحتملة مسبقًا، يدعم قياسات متسقة، ويتيح للمتخصّصين التركيز على أصعب الحالات. النسخة الحالية ما تزال تفوت بعض الأورام الصغيرة جدًا أو المبكرة — خاصة عينات المثانة المجزأة ومن المحتمل أن عينات شبيهة بالخزعات — لذا فهي ليست مناسبة بعد لاكتشاف أضعف آثار السرطان. ومع ذلك، تُظهر الدراسة أن تقسيم الورم الشامل "عبر السرطانات" ممكن في ظروف العالم الحقيقي ويمكن أن يشكّل خطوة أولى قوية لأدوات آلية مستقبلية لتقييم درجة السرطان، أو التنبؤ باستجابة العلاج، أو توجيه العلاجات الموجّهة.
الاستشهاد: Skrede, OJ., Pradhan, M., Isaksen, M.X. et al. Generalisation of automatic tumour segmentation in histopathological whole-slide images across multiple cancer types. npj Precis. Onc. 10, 107 (2026). https://doi.org/10.1038/s41698-026-01311-6
الكلمات المفتاحية: الباثولوجيا الرقمية, التعلّم العميق, تقسيم الورم, تصوير الشريحة الكاملة, نموذج عابر للسرطان