Clear Sky Science · ar
التحليل أحادي الخلية واسع النطاق والمحاكاة الحاسوبية للتداخل تكشف التطور الديناميكي لسرطان الكبد: من البداية إلى الاستهداف العلاجي
لماذا الحياة الداخلية لسرطان الكبد مهمة
سرطان الكبدة الخلوي، أكثر أشكال سرطان الكبد شيوعًا، يصعب علاجه بشكل ملحوظ. كثير من المرضى لا يستجيبون جيدًا للأدوية الحالية، وغالبًا ما تعاود الأورام الظهور أو تنتشر. سبب واحد رئيسي هو أن كل ورم عبارة عن خليط فوضوي من خلايا مختلفة تتطور مع الزمن وتتواصل باستمرار مع محيطها. تستخدم هذه الدراسة تقنيات متقدمة لقراءة الجينات على مستوى الخلية الواحدة والمكانية لمراقبة هذا التطور خليةً بخلية، من نمو الورم المبكر إلى المرض المتقدم المقاوم للعلاج، وتحديد نقاط ضعف قد تستغلها علاجات جديدة.
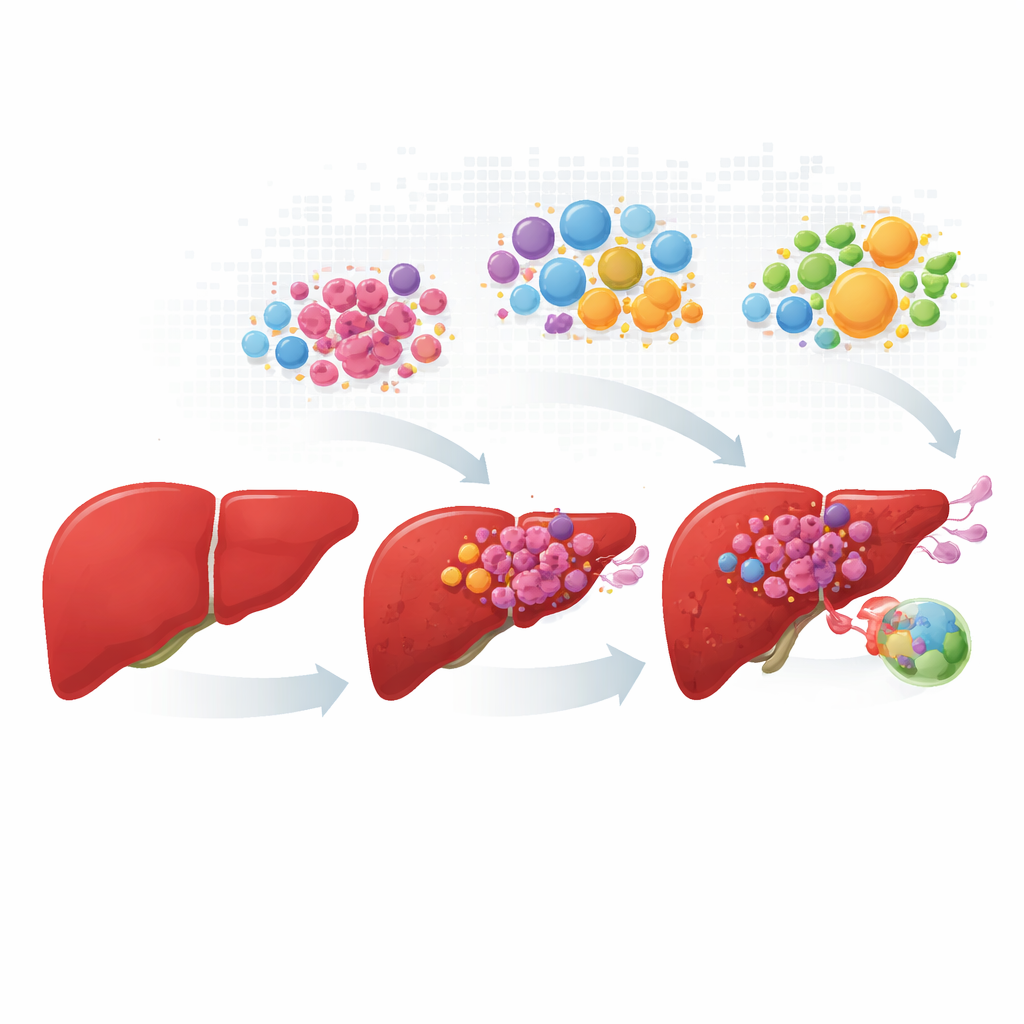
ملاحقة خلايا السرطان من التغير المبكر إلى الانتشار
جمع الباحثون ونسقوا بيانات من أكثر من مئة مريض، شاملة نسيج الكبد الطبيعي والأورام الأولية والنمو داخل الأوعية الدموية وانتقالات إلى العقد الليمفاوية. بدلًا من اعتبار كل ورم كتلة متجانسة، قاموا بتمييز مئات الآلاف من الخلايا الفردية، ثم رسموا مواضع تلك الخلايا في مقاطع الأنسجة الحقيقية. انقسمت خلايا الكبد السرطانية إلى أربع «شخصيات» متكررة. احتفظت مجموعة بقدرات الكبد الطبيعية والمهام الأيضية؛ أما الثلاث مجموعات الأخرى فأظهرت نموًا بدافع الإجهاد، ونشاطًا عاليًا لمسار النمو MYC، أو سلوكًا غازيًا مرتبطًا بالالتهاب. ظهرت هذه الحالات الأربع بنسب مختلفة مع تقدم المرض، حيث سيطرت الخلايا سريعة النمو والغازية في آفات الأوعية والعقد الليمفاوية.
أربع شخصيات للورم ومستقب drawnوات مختلفة
لم تكن حالات الخلايا السرطانية الأربع مجرد تصنيفات نظرية؛ بل ارتبطت بنتائج المرضى. الأورام الغنية بالحالة الشبيهة بالكبد والنشطة أيضيًا كانت مرتبطة ببقاء أفضل، بينما الأورام التي كانت تهيمن عليها الحالات الثلاث العدائية الأخرى انطوت على نتائج أسوأ. ومع ذلك، حتى الحالة «الجيدة» كانت تحمل مفاجأة: فقد كانت موجودة بكثافة لدى المرضى الذين لم يستفيدوا من دواء السورافينيب لعلاج سرطان الكبد، على الأرجح لأن هذه الخلايا تحتفظ بآليات إزالة السموم التي قد تعطّل الأدوية. من خلال إعادة تمثيل تحركات الخلايا على المسارات التنموية، أظهر الفريق أن الخلايا الغازية والالتهابية يمكن أن تتفرع نحو حالات أكثر تمايزًا أو نحو حالات ذات تكاثر أعلى، مما يشير إلى أن خلايا الورم قد تغير هويتها وتتهرب من العلاجات الموجهة لحالة واحدة.
الركن المساند: الحلفاء المناعيون والليفية
الخلايا السرطانية لا تعمل بمفردها. كشفت الدراسة عن خلايا مناعية وخلايا داعمة متخصصة إما تقاتل الأورام أو تساعدها بصمت. ضمن البلعمات، تلك الخلايا التي تعمل كجامعي نفايات وحراس للأنسجة، أنتجت بعض الأنواع إشارات التهابية قد تدعم المناعة المضادة للأورام، بينما أعيد توصيل أنواع أخرى أيضيًا، وكبتت إشارات مفيدة، وعزّزت نمو الأوعية الدموية والغزو. توسعت هذه البلعمات «المسيئة» في العينات المتقدمة. وبالمثل، شكَّلت بعض الخلايا البطانية المبطنة للأوعية والخلايا الليفية التي تبني النسيج الضام مجموعات فرعية مميزة مرتبطة بتنبؤ سيء. في المرض المتقدم، شكلت فئة بطانية معينة ونوعان من الخلايا الليفية عقدًا مترابطة أعادت تشكيل السقالة خارج الخلوية، وأمدت تشكل أوعية دموية جديدة، وارتبطت بأشد حالات الخلايا السرطانية عدائية.
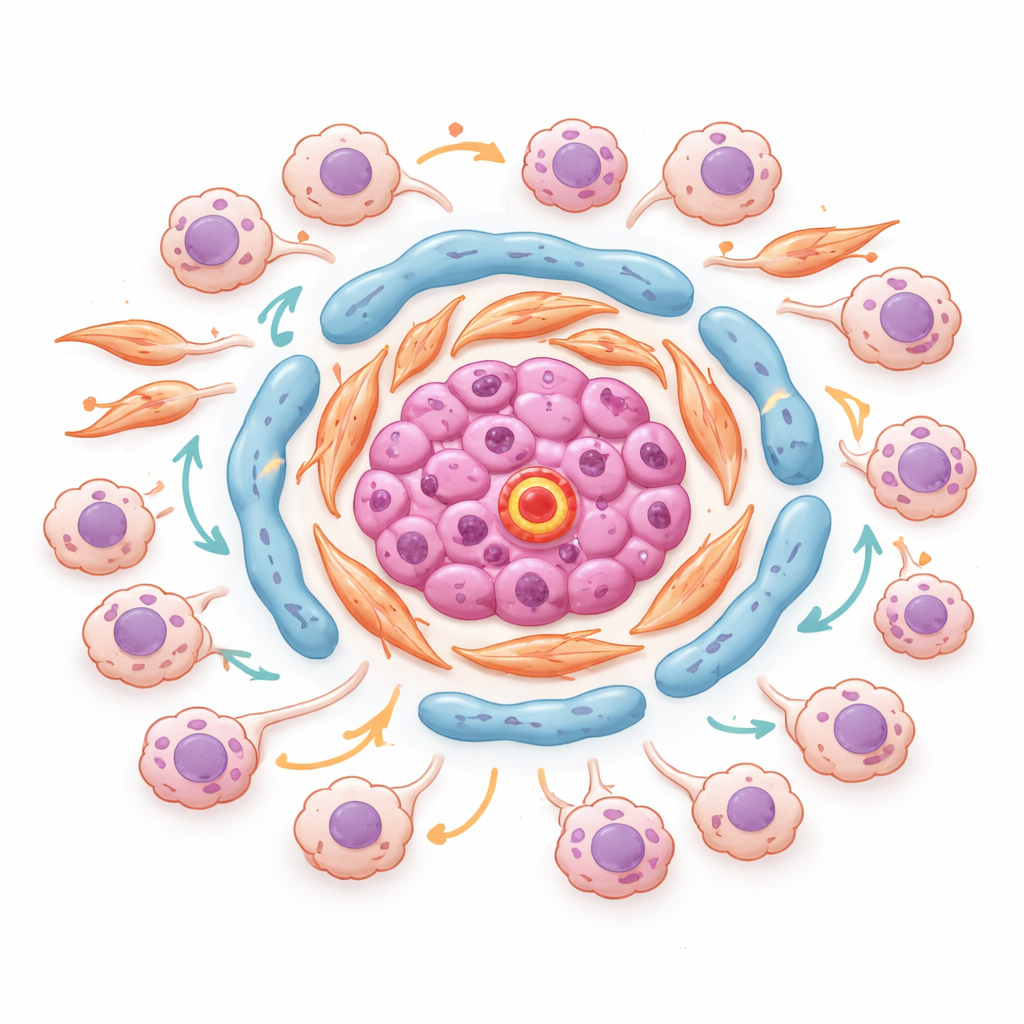
رؤية الأحياء الخطرة داخل الأورام
باستخدام النسخ المكاني، الذي يقيس نشاط الجينات دون فقدان الخريطة المكانية لكل بقعة في النسيج، حدّد المؤلفون «أحياءً» منظمة داخل الأورام. في ورم نموذجي، تجمعت الخلايا البطانية الغنية بجزيء يُدعى ESM1 مع خلايا ليفية راغبة في الدهون ومنتجة للمصفوفة في قلب جزر النسيج الداعم. حول هذه النوى تراكمت خلايا سرطانية مدفوعة بالإجهاد وغازية، في مناطق تتمتع بإشارات قوية لمركب TGF‑beta وإشارات نقص الأكسجة. كانت عوامل النسخ الرئيسية التي تتحكم في استجابة الخلايا للإجهاد والالتهاب مشتركة بين هذه الحالات السرطانية وكانت الأكثر نشاطًا بالذات حيث لامست خلايا الورم تلك العُقد الليفية. هذا يشير إلى أن مناطق ميكروبية محددة عند حواف الورم والنسج الداعمة تشجع بنشاط تحول خلايا السرطان لتصبح أكثر عدائية ومقاومة للعلاج.
العثور على نقطة ضعف مشتركة لعلاجات جديدة
للانتقال من الوصف إلى التدخل، استخدم الفريق نموذج تعلم آلي تدرب على ملايين الخلايا لمحاكاة «حذوفات افتراضية» للجينات والتنبؤ بالتغييرات التي قد تدفع الخلايا الضارة نحو حالات أكثر صحة. بمقارنة البلعمات والخلايا البطانية والخلايا السرطانية، وجدوا مجموعة صغيرة من الجينات التي ساعدت إزالتها على تطبيع الثلاثة معًا. من بينها برزت HSP90B1: تعتمد عليها خطوط خلايا السرطان بدرجة كبيرة، وهي مفرطة الإنتاج في أورام الكبد، خصوصًا تلك المقاومة للأدوية الموجهة والعلاج المناعي، وترتبط مستوياتها العالية ببقاء أسوأ. يشفر HSP90B1 شوهدًا يساعد على التعامل مع الإجهاد في مصنع طي البروتين داخل الخلية ويدعم العديد من المستقبلات السطحية ومسارات الإشارة. وبما أن أدوية انتقائية ضد هذا الشوِد موجودة بالفعل ويمكنها أيضًا إعادة تشكيل البيئة المناعية، تقترح الدراسة HSP90B1 كهدف واعد لتجاوز المقاومة، خاصة عند الجمع معه بعلاجات كبدية حالية.
ماذا يعني هذا للمرضى والعلاجات
تُظهر هذه الدراسة مجتمعة أن سرطان الكبد ليس مرضًا واحدًا بل منظومة ديناميكية من حالات الخلايا والمواضع المكانية التي تتغير مع نمو الورم وانتشاره. من خلال ربط شخصيات خلايا السرطان المحددة والخلايا المساندة والأحياء المكانية بنتيجة المرض واستجابة الدواء، تقدم الدراسة خارطة طريق للعلاج الأدق: مطابقة العلاجات مع الحالات الخلوية السائدة، وتعطيل العقد الليفية التي تزرع السلوك العدائي، واستهداف الاعتماديات المشتركة مثل HSP90B1 التي تعتمد عليها العديد من خلايا الورم وبيئته. وبينما يلزم المزيد من التجارب المخبرية والسريرية، يوفر الأطلس الذي بنته هذه المجموعة مخططًا مفصلًا لتحويل التعقيد الداخلي للورم من عقبة إلى فرصة لعلاجات أكثر ذكاءً وديمومة لسرطان الكبد.
الاستشهاد: Xia, P., Shuang, S., Fu, D. et al. Large-scale single-cell analysis and in silico perturbation reveal dynamic evolution of HCC: from initiation to therapeutic targeting. npj Precis. Onc. 10, 100 (2026). https://doi.org/10.1038/s41698-026-01307-2
الكلمات المفتاحية: سرطان الكبدة الخلوي, تحليل أحادي الخلية, البيئة المصاحبة للورم, نسخ مكاني, HSP90B1