Clear Sky Science · ar
فقدان microRNA-29b يعزز قمع STING عبر DNMT3b ليضعف مناعة الأورام المستحثة بالإشعاع في سرطان القولون والمستقيم المتحور KRAS
لماذا تهم هذه الدراسة
بالنسبة لكثير من مرضى سرطان المستقيم والقولون، يلعب الإشعاع دورًا أساسيًا كجزء من العلاج قبل الجراحة. ومع ذلك، تَكاد بعض الأورام لا تنكمش، وغالبًا ما يعود السرطان أو ينتشر. تستقصي هذه الدراسة سبب مقاومة هذه الأورام للعلاج بالإشعاع والعلاجات المناعية الحديثة من خلال نظرة إلى تغيير جيني شائع في سرطان القولون والمستقيم — وهو طفرة في جين KRAS — وتقترح استراتيجية لإعادة تشغيل جهاز المناعة في الجسم لمواجهتها.
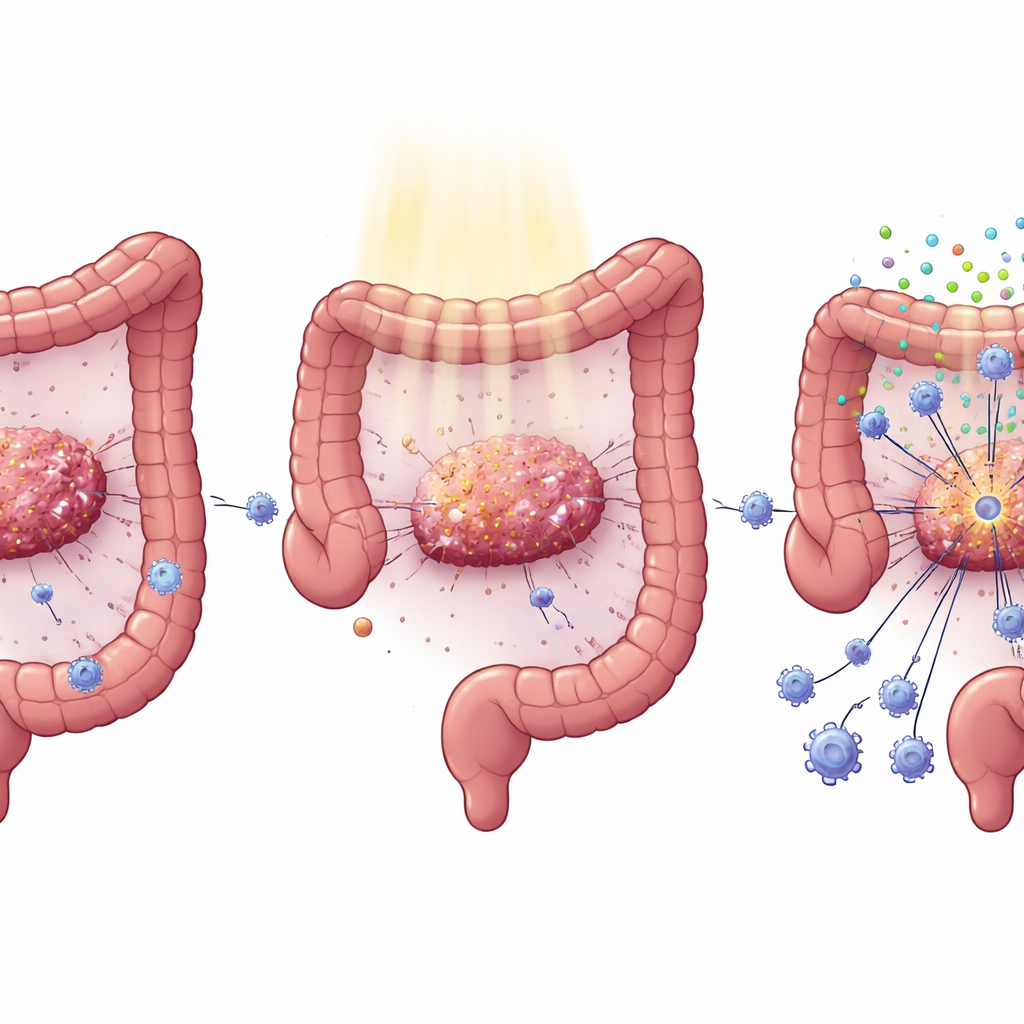
طفرة شائعة تخفي الأورام عن الهجوم المناعي
يحمل سرطان القولون والمستقيم في كثير من الأحيان طفرات في جين KRAS، وهو محرك رئيسي لنمو الورم وانتشاره. لاحظ الأطباء أن الأورام المتحورة في KRAS تميل للاستجابة بشكل سيئ لكل من الأدوية الموجهة والعلاج بالإشعاع. من خلال تحليل قواعد بيانات سرطانية واسعة وفحص عينات مرضى، وجد الباحثون أن الأورام الحاملة لطفرة KRAS تحتوي على عدد أقل من خلايا CD8 القاتلة للسرطان ونشاط أضعف لإشارات الإنترفيرون المعززة للمناعة. لدى المرضى الذين تلقوا العلاج الكيميائي الإشعاعي القياسي قبل جراحة سرطان المستقيم، اكتسبت أورام أصحاب KRAS الطبيعي عددًا أكبر بكثير من خلايا CD8 داخل الأورام بعد العلاج مقارنةً بأصحاب طفرات KRAS، ما يفسر تحسن نتائجهم.
نظام الإنذار الداخلي المفقود داخل خلايا السرطان
لا يعمل الإشعاع فقط على إتلاف حمض نووي الورم؛ بل يمكنه أيضًا أن يكون بمثابة صافرة إنذار، حيث يتسبب في إفراز خلايا السرطان لقطع من الحمض النووي التي تشغل مسار إنذار داخلي يُدعى cGAS–STING. عندما يكون STING نشطًا، تنتج الخلايا إنترفيرونات النوع الأول وإشارات أخرى تجذب الخلايا المناعية وتنشطها، بما في ذلك الخلايا التائية والخلايا الشجرية. أظهر الباحثون أنه في خلايا سرطان القولون والمستقيم المعدلة حسيًا لحمل طفرة KRAS، يكون هذا النظام المكبر مخففًا: بعد الإشعاع، أنتجت هذه الخلايا كمية أقل بكثير من الإنترفيرون والجزيئات ذات الصلة. في الفئران، أدت إسكات KRAS في الأورام إلى استعادة مستويات STING، وتعزيز إشارات الإنترفيرون، وزيادة خلايا CD4 وCD8، وتقليل الخلايا التائية المنظمة، وتحكم أقوى في الورم — ليس فقط في الأورام المعرضة للإشعاع ولكن أيضًا في الأورام النائية غير المعرضة للإشعاع (الظاهرة المسماة abscopal).
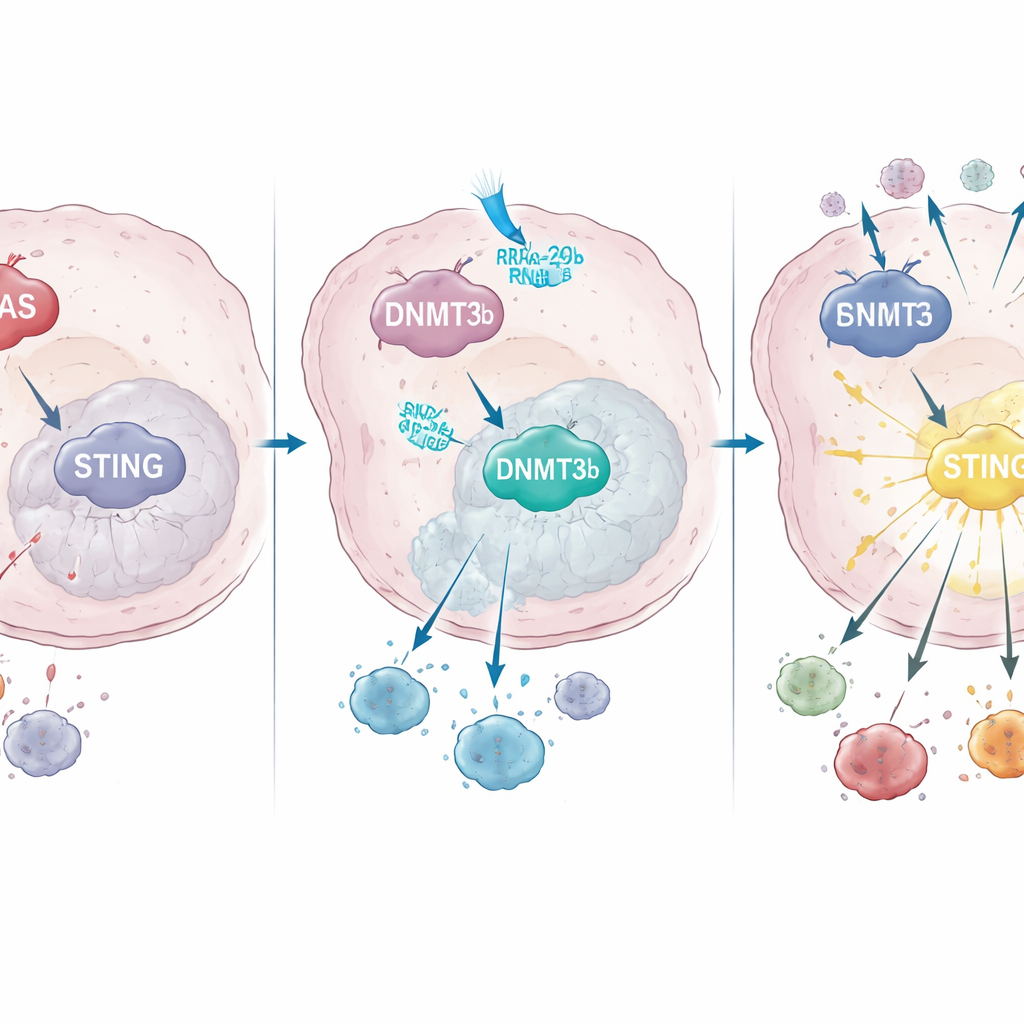
كيف يعيد KRAS ترتيب التحكم الجيني لإيقاف STING
بالغوص أعمق، اكتشف الفريق أن KRAS المتحور يزيد من نشاط إنزيم يعدل الحمض النووي يُدعى DNMT3b، والذي يضيف مجموعات ميثيل إلى مناطق معينة من الحمض النووي ويغلق الجينات المجاورة. في خطوط خلايا سرطانية وعيّنات مرضى، ارتبط ارتفاع DNMT3b بانخفاض STING. كانت منطقة رئيسية من مُروّج STING — أي منطقة "مفتاح التشغيل" الجيني — مغطّاة بشكل كثيف بالميثلة في أورام حاملة لطفرة KRAS، وليس في تلك ذات KRAS الطبيعي. المرضى الذين كانت أورامهم قادرة على زيادة STING بعد العلاج الكيميائي الإشعاعي أظهروا تسللًا أعلى لخلايا CD8 وبقاءً أفضل، مما يبرز أهمية هذا المسار لنجاح العلاج.
حمض رنيني صغير يمكنه إعادة إيقاظ الإنذار
سأل المؤلفون بعد ذلك ما الذي يجعل DNMT3b وفيرًا في السرطانات المتحورة في KRAS. باستخدام تسلسل microRNA، حددوا حمضًا رنينيًا تنظيميًا صغيرًا، microRNA‑29b‑3p، الذي عادةً ما يحدّ DNMT3b لكنه يُقمع بشدة بفعل KRAS المتحور. إعادة هذا microRNA في خلايا KRAS المتحورة المزروعة مخبريًا خفّضت DNMT3b، وأطلقت STING من القمع، وعزّزت إنتاج الإنترفيرون بعد الإشعاع؛ أما حجبها فكان له التأثير المعاكس. في عينات الأورام، مال مرضى KRAS المتحورين إلى وجود مستويات منخفضة من microRNA‑29b‑3p، وارتفاع DNMT3b، وانخفاض STING، وأولئك الذين كانوا لديهم microRNA‑29b‑3p أعلى عاشوا لفترة أطول، ما يربط هذه السلسلة الجزيئية مباشرةً بالنتائج السريرية.
نهج توصيل جيني مستهدف يعزز الإشعاع والمناعة
لتحويل هذه الاكتشافات إلى علاج محتمل، صمّم الفريق فيروسًا غير ضار (AAV) يوصل microRNA‑29b‑3p تحت سيطرة مُروّج نشط أساسًا في خلايا سرطان القولون والمستقيم. في نماذج فأرية تحمل أورامًا متحورة في KRAS، أدى إعطاء هذا الـ AAV مع إشعاع موضعي إلى تقلص كبير في كل من الأورام المشعّة والأورام البعيدة التي لم تتلقَّ إشعاعًا. أظهرت الأورام انخفاضًا في DNMT3b، وزيادةً في STING، ومزيدًا من إشارات الإنترفيرون، واختراقًا واسعًا من قبل الخلايا التائية وخلايا مناعية أخرى. عندما تم دمج نفس علاج microRNA‑29b‑3p مع مثبط نقطة تفتيش مناعية يستهدف PD‑1، تحسّن البقاء أكثر، واعتمد هذا الفائدة على خلايا CD8، مؤكّدًا أن الجهاز المناعي كان يقوم بالمهمة الرئيسية.
ماذا قد يعني هذا للمرضى
بعبارات بسيطة، تكشف هذه الدراسة كيف يقطع سرطان القولون والمستقيم المتحور في KRAS "الوصلة" إلى نظام إنذار داخلي يُفعل عادةً بالإشعاع، ما يسمح له بتفادي الهجوم المناعي. من خلال استعادة حمض رنيني صغير واحد، microRNA‑29b‑3p، استطاع الباحثون تقليل DNMT3b، وإعادة تنشيط STING، وتحويل الأورام المناعية "الباردة" إلى "ساخنة" تستجيب أفضل لكل من الإشعاع ومانعيات نقاط التفتيش. ورغم أن هذا العمل لا يزال في مرحلة ما قبل السريرية، إلا أنه يشير إلى علاجات مستقبلية تجمع بين الإشعاع والعلاج الجيني المستهدف للورم للتغلب على المقاومة في سرطان القولون والمستقيم المتحور KRAS، مما قد يجعل العلاجات الحالية فعّالة لعدد أكبر من المرضى.
الاستشهاد: Chang, HY., Chen, JY., Ke, TW. et al. Loss of MicroRNA-29b promotes DNMT3b-mediated STING downregulation to attenuate radiotherapy-induced antitumor immunity in KRAS-mutated colorectal cancer. npj Precis. Onc. 10, 93 (2026). https://doi.org/10.1038/s41698-026-01290-8
الكلمات المفتاحية: سرطان القولون والمستقيم المتحور KRAS, مقاومة العلاج بالإشعاع, مسار STING, microRNA-29b, علم مناعة الأورام