Clear Sky Science · ar
زيادة تعبير الوحدة الفرعية NDUFS4 في المُركب الميتوكوندري الأول تُسرّع تقدم الورم الدبقي عبر تنظيم وظيفة الميتوكوندريا وCOX5B
لماذا تهم الأورام الدماغية الشهية للطاقة
الأورام الدبقِيَّة تُعد من أكثر أورام الدماغ عدوانية، وغالبًا ما تعاود الظهور حتى بعد الجراحة والإشعاع والعلاج الكيميائي. تدرس هذه الدراسة خلايا الورم الدبقي لتطرح سؤالًا بسيطًا له تبعات كبيرة: هل تعتمد هذه الأورام على جزء معين من "محطات الطاقة" الداخلية لديها للنمو والانتشار؟ من خلال تتبع بروتين ميتوكوندري صغير يُدعى NDUFS4، يكشف الباحثون عن نقطة ضعف استقلابية تبدو أنها تغذي تقدم الورم بينما تترك الخلايا الدماغية السليمة متأثرة بدرجة أقل بكثير.
مفتاح مخفي في محطات طاقة الورم الدماغي
داخل كل خلية تعمل الميتوكوندريا كمولدات صغيرة تحول المغذيات إلى طاقة قابلة للاستخدام. في خلايا الورم الدبقي، تُدفع هذه المولدات إلى حالة مفرطة النشاط. حلل الفريق مجموعات بيانات سرطانية عامة كبيرة وبيانات تسلسل خلية واحدة ووجد أن بروتين NDUFS4، وهو مكوّن في أحد المركبات الرئيسية المنتجة للطاقة في الميتوكوندريا، مرتفع باستمرار في أنسجة الورم الدبقي مقارنة بالدماغ الطبيعي. ارتبطت مستويات NDUFS4 الأعلى بدرجة ورم أكثر تقدمًا وبمرضى توفوا مبكرًا نتيجة مرضهم. وعلى مستوى خلية واحدة، أظهرت البيانات أن هذا الارتفاع في NDUFS4 يتركز تحديدًا في خلايا الورم وليس في الخلايا المحيطة غير السرطانية في الدماغ.
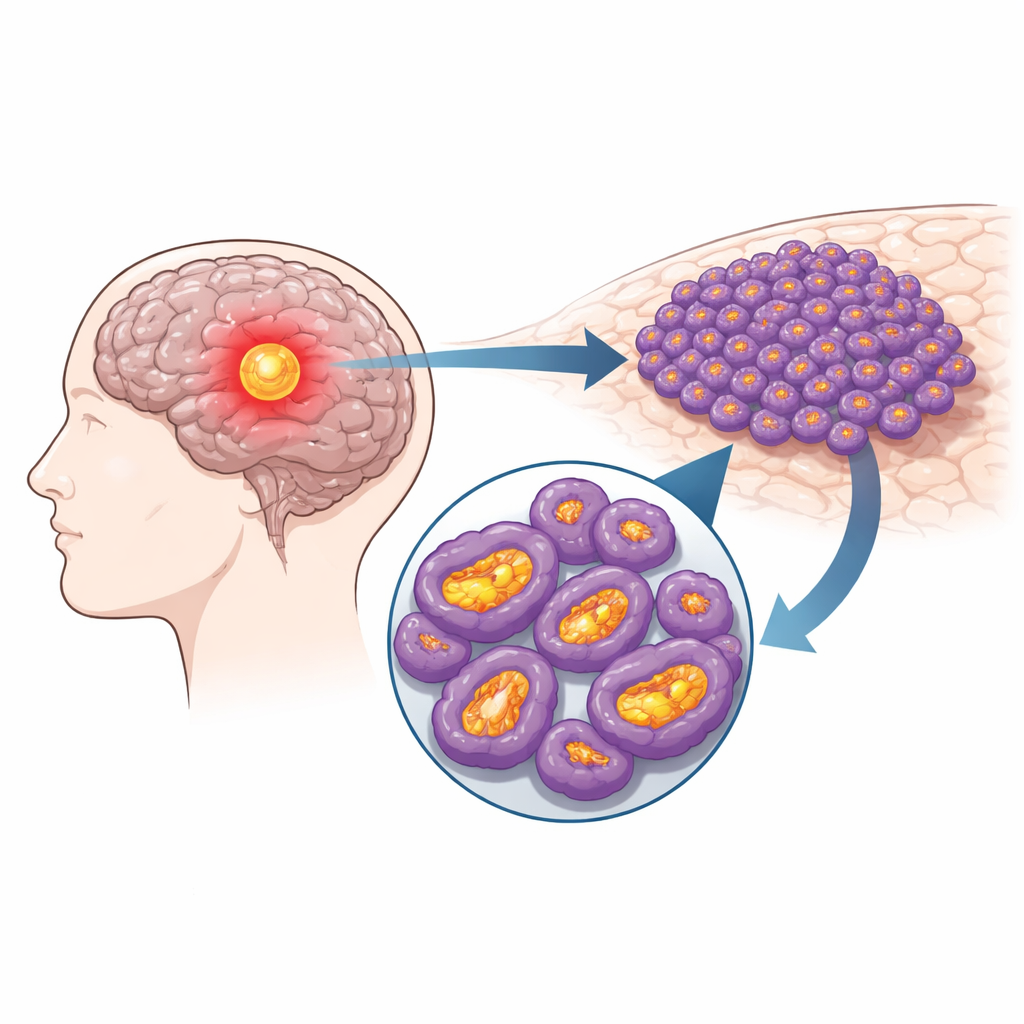
خفض مستوى الطاقة لإبطاء السرطان
لاختبار ما إذا كان NDUFS4 مجرد علامة أم محرك حقيقي، قلّل الباحثون عمدًا من مستوياته أو ألغوه في خلايا ورم دبقي مشتقّة من مرضى ونمت في المختبر. عندما تم إسكات NDUFS4 أو حذفه، تدهورت وظيفة الميتوكوندريا: انخفض استهلاك الأكسجين، تباطأت خطوة رئيسية في تصنيع الطاقة، وتراجع مستوى الوقود الخلوي (ATP). في الوقت نفسه، ازداد تكون نواتج ضارة معروفة بأنواع الأكسجين التفاعلية، وأظهرت الأغشية الداخلية للخلية علامات إجهاد وأكسدة. وظيفيًا، انقسمت هذه الخلايا الجوفاء بالطاقة أقل، شكلت مستعمرات أقل، تحرّكت وغزت بدرجة أقل، وأبدت مزيدًا من علامات الموت المبرمج. اللافت أن نفس الضربة الجينية في الخلايا النجمية غير السرطانية — خلايا داعمة من نسيج دماغي طبيعي — سببت ضررًا ضئيلاً أو لم تسبب ضررًا، مما يوحي بأن خلايا الورم تعتمد بصورة غير عادية على هذا المفتاح الميتوكوندري.
زيادة الطاقة تجعل الأورام أكثر عدوانية
الجانب المعاكس من التجربة رسم صورة واضحة بنفس القدر. عندما أجبر العلماء خلايا الورم الدبقي على إنتاج كميات إضافية من NDUFS4، أصبحت ميتوكوندرياتها أكثر نشاطًا: ارتفع إنتاج الطاقة وعمل المركب التنفسي الرئيسي بوتيرة أعلى. نمت هذه الخلايا المعززة بسرعة أكبر، وهاجرت بسهولة أكبر، وغزت الحواجز بشكل أكثر عدوانية، سواء في خلايا مريض أولية أو في خطوط خلوية مختبرية قياسية. في الفئران، شكلت خلايا ورم دبقي مُهندَسة للحفاظ على مستويات عالية من NDUFS4 أورامًا داخل القحف أكبر، بينما نمت الخلايا ذات NDUFS4 المخفض ببطء أكبر في الدماغ، وأظهرت أداءً ميتوكوندريًا أضعف، ومزيدًا من الضرر التأكسدي، وخلايا أقل انقسامًا، ومزيدًا من الخلايا الميتة. معًا، تؤكد هذه التجارب أن NDUFS4 ليس مجرد راكب بل سائق لتقدم الورم الدبقي.
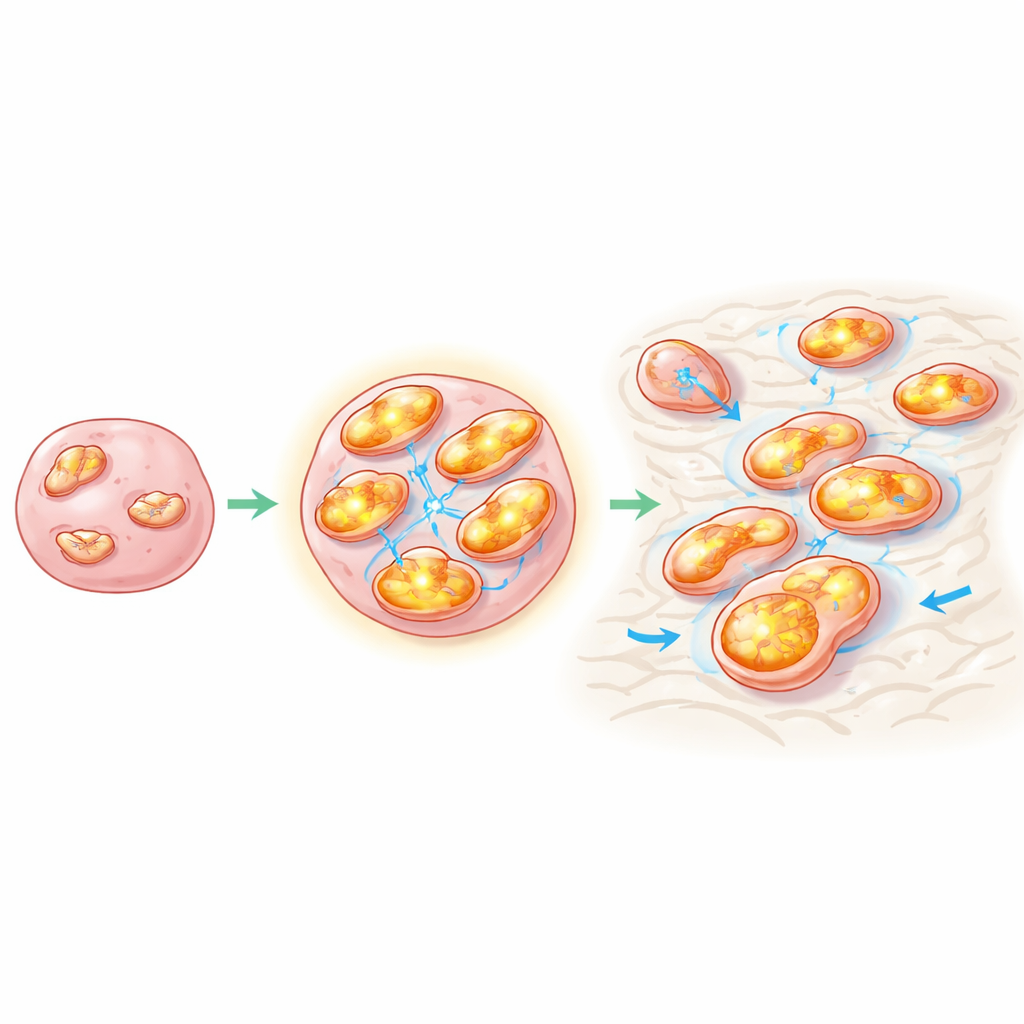
بروتين شريك يربط ضبط الطاقة بسلوك الورم
بتعمق أكثر، سأل الفريق كيف يمارس NDUFS4 مثل هذه التأثيرات الواسعة. من خلال تقاطع بيانات التعبير الجيني من الأورام الكتلية، والخلايا الفردية، وخرائط بروتينات خلايا السرطان، ركزوا على بروتين ميتوكوندري آخر، COX5B، كشريك رئيسي. يساعد COX5B في تشغيل الخطوة النهائية لسلسلة الطاقة الرئيسية في الخلية. وُجد أنه مرتبط بإحكام بمستويات NDUFS4 في الأورام الدبيقية ومعروف بالفعل بارتفاعه في سرطانات أخرى. عندما خفّض الباحثون COX5B في خلايا الورم الدبقي، ظهر النمط نفسه كما في خسارة NDUFS4: تراجع أداء الميتوكوندريا، ازداد الإجهاد التأكسدي، تباطأ النمو والحركة، وارتفع معدل موت الخلايا. والأهم من ذلك، عندما أعادوا COX5B في خلايا ناقصة NDUFS4، انعكس كثير من ضرر الميتوكوندريا والتأثير المضاد للورم. كما وجدوا أن NDUFS4 يؤثر على قوة ارتباط عامل النسخ (Sp1) بمنطقة التحكم في جين COX5B، مما يساعد في ضبط مقدار COX5B الذي تنتجه الخلية.
ماذا يعني هذا لعلاجات سرطان الدماغ مستقبلًا
لغير المتخصص، الرسالة الأساسية هي أن العديد من الأورام الدبيقية تبدو معتمدة على نظام طاقة مفرط النشاط يتمحور حول NDUFS4 وشريكه التالي COX5B. خفض هذا النظام يحرم خلايا الورم من الوقود والتوازن اللازمين للنمو والغزو، بينما يترك خلايا الدعم الدماغية الطبيعية بأذى نسبي قليل. وبما أن هذه الضعف يظهر بثبات في عينات المرضى والخلايا المعزولة وأورام الفئران الدماغية، يبرز NDUFS4 — وسيطرته على COX5B — كهدف واعد لأدوية جديدة. قد تكمل العلاجات التي تعطل هذا "الدائرة الكهربائية" الميتوكوندرية بشكل انتقائي العلاجات القائمة، مما يبطئ نمو الورم ويطيل البقاء دون أن تُلحق أذى جسيمًا بأنسجة الدماغ السليمة.
الاستشهاد: Wu, J., Li, J., Xu, L. et al. Mitochondrial complex I subunit NDUFS4 overexpression drives glioma progression by regulating mitochondrial function and COX5B. npj Precis. Onc. 10, 99 (2026). https://doi.org/10.1038/s41698-026-01281-9
الكلمات المفتاحية: الورم الدبقي, الميتوكوندريا, NDUFS4, COX5B, استقلاب سرطان الدماغ