Clear Sky Science · ar
أطلس متكامل لخلايا سرطان الرئة على مستوى الخلية الواحدة يكشف عن أنماط فيبروبلاست مميزة بين الغددية وسرطان الخلايا الحرشفية
لماذا يهم الحي المحيط بالورم
سرطان الرئة ليس مكوَّناً من الخلايا السرطانية وحدها. إنه أشبه بمدينة مكتظة حيث تعيش الخلايا السرطانية جنباً إلى جنب مع الأوعية الدموية والخلايا المناعية وخلايا الدعم. تطرح هذه الدراسة سؤالاً بسيطاً إلى حد ما لكن ذي تبعات كبيرة: هل يبني الشكلان الرئيسيان من سرطان الرئة غير صغير الخلية — الغُدِّي وسرطان الخلايا الحرشفية — “أحياء” مختلفة داخل الرئة، وهل قد تفسر هذه الاختلافات سبب تحسن أو تدهور حالة المرضى؟ باستخدام أدوات قوية لقراءة الحمض النووي الريبي على مستوى الخلية الواحدة، يرسم الباحثون خريطة لمئات الآلاف من الخلايا الفردية ليكشفوا كيف تتصرف مجموعة رئيسية من خلايا الدعم، المسماة فيبروبلاستات، بشكل مختلف جداً في هذين النوعين من السرطان.
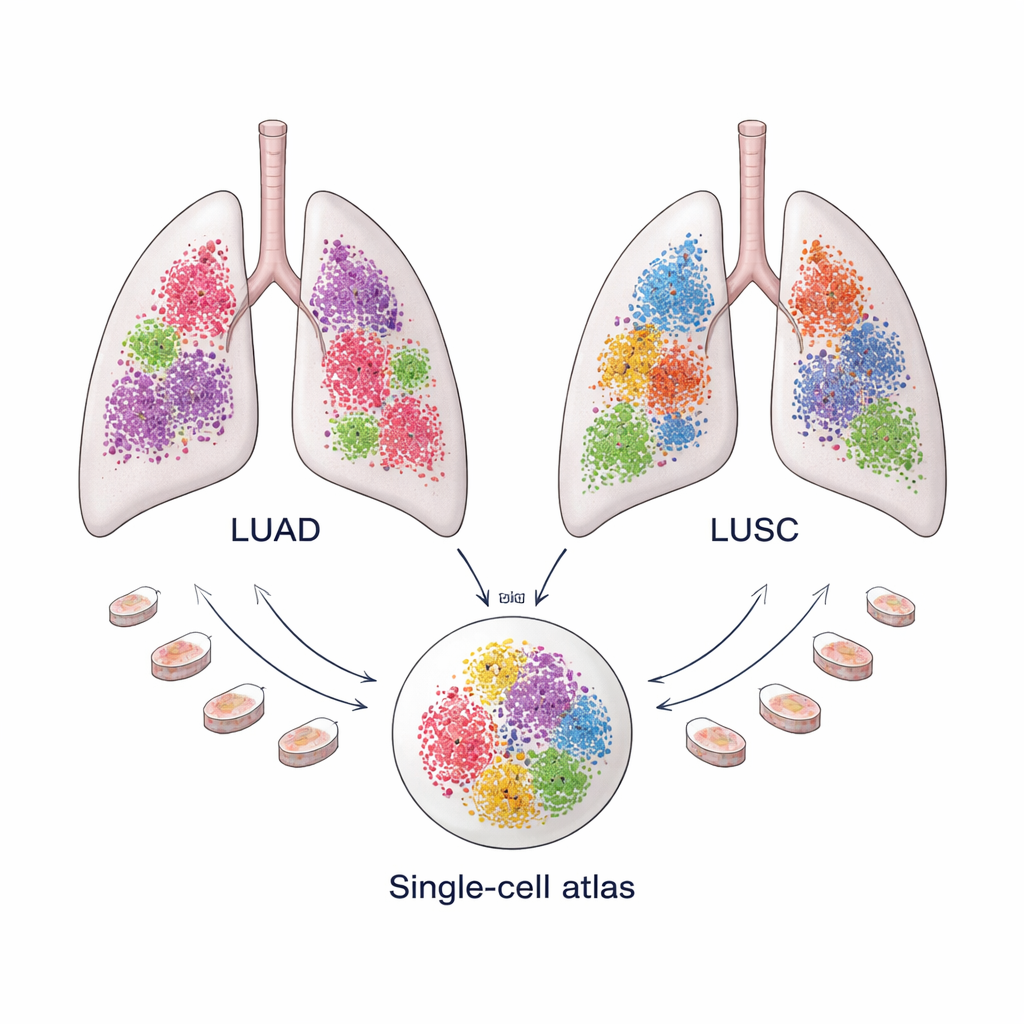
سرطانان شائعان للرئة، نظامان بيئيان مميزان
يشكل سرطان الرئة غير صغير الخلية نحو 85 في المئة من سرطانات الرئة ويهيمن عليه نوعان: الورم الغدي الرئوي (LUAD)، الذي ينشأ غالباً في أجزاء خارجية من الرئة، وسرطان الخلايا الحرشفية الرئوي (LUSC)، الذي يميل إلى الحدوث في مناطق مركزية أكثر. على الرغم من أنهما يُعالجان حالياً تحت تصنيف واحد واسع، فإن استجابتهما للعلاج ونتائجهما على المدى الطويل تختلفان. تشير أدلة متزايدة إلى أن هذه الاختلافات لا تعود للخلايا السرطانية وحدها، بل أيضاً إلى «البيئة الدقيقة للورم» — مزيج الخلايا المناعية والأوعية الدموية والخلايا البنائية التي تحيط بالورم وتتفاعل معه.
بناء أطلس لسرطان الرئة على مستوى الخلية الواحدة
لفهم هذه البيئات الدقيقة تفصيلياً، جمع الفريق «أطلساً» واسع النطاق من بيانات تسلسل الحمض النووي الريبي على مستوى الخلية الواحدة: 366,652 خلية من 175 عينة LUAD و125,238 خلية من 74 عينة LUSC، مأخوذة من عشرة مجموعات بيانات عامة. عمل نمط نشاط الجينات في كل خلية كبصمة سمحت للباحثين بفرز الخلايا إلى مجموعات رئيسية مثل الخلايا المناعية، وخلايا الأوعية الدموية، والخلايا السرطانية، والخلايا البنائية أو «الستروما». ثم أزالت طرق حسابية متقدمة الضوضاء التقنية وموّاءمت العينات بحيث يمكن مقارنة خلايا من مرضى مختلفين مباشرة. هذا الحجم مهم لكون بعض أنواع الخلايا — وخصوصاً الفِيبروبلاست — نادرة ويصعب عزلهن بأعداد كافية في أي دراسة واحدة.
الفِيبروبلاست: صانعو الشكل في مشهد الورم
الفِيبروبلاست خلايا داعمة تبني وتعيد تشكيل النسيج الضام. في الأورام، تتحول إلى فيبروبلاستات مرتبطة بالسرطان (CAFs)، والتي قد تقيد أو تعزز نمو الورم اعتماداً على حالتها. من خلال التركيز على أكثر من 8,700 فيبروبلاست، حدد المؤلفون خمسة أنواع رئيسية من CAFs: فيبروبلاستات ميوفية (mCAFs)، فيبروبلاستات التهابية (iCAFs)، فيبروبلاستات مرتبطة بالأوعية (vCAFs)، فيبروبلاستات دَورانية/منقسمة (cCAFs)، وفيبروبلاستات عارضة للمستضدات (apCAFs). اختلف توازن هذه الأنواع اختلافاً واضحاً بين LUAD وLUSC. ميَّلت أورام LUAD إلى احتواء مزيد من iCAFs التي تفرز مستويات عالية من الجزيئات الالتهابية، بينما كانت أورام LUSC أغنى بـmCAFs التي تنتج نسيجاً صلباً ليفياً وتساعد في تشكيل السقالة الفيزيائية للورم.
خلايا السرطان تعلم الفِيبروبلاست أدوارها
لاختبار ما إذا كانت الخلايا السرطانية نفسها تُوجّه الفِيبروبلاست لتبني هذه الهويات، قام الباحثون بزراعة فيبروبلاستات رئوية طبيعية في أطباق جانب خطوط خلايا LUAD أو LUSC. عند تعرضها لخلايا LUAD، شغّلت الفِيبروبلاست جينات نموذجية لـiCAFs، بما في ذلك إشارات التهابية معروفة مثل IL-6 وبعض الكيميائيّات الجاذبة. وعند اقترانها بخلايا LUSC، شغّلت نفس الفِيبروبلاست جينات mCAF المشاركة في الانقباض الشبيه بالعضل وإنتاج الكولاجين. أشارت تحليلات التواصل بين الخلايا إلى أن خلايا LUAD تستخدم سايتوكينات مثل IL-1 وLIF وOSM لدفع الحالة الالتهابية لـiCAFs، بينما تعتمد خلايا LUSC أكثر على الإشارات الميكانيكية ومسار WNT غير التقليدي لدفع الفِيبروبلاست نحو حالة بناء المصفوفة mCAF.
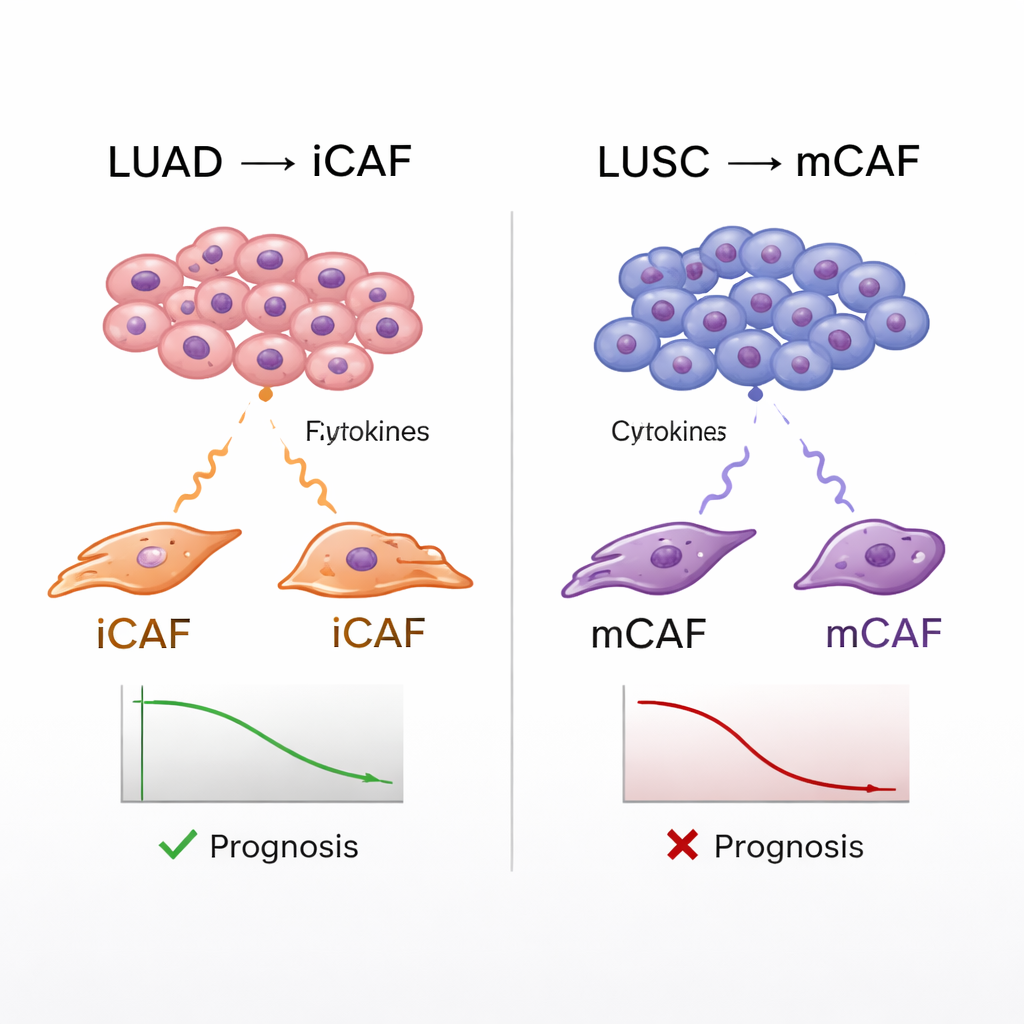
ربط أنواع الفِيبروبلاست بنتائج المرضى
سمح الأطلس أيضاً للفريق بربط أنواع CAFs ببيانات المرضى الواقعية. باستخدام قواعد بيانات سرطانية كبيرة، قدَّروا مدى تعبير كل ورم عن توقيعات جينية لأنواع الفِيبروبلاست المختلفة، ثم قارنوا هذه الدرجات مع البقاء على قيد الحياة. عبر كل من LUAD وLUSC، ارتبطت الأورام الغنية بـmCAFs بنتائج أسوأ، تماشياً مع الفكرة القائلة بأن كبسولة كثيفة ليفية حول الأورام قد تساعد على تقدم السرطان وتعيق الهجوم المناعي. أما iCAFs فأظهرت شخصية منقسمة: في LUSC، تنبأت تواقيع iCAF العالية أيضاً بسوء البقاء، بينما في LUAD ارتبطت بنتائج أفضل. أشارت تحليلات إضافية إلى أنه في LUSC تساعد iCAFs على جذب العدلات — خلايا مناعية تبدو في هذا السياق أنها تقمع الخلايا التائية المفيدة — مما يخلق بيئة معادية بشكل خاص للاستجابات المناعية الفعالة.
ماذا يعني هذا لرعاية سرطان الرئة في المستقبل
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن ليس كل خلايا الدعم في أورام الرئة متشابهة، وأن نفس نوع الفِيبروبلاست يمكن أن يحمل دلالات متعارضة اعتماداً على سياق السرطان. لا تختلف LUAD وLUSC في الشفرة الوراثية لخلايا السرطان فحسب؛ بل تبنيان أنظمة بيئية دقيقة مختلفة تشكل طريقة نمو الأورام ومصائر المرضى. من خلال رسم هذه النظم خلية بخلية، تحدد هذه الدراسة مجموعات محددة من الفِيبروبلاست التي قد تعمل كعلامات للتنبؤ أو كأهداف لعلاجات مستقبلية — مما يتيح، بصورة مثالية، تكييف العلاجات ليس فقط مع نوع السرطان، بل أيضاً مع مزيج الخلايا التي تحيط به وتغذيه.
الاستشهاد: Hirano, Y., Suzuki, H., Nakayama, J. et al. An integrated single-cell lung cancer atlas reveals distinct fibroblast phenotypes between adenocarcinoma and squamous cell carcinomas. npj Precis. Onc. 10, 72 (2026). https://doi.org/10.1038/s41698-026-01279-3
الكلمات المفتاحية: سرطان الرئة, البيئة الدقيقة للورم, الفِيبروبلاست, تسلسل الحمض النووي الريبي على مستوى الخلية الواحدة, تنبؤ السرطان