Clear Sky Science · ar
TheraMind: مجموعة متعددة من نماذج اللغة لتسريع إعادة توظيف الأدوية في سرطان الرئة عبر تنقيب تقارير الحالات
لماذا يهم هذا المرضى والأطباء
بالنسبة للأشخاص المصابين بسرطان الرئة المتقدم، الوقت ثمين وغالبًا ما تنفد خيارات العلاج بسرعة. قد تستغرق عملية تطوير أدوية جديدة من الصفر أكثر من عقد من الزمن، لكن دلائل متفرقة حول علاجات مفيدة قد تكون موجودة بالفعل مختبئة في قصص المرضى المنشورة المعروفة بتقارير الحالات. يقدم هذا المقال TheraMind، نظام ذكاء اصطناعي يبحث عبر آلاف هذه التقارير لاكتشاف أدوية موجودة قد يكون من الآمن إعادة استخدامها لمساعدة مرضى سرطان الرئة صعب العلاج.
تحدي إيجاد استخدامات جديدة لأدوية قديمة
سرطان الرئة غير صغير الخلايا هو أكثر أنواع السرطان فتكًا في العالم، مع معدلات بقاء منخفضة جدًا بمجرد أن ينتشر المرض. إن اكتشاف واختبار أدوية جديدة من الصفر عملية بطيئة ومكلفة ومحفوفة بالمخاطر. بالمقابل، الأدوية «المعاد توظيفها» معتمدة بالفعل لحالات أخرى، لذا فمخاطرها الجانبية معروفة بشكل أفضل. يهتم أطباء الأورام بمثل هذه الأدوية، خصوصًا للمرضى الذين استنفدوا العلاجات القياسية، لكنهم يحتاجون إلى دليل واقعي يشير إلى أن الدواء ساعد بالفعل مريضًا مصابًا بسرطان الرئة—وليس مجرد بيانات مختبرية واعدة. غالبًا ما تظهر هذه الإشارات السريرية في تقارير الحالات الفردية المدفونة عميقًا في الأدبيات الطبية، والتي يصعب العثور عليها يدويًا وتستغرق وقتًا طويلاً.
قارئ رقمي لآلاف قصص المرضى
بنى الباحثون TheraMind ليعمل كقارئ متفانٍ وحذر لتقارير الحالات. انطلاقًا من 18 مرشحًا دوائيًا اقترحتها دراسات جينية ومخبرية سابقة، سحب النظام تلقائيًا 10,023 تقرير حالة من PubMed، أكبر قاعدة بيانات للمقالات الطبية. ثم زوَّد نص كل تقرير لثلاثة نماذج لغوية منفصلة—«قراء» ذكاء اصطناعي مختلفون مدرَّبون على فهم الكتابة الطبية. لكل تقرير، أجابت هذه النماذج عن نفس الأسئلة الأربعة البسيطة: هل وُصف المريض على أنه مصاب بسرطان الرئة غير صغير الخلايا؟ هل أعطي الدواء قيد الدراسة خصيصًا لعلاجه؟ هل تم إيقاف العلاج مبكرًا؟ وهل حقق المريض نتيجة سريرية جيدة؟
كيف تتوصل فريق الذكاء الاصطناعي إلى قرار مشترك
بمجرد أن يحول TheraMind كل تقرير إلى مجموعة من إجابات بنعم أو لا، تدخل عدة طبقات من صنع القرار حيز التنفيذ. تستخدم طريقة واحدة شجرة قرار مصممة يدويًا تتطلب تحقق الشروط الأربعة كلها قبل أن تُعتبر الحالة ذات صلة بإعادة توظيف الدواء. تتيح طريقة أخرى لنموذج واحد تقييم الأدلة بشكل أكثر مرونة، مع الأخذ في الاعتبار إجابات نعم/لا والتوضيحات القصيرة التي أنتجها. وأقوى طريقة تجمع بين ثلاثة مُصنِّفات منفصلة، كلٌّ منها مبني على نموذج مختلف، وتقبل التقرير فقط عندما يتفق اثنان من الثلاثة على أنه ذي صلة. تساعد مقاربة «التصويت بالأغلبية» هذه على إلغاء أخطاء فردية، تمامًا مثل سؤال عدة أطباء مستقلين لمراجعة نفس السجل.
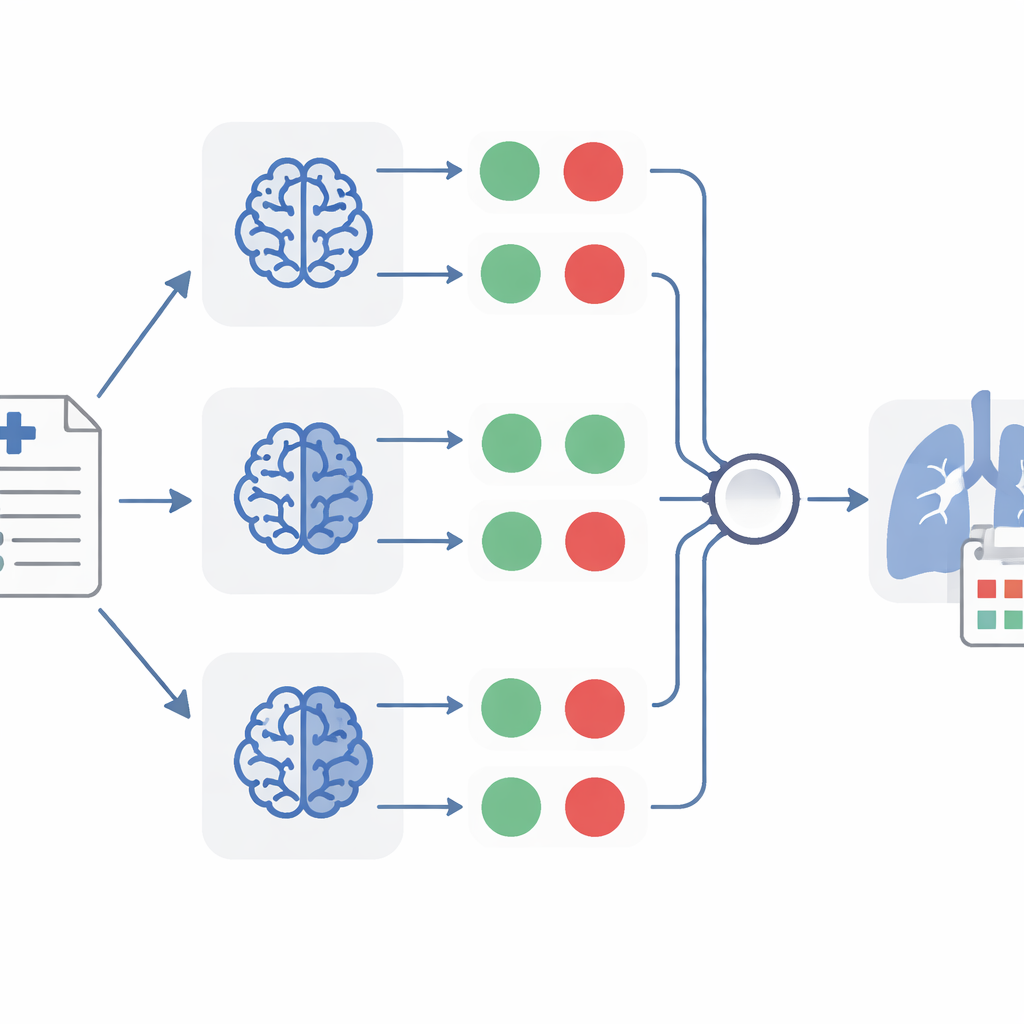
ما اكتشفه TheraMind في تقارير سرطان الرئة
عند تطبيقه على مجموعة كبيرة من تقارير الحالات، وضع TheraMind إشارة على 26 تقريرًا باعتبارها تدعم بقوة استخدام عشرة أدوية مختلفة في سرطان الرئة غير صغير الخلايا. حققت طريقة المجموعة استرجاعًا بنحو 92 بالمئة، مما يعني أنها التقطت تقريبًا جميع التقارير ذات الصلة الحقيقية، مع الحفاظ على خصوصية عالية جدًا بلغت 99.7 بالمئة، بحيث تسلل عدد ضئيل جدًا من التقارير غير ذات الصلة. لكل تقرير مختار، استخرج النظام أيضًا تفاصيل رئيسية عن المريض—مثل العمر، الجنس، السجل الطبي، الحالة، والدواء المشتبه به—في تنسيق بيانات موحد، وأنتج ملخصًا قصيرًا وبسيطًا للحالة. تحقق مراجِعون بشريون من خلفيات في علم الأحياء وعلوم الحاسوب من هذه المخرجات وأكدوا أن أحد النماذج على وجه الخصوص أنتج استخلاصات دقيقة وكاملة للغاية.
تجاوز سرطان الرئة والدخول إلى العيادات
لاختبار مرونة النظام، وجه الفريق TheraMind أيضًا نحو سرطان الثدي وعدة أدوية مرشحة حددتها أبحاثهم السابقة. في ذلك السياق، لم يبلغ النظام عن أي تقارير حالات مطابقة، مما عكس السجل العلمي الحالي بدقة بدلًا من اختراع أدلة. يجادل المؤلفون بأن هذا النوع من خطوط الأنابيب الشفافة والمنظمة—الذي يجمع منطقًا قائمًا على القواعد مع عدة قرّاء ذكاء اصطناعي—يمكن أن يساعد في سد الفجوة بين الاكتشافات المخبرية والعلاجات الجاهزة للتجارب السريرية. ويبرزون كلًا من وعد تطبيق طرق مماثلة على أنواع سرطانات أخرى والحاجة إلى التعامل بحرص مع خصوصية المرضى إذا ما رُبطت الإصدارات المستقبلية مباشرةً بسجلات الصحة الإلكترونية.
ماذا يعني هذا للعلاجات المستقبلية
بعبارة بسيطة، يحول TheraMind قصص المرضى المتناثرة وغير المهيكلة إلى أدلة منظمة يمكن للأطباء والباحثين أن يتصرفوا بناءً عليها. من خلال إبراز التقارير بسرعة التي يبدو أن أدوية موجودة تساعد فيها مرضى سرطان الرئة، يمكنه توجيه أي الأدوية المعاد توظيفها تستحق دراسة أعمق في التجارب السريرية. وبينما لا يحل محل الحكم الطبي، يقدم قارئ الذكاء الاصطناعي متعدد النماذج هذا وسيلة لتنقية جبال من النصوص الطبية وتسليم قائمة قصيرة وموثوقة من الخيارات الواعدة للمرضى الذين يحتاجون بشدة لخيارات جديدة.
الاستشهاد: More, V., Lu, L., Ding, Z. et al. TheraMind: a multi-LLM ensemble for accelerating drug repurposing in lung cancer via case report mining. npj Precis. Onc. 10, 95 (2026). https://doi.org/10.1038/s41698-025-01265-1
الكلمات المفتاحية: إعادة توظيف الأدوية, سرطان الرئة, تقارير الحالات, نماذج اللغة الكبيرة, تنقيب الأدلة السريرية