Clear Sky Science · ar
سِنْتِليماب قبل الجراحة مع باكليتاكسيل مربوط بالألبومين وكاربوبلاتين لسرطان الخلايا الحرشفية المريئي القابل للاستئصال محلياً: دراسة سريرية واستكشاف آلي
قلب المعادلة ضد سرطان الحلق القاتل
يُعد سرطان المريء واحداً من أخطر أنواع السرطان على مستوى العالم، وغالباً ما يُكتشف بعدما يتوغل عميقاً في الصدر. لا يزال بإمكان العديد من المرضى الخضوع للجراحة، لكن حتى مع أفضل برامج العلاج الكيميائي والإشعاعي الحالية، يظل خطر عودة المرض مرتفعاً. تختبر هذه الدراسة نهجاً جديداً لتعزيز دفاعات الجسم قبل الجراحة وتفحص تحت المجهر كيفية تغير الأورام والخلايا المحيطة بها استجابةً للعلاج. تشير النتائج إلى إمكانية علاج أكثر فعالية ومسار نحو رعاية شخصية حقاً.
خطة جديدة بثلاثة أدوية قبل الجراحة
سجل الباحثون 24 مريضاً في الصين يعانون شكلًا شائعاً وعدوانياً من سرطان المريء يُدعى سرطان الخلايا الحرشفية. كانت جميع الحالات متقدمة لكن قابلة للإزالة بالجراحة. قبل الخضوع للجراحة، تلقى كل مريض ثلاث دورات من علاج مركب: سنتيلماب، وهو جسم مضاد منشط للمناعة يساعد الخلايا التائية على التعرف على السرطان؛ بالإضافة إلى دوائين كيماويين قياسيين، باكليتاكسيل مربوط بالألبومين وكاربوبلاتين. بعد هذه المرحلة «قبل الجراحية» أجرِيَت للمرضى العمليات لإزالة ورم المريء، واستمر معظمهم بعد ذلك في تلقي سنتيلماب.
انكماش أعمق للأورام وبقاء مشجع
عندما فحص الجراحون وعلماء الأمراض الأورام المستأصلة، وجدوا أن هذا النظام قبل الجراحة أدى إلى انكماش عميق في العديد من المرضى. نحو 42% أظهروا ما يسميه الأطباء استجابة مرضية كبيرة، بمعنى أن جزءًا صغيرًا فقط من الخلايا السرطانية الحية بقي. واحد من كل ثلاثة مرضى لم يُكتشف فيه أي خلية سرطانية قابلة للكشف في منطقة الورم الرئيسية. على الفحوصات والمتابعة السريرية، كانت النتائج واعدة أيضاً: بعد ثلاث سنوات من العلاج، بقي نحو ثلاثة من بين أربعة مرضى على قيد الحياة دون علامات لعودة المرض، وما يقرب من أربعة من كل خمسة ما زالوا على قيد الحياة. ومن المهم أن الآثار الجانبية لهذا النهج المعزز كانت قابلة للإدارة، دون وفيات متعلقة بالعلاج وبقاء الاستئصال الجراحي آمناً ومُمكِناً.
كيف يشكل «حي» الورم الاستجابة
لم يستفد كل مريض بنفس القدر، لذا تساءل الفريق عن السبب. ركزوا على البيئة الميكروية للورم — الحي المعقّد من الخلايا السرطانية وخلايا المناعة وجزيئات الإشارات. باستخدام قياسات بروتينية مستهدفة على عينات ورمية مُفصولة بعناية، قارنوا بين من استجاب جيداً ومن لم يستجب. قبل العلاج وجدوا 14 بروتيناً اختلفت مستوياتها بين المجموعتين. برز بروتين سطحّي واحد، CD44: الأورام ذات مستويات أعلى من CD44 كانت تميل إلى الاستجابة بشكل أفضل للعلاج القائم على سنتيلماب. بعد العلاج، انخفضت العديد من البروتينات المرتبطة بالنشاط المناعي وإصلاح الحمض النووي لدى المستجيبين، ما يشير إلى أن العلاج المركب نجح في تفكيك نظم دعم السرطان وإعادة تشكيل المشهد المناعي المحلي.
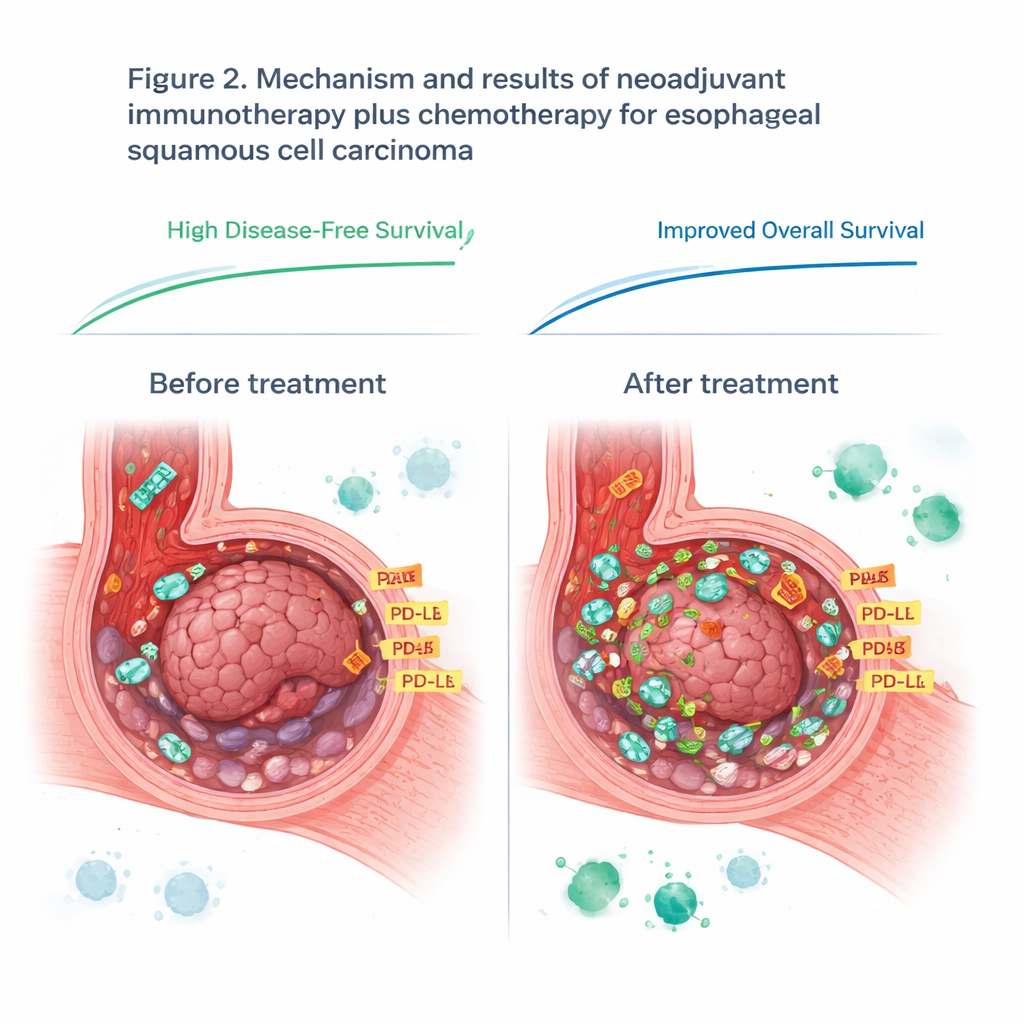
إعادة التفكير في علامة مناعية شائعة
فحصت الدراسة أيضاً PD-L1، وهو بروتين يُستخدم غالباً كدليل لتحديد من قد يستفيد من أدوية نقاط التفتيش المناعية. قبل العلاج، لم تتنبأ مستويات PD-L1 على عينات الورم بمن سيستجيب جيداً، مما يتحدى الممارسة الحالية في هذا النوع من السرطان. مع ذلك ارتفعت مستويات PD-L1 لدى كل مريض أثناء العلاج، على الأرجح لأن الجهاز المناعي المنشط أغرق الورم بإشارات التهابية. بعد العلاج، كانت المستويات الأعلى من PD-L1 في نسيج الورم المتبقي مرتبطة بصورة أوثق بمدى فاعلية العلاج المناعي. هذا يوحي بأن التوقيت مهم: لقطة واحدة لمستوى PD-L1 قبل العلاج قد تغفل تغيرات حاسمة تحدث بمجرد انخراط الجهاز المناعي.
ماذا يعني هذا للمرضى والمستقبل
بالنسبة للأشخاص الموعودين بإجراء جراحة لسرطان المريء المتقدم، تقدم هذه الدراسة رسالتين مشجعتين. أولاً، يبدو أن دمج سنتيلماب مع العلاج الكيميائي قبل الجراحة يُحدث انكماشاً أعمق للأورام وقد يحسّن فرص البقاء طويل الأمد، من دون إضافة آثار جانبية خطيرة. ثانياً، تُظهر الدراسة أن الورم وبيئته الميكروية ليسا ثابتين؛ إنهما يُعاد تشكيلهما بفعل العلاج بطرق يمكن تتبعها عبر بروتينات مثل PD-L1 وCD44. في المستقبل، قد تساعد هذه البصمات الجزيئية الأطباء على اختيار وتعديل العلاجات في الوقت الحقيقي، لتحويل المزيد من الأورام «الباردة» التي تتجاهل الجهاز المناعي إلى أورام «حارة» تدعو إلى هجوم مناعي قوي ودائم.
الاستشهاد: Wu, H., Jiang, Q., Li, X. et al. Neoadjuvant sintilimab, albumin-bound paclitaxel, and carboplatin for locally advanced, resectable esophageal squamous cell carcinoma: clinical study and mechanistic exploration. npj Precis. Onc. 10, 82 (2026). https://doi.org/10.1038/s41698-025-01248-2
الكلمات المفتاحية: سرطان المريء, العلاج المناعي, العلاج قبل الجراحة, مثبطات PD-1, البيئة الميكروية للورم