Clear Sky Science · ar
تصميم علاجات مخصّصة بمساعدة الخوارزميات يحسّن البقاء على قيد الحياة في نموذج فأري لسرطان الثدي ثلاثي السلبيات
لماذا يهمّ تحسين العلاج الكيميائي
العلاج الكيميائي ينقذ الأرواح، لكنه لا يزال يُعطى في الغالب بطريقة «مقاس واحد يناسب الجميع»: يحصل المرضى الذين يعانون من نوع مشابه من السرطان غالبًا على نفس جرعة الدواء في نفس الجدول الزمني. قد يؤدي ذلك إلى آثار جانبية شديدة لبعض الأشخاص وعدم كفاية الفائدة لآخرين. تطرح الدراسة الموضحة هنا سؤالاً بسيطًا لكنه قويًا: ماذا لو كان بإمكاننا استخدام خوارزميات حاسوبية لضبط العلاج الكيميائي لكل مريض في الوقت الحقيقي، بالطريقة التي يضبط بها منظم الحرارة التدفئة في المنزل؟ باستخدام نموذج فأري متقدّم لسرطان ثدي عدواني، يبيّن الباحثون أن مثل هذا التخصيص للجرعات يمكن أن يطيل البقاء ويحدّ من تطور المقاومة للدواء.
مشكلة جداول أدوية السرطان القياسية
اليوم، يتلقى العديد من المرضى أعلى جرعة من العلاج الكيميائي يمكنهم تحملها، تُعطى على فترات ثابتة. لا يأخذ ما يُسمى ببروتوكول الحد الأقصى للجرعة المتحملة في الاعتبار سرعة نمو ورم معيّن، أو كيفية تعامل جسم المريض مع الدواء، أو كيفية استجابة ذلك الورم مع مرور الوقت. نتيجةً لذلك، قد تتقلّص الأورام في البداية ثم تعود لاحقًا بأشكال أكثر مقاومة للدواء، بينما يتحمّل المرضى وطأة الآثار الجانبية القوية. المحاولات السابقة لتحسين ذلك، مثل العلاج الكيميائي «المترونومي» باستخدام جرعات أصغر وأكثر تكرارًا، أعطت نتائج متباينة في التجارب السريرية ولم تحدّد بوضوح أفضل طرق اختيار الجرعات والتوقيت. هناك حاجة واضحة إلى طريقة أكثر عقلانية ومخصّصة لجدولة العلاج الكيميائي.
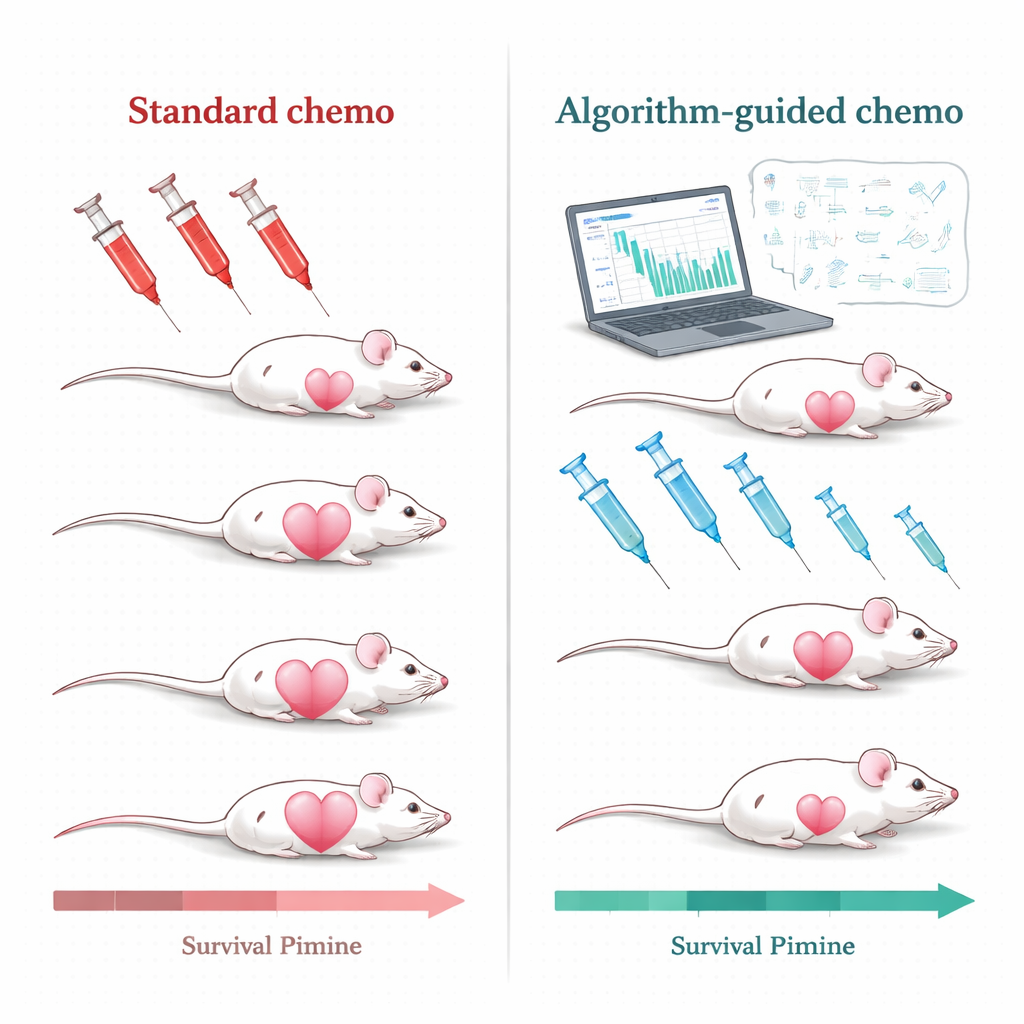
استخدام الخوارزميات لتفصيل العلاج
تعامل فريق البحث مع هذا التحدّي في فئران حاملة لأورام سرطان ثدي ثلاثي السلبيات، وهو نوع من سرطان الثدي يصعب علاجه لدى البشر ويعتمد إلى حدّ كبير على العلاج الكيميائي. عولجت الفئران بصيغة دواء مستخدمة على نطاق واسع، دوكسوروبيسين محاط بالليبوزومات ميثلة (pegylated liposomal doxorubicin). بدلاً من تكرار العلاج بجرعات عالية فقط عندما تعود الأورام إلى حجم محدد، بنى العلماء نماذج رياضية تصف كيفية نمو الورم وتراجع حجمه تحت العلاج، وكيف يتحرّك الدواء داخل مجرى الدم. ثم زوّدوا النماذج بقياسات بسيطة واقعية سريريًا: قراءات متكررة لحجم الورم ومستويات الدواء في الدم. من هذه المدخلات، ولّد خوارزم حاسوبي خطط علاج مخصّصة لكل فأر.
طريقتان لاستخدام الحاسوب للمساعدة
اختبرت الدراسة نمطين من تصميم العلاج بمساعدة الخوارزميات. في نهج واحد، يسمى PDPK، استخدم الحاسوب بيانات مبكرة لتصميم جدول لمدة 30 يومًا من جرعات متكررة إلى حدّ ما وصغيرة تهدف إلى الحفاظ على مستوى الدواء في الدم ثابتًا لكنه منخفضًا — مرتفعًا بما يكفي للتحكم في الورم، ومنخفضًا بما يكفي للحد من السُّمّية. في النهج الثاني، المسمّى التحكم التنبّؤي النموذجي، حدّثت الخوارزمية الخطة يوميًا بناءً على أحدث قياس لحجم الورم، مضبطة أحجام الجرعات لدفع الورم نحو هبوط مستمر. اعتمدت كلتا الطريقتين على نفس الفكرة الأساسية: استخدام «توأم رقمي» واقعي للفأر الحامل للورم لمحاكاة العديد من أنماط الجرعات المحتملة مسبقًا واختيار تلك المرجّحة لتعمل بأفضل شكل ضمن قيود السلامة.
بقاء أطول ومقاومة دوائية أقل
عندما قارَن الفريق هذه الأنظمة الموجهة بالخوارزمية مع بروتوكول الجرعات العالية التقليدي المشغل عند نمو الورم، كانت الفروقات لافتة. تحت العلاج التقليدي، غالبًا ما تتقلّص الأورام حادًا في البداية لكنها تعود في نهاية المطاف، وتشجّع الجرعات الكبيرة المتكررة ظهور أشكال مقاومة للدواء. بالمقابل، حافظت معظم العلاجات المصممة بالخوارزمية على تحكمٍ أشدّ في حجم الأورام، وأطالت زمن الانتكاس، وفي كثير من الحالات منعت ظهور علامات واضحة للمقاومة خلال فترة الدراسة. عبر عشرات الفئران، عاش كلّ من مجموعات PDPK والتحكم التنبّؤي النموذجي لفترة أطول بكثير من الحيوانات التي خضعت للجدول القياسي، مع إظهار عدة استراتيجيات معتمدة على الخوارزميات مكاسب بقاء قوية ذات دلالة إحصائية.
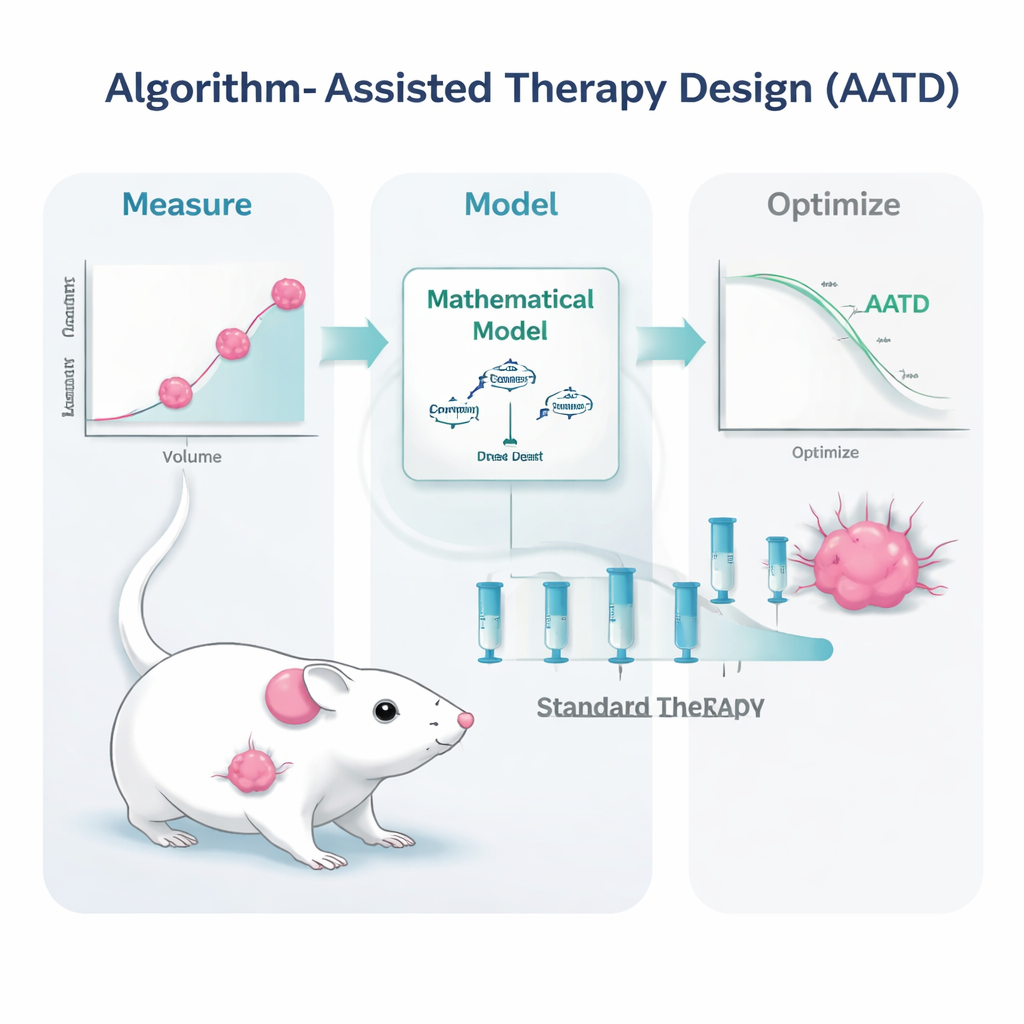
ماذا قد يعني هذا للمرضى في المستقبل
على الرغم من أن هذا العمل أُجري على الفئران، فإن مكوّناته الأساسية — قياس حجم الورم، مراقبة مستويات الدواء في الدم، وتشغيل نماذج حاسوبية — ممكنة بالفعل في المرضى البشر باستخدام تقنيات تصوير ومختبرات حديثة. تقترح الدراسة أنه بدلاً من طرح سؤال «ما هي الجرعة القياسية؟»، قد يتساءل الأطباء يومًا ما: «بالنظر إلى سلوك ورم هذا المريض وكيفية تعامل جسده مع الدواء، ما الجرعة والتوقيت الأنسب الآن؟» تبقى عقبات عملية، مثل الحاجة إلى قياسات أكثر تكرارًا ولوجستيات إعطاء جرعات مرنة، لكن الرسالة واضحة: لا يجب أن يكون العلاج الكيميائي أداة غليظة وموحدة. بمساعدة الخوارزميات، يمكن تحويله إلى أداة أكثر دقة وتكيّفًا تقدّم للمرضى فرصة أفضل للسيطرة طويلة الأمد على السرطانات العدوانية.
الاستشهاد: Gombos, B., Léner, V., Drexler, D.A. et al. Algorithm-assisted individualized therapy design improves survival in a mouse model of triple-negative breast cancer. npj Precis. Onc. 10, 84 (2026). https://doi.org/10.1038/s41698-025-01245-5
الكلمات المفتاحية: العلاج الكيميائي المخصّص, سرطان الثدي ثلاثي السلبيات, العلاج بمساعدة الخوارزميات, نمذجة رياضية للأورام, تحديد جرعات دوكسوروبيسين