Clear Sky Science · ar
فك شفرة النقائل الدماغية في سرطانات المبيض الظهارية: تحليل متعدد الوسائط ومؤشرات حيوية محتملة
لماذا تهم هذه الدراسة
سرطان المبيض مرض خطير بالفعل، لكن لدى عدد قليل من النساء يظهر لاحقًا في موقع أكثر هشاشة: الدماغ. هذه النقائل الدماغية نادرة لكنها غالبًا ما تكون قاتلة، ولا يزال لدى الأطباء وسائل محدودة للتنبؤ بمن هم الأكثر عرضة أو كيفية علاجها بأفضل شكل. تتبع هذه الدراسة ذلك الانتقال من الحوض إلى الدماغ على مستوى جزيئي، مستخدمة أدوات حديثة لتحليل الحمض النووي والحمض النووي الريبي لفهم كيف تتكيف أورام المبيض مع بيئة الدماغ ولتحديد علامات تحذيرية مبكرة قد توجه في يوم من الأيام رعاية أكثر تفصيلاً.
من سرطان شائع إلى تهديد دماغي نادر
السرطان الظهاري للمبيض هو أكثر سرطانات النساء فتكًا في البلدان المتقدمة. يستجيب معظم المرضى في البداية للجراحة والعلاج الكيميائي، لكن نحو 80 في المئة يشهدون في النهاية عودة المرض وتطوره لمقاومة الأدوية. عادةً ما تبقى الانتكاسات داخل البطن؛ فقط جزء صغير من النساء يصبحن عرضة للانتشار البعيد مثل الوصول إلى الدماغ. مع تحسّن العلاجات واطالة عمر النساء، تتاح وقتًا أطول للخلايا السرطانية الشاردة لتستقر في الدماغ، ويلاحظ الأطباء هذه النقائل بتواتر أكبر. بمجرد ظهور النقائل الدماغية، ينخفض متوسط البقاء عادةً إلى أقل من سنة، مما يؤكد الحاجة لفهم كيف ولماذا يحدث ذلك.
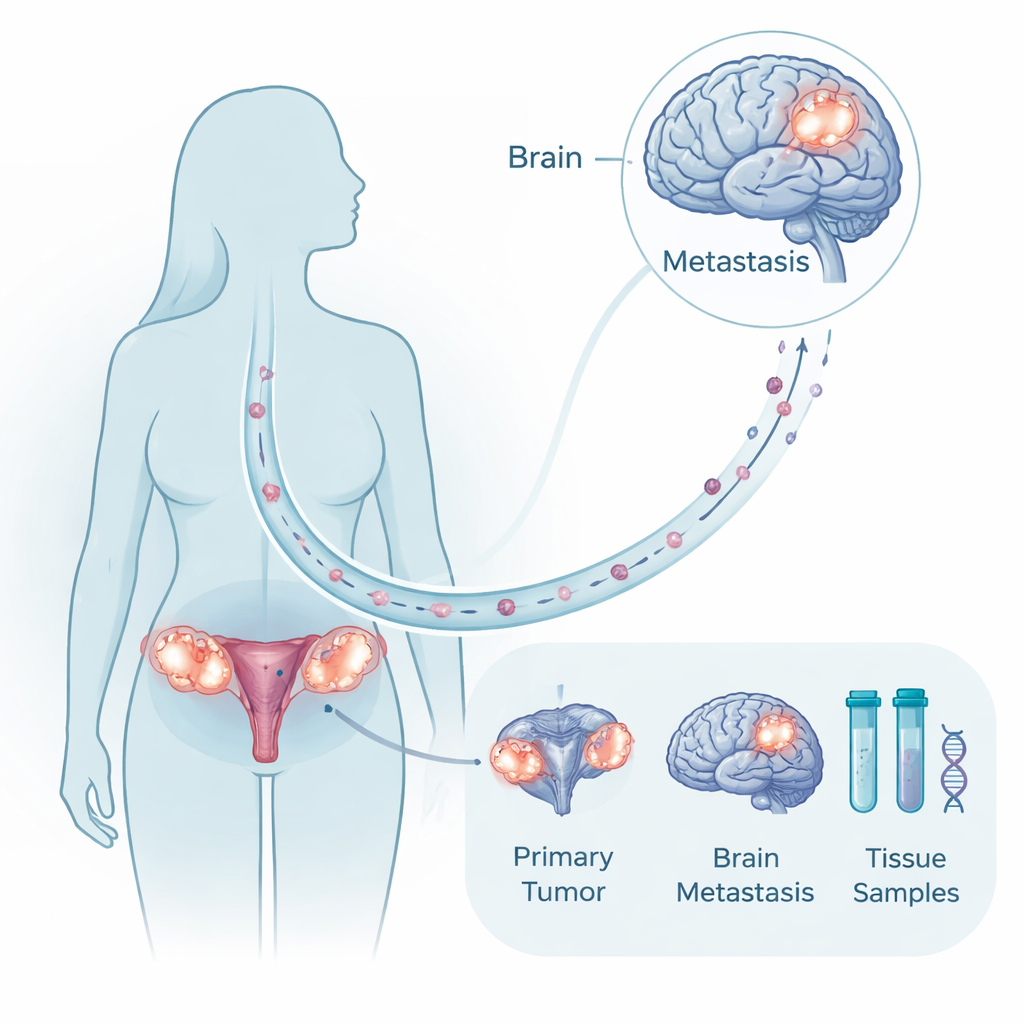
مجموعة نسيجية نادرة لكنها قوية
نظراً لأن جراحة الدماغ غير ممكنة أو غير مناسبة للعديد من المرضى، فمن غير المألوف أن تتوافر عينات ورمية من كل من الكتلة المبيضية الأصلية والترسيب الدماغي المطابق لدى نفس المرأة. جمع الباحثون هذا النوع من المواد المزدوجة لعشر مريضات عولجن على مدار عقدين، إلى جانب عينات مقارنة من دماغ ومبيض سليمين ومن نقائل غير دماغية. حللوا الحمض النووي الورمي للبحث عن طفرات وتغيرات كروموسومية كبيرة، ودرسوا الحمض النووي الريبي لرصد أي الجينات كانت مفعّلة أو مطفأة. سمح لهم هذا النهج متعدد الوسائط بالسؤال عما إذا كانت أورام الدماغ تفرعات جديدة كليًا أم أقارب وثيقة للورم الأولي، وأي البرامج الجزيئية تتغير عندما تستقر الخلايا في الدماغ.
استقرار جيني، لكن سلوك جديد
أظهرت تحليلات الحمض النووي أن الأورام المبيضية الأصلية ونظيراتها من النقائل الدماغية كانت متشابهة بشكل لافت. كلاهما حمل الكثير من نفس الطفرات المسببة للسرطان، خاصة في جين يُدعى TP53، وشارك أصلًا "أحادي النسيلة" عمومًا، ما يعني أن الآفات الدماغية بدت نابعة من نفس الخلية السرطانية الأم. كانت مكتسبات وخسائر كروموسومية كبيرة أكثر شيوعًا إلى حد ما في آفات الدماغ لكنها لم تكن ساحقة. يشير هذا إلى أن الانتقال إلى الدماغ لا يعتمد بالضرورة على اكتساب مجموعة جديدة تمامًا من الطفرات. بدلاً من ذلك، يبدو أن التحول الحاسم يحدث على مستوى نشاط الجينات: أي التعليمات تُقرأ من الحمض النووي وتُستخدم من قبل الخلايا السرطانية أثناء تكيفها مع بيئة الدماغ الفريدة.
كيف تتعلم أورام المبيض العيش في الدماغ
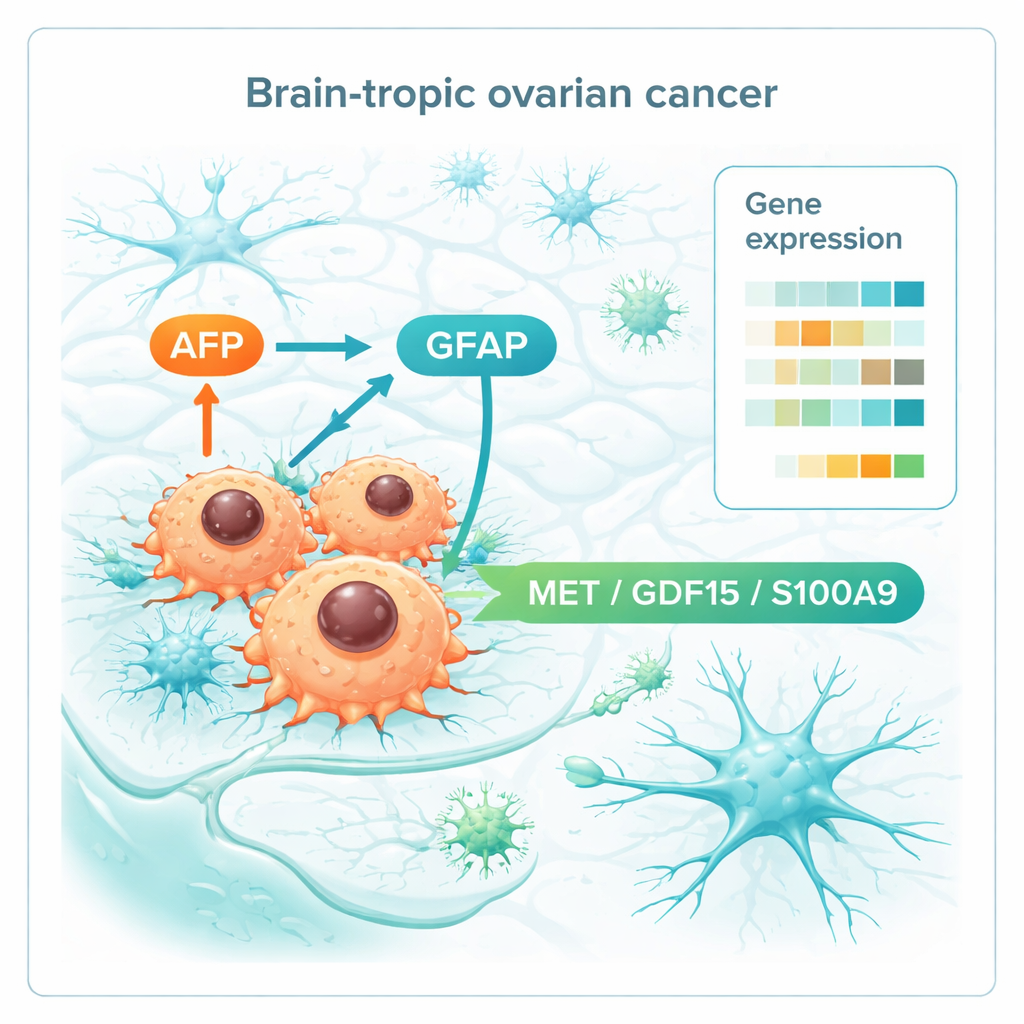
عند مقارنة نشاط الجينات عبر كل الأنسجة، برزت بصمة مميزة للنقائل الدماغية. أظهرت الآفات الدماغية علامات على نمو عدواني، مع تنشيط برامج دورة الخلية التي يقودها منظمات سرطانية معروفة مثل MYC وE2F. كما عدلت البروتينات التي تشكل وتعيد تشكيل السقالة النسيجية، مما يساعد الخلايا على الغزو والتثبيت داخل نسيج الدماغ. ومن اللافت أن بعض الجينات المرتبطة بالخلايا العصبية والخلايا الدبقية أصبحت مفعّلة، مما يوحي بأن خلايا سرطان المبيض تُحاكي جزئيًا خلايا الدماغ للتأقلم. من أبرز هذه الجينات AFP، النشط عادةً في الجنين وبعض الأورام، وGFAP، وهو بروتين مميز لخلايا الدعم في الدماغ. كما حدّد الباحثون مجموعة صغيرة من الجينات المرتفعة بالفعل في الأورام المبيضية الأولية لدى نساء تطورت لديهن لاحقًا نقائل دماغية ولكنها لم تكن مرتفعة لدى الناجيات طويلات الأمد دون إصابة الدماغ. شملت هذه البصمة "ما قبل النقيليّة" تعديلًا مناعيًا، وتواصلًا مع إشارات شبيهة بالعصب، وتغيرات في التمثيل الغذائي.
إشارات تحذير مبكرة وتواصل جزيئي
بتعمق أكبر، ركز الباحثون على الجزيئات الموجودة على سطح الخلية أو المطروحة خارجيًا، لأنها مرشّحة أساسية لفحوصات دم أو أهداف علاجية. حدّدوا ثلاثة عوامل — MET وGDF15 وS100A9 — كانت أعلى باستمرار سواء في الأورام الأولية المهيأة للانتقال إلى الدماغ أو في النقائل الدماغية نفسها. تشارك هذه الجزيئات في حركة الخلايا، واستشعار الإجهاد والمغذيات، وتشكيل البيئة المناعية، مما يوحي بأنها تساعد خلايا سرطان المبيض على التواصل مع نسيج الدماغ وإعادة تشكيله لصالحها. مع AFP وGFAP، تشكل هذه قائمة قصيرة من المؤشرات الحيوية المحتملة التي قد تُشير يومًا ما إلى المرضى المعرضين لخطر عالٍ أو توجه إلى عقاقير تعطل تواصل الورم مع الدماغ.
ماذا يعني هذا للمرضى
في الوقت الراهن، لن يغير هذا العمل العلاج فورًا، ويعترف المؤلفون بأن مجموعة المرضى لديهم صغيرة. ومع ذلك، من خلال إظهار أن أورام المبيض التي تنتشر إلى الدماغ تحتفظ بجزء كبير من تركيبتها الجينية الأصلية بينما تعيد برمجة كيفية استخدام جيناتها، تبرز الدراسة طرقًا جديدة لرصد المشكلة مبكرًا. إذا أكدت الأبحاث المستقبلية أن مؤشرات مثل AFP وGFAP وMET وGDF15 وS100A9 تشير بشكل موثوق إلى ميل للانتشار إلى الدماغ، قد يراقب الأطباء بعض المرضى عن كثب، أو يعدّلون خيارات العلاج، أو يجرّبون أدوية تعيق هذه المسارات. جوهريًا، تبدأ الدراسة في تحويل هذه المضاعفة المتأخرة المرعبة إلى عملية يمكن قياسها وفهمها وفي النهاية اعتراضها.
الاستشهاد: Trozzi, R., Salvi, M., Karimi, M. et al. Deciphering brain metastasis in epithelial ovarian cancer: multimodal analysis and potential biomarkers. npj Precis. Onc. 10, 83 (2026). https://doi.org/10.1038/s41698-025-01206-y
الكلمات المفتاحية: سرطان المبيض, نقائل دماغية, مؤشرات حيوية, تعبير جيني, طب دقيق للسرطان