Clear Sky Science · ar
محور STAT3-ANGPT2-PTGIS المدفوع بالخلايا الدهنية يعزز النقائل الجلدية في سرطان الثدي ويمثل مسارًا قابلاً للاستهداف
لماذا انتشار سرطان الثدي إلى الجلد مهم
عندما ينتشر سرطان الثدي، يتبادر إلى ذهن معظم الناس العظام أو الكبد أو الرئتين. ومع ذلك، يعاود السرطان الظهور لدى كثير من المرضى في مكان غير متوقع: جلد جدار الصدر، أحيانًا بعد سنوات من استئصال الورم الأصلي. هذه العقيدات الجلدية المستمرة والمؤلمة ليست مجرد مسألة تجميلية—بل هي علامة على مرض عدواني يصعب علاجه. تبحث هذه الدراسة في سبب انجذاب بعض سرطانات الثدي إلى الجلد، كاشفة عن شراكة مفاجئة بين خلايا السرطان والنسيج الدهني المجاور والأوعية الدموية واللمفاوية التي تغذي الأورام.
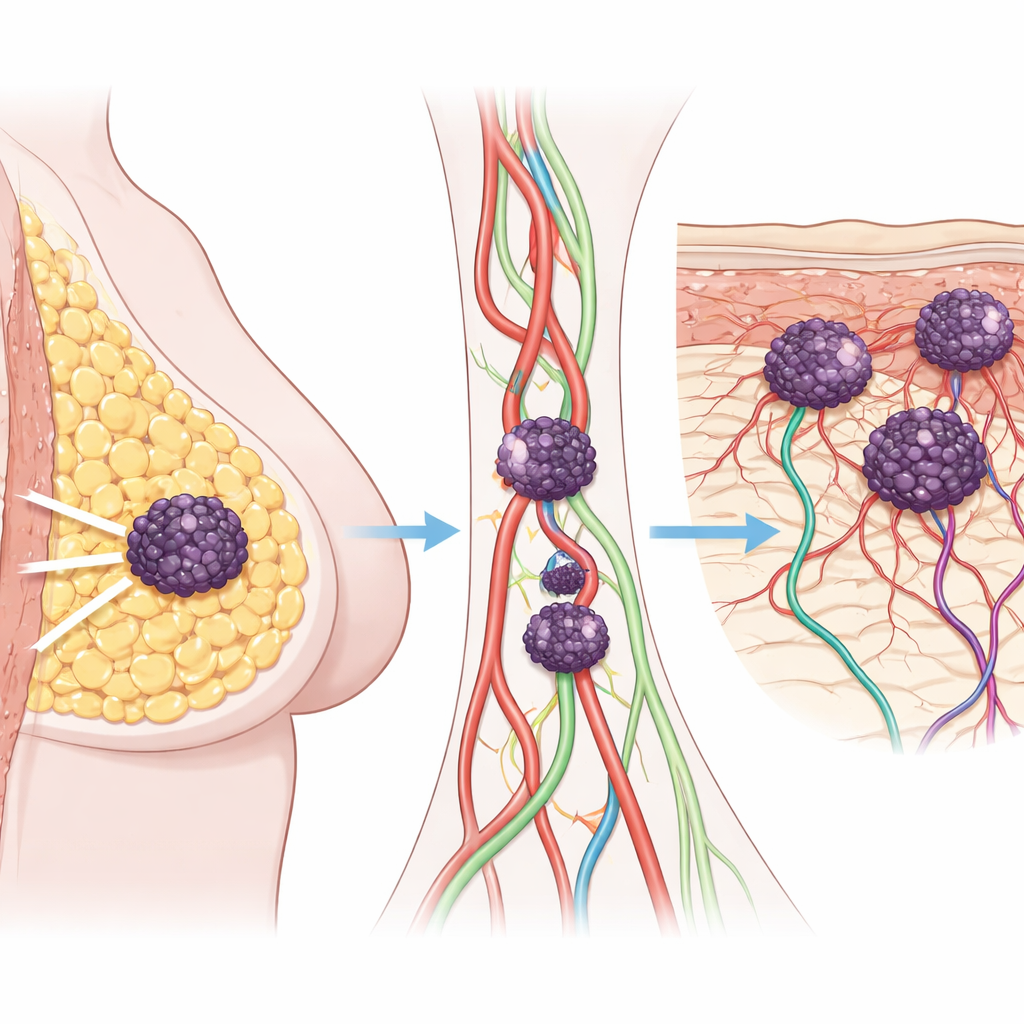
الأورام الجلدية كعلامة تحذيرية
فحص الباحثون أولًا السجلات الطبية لـ126 شخصًا مصابًا بسرطان الثدي، ووافقوا بين من لم ينتكسوا أبدًا، ومن انتشر لديهم السرطان إلى أعضاء مثل الرئتين أو العظام، ومن طور نقائل جلدية. المرضى الذين عادت إليهم الإصابة في الجلد فقط كانوا لديهم بالفعل أورام أكثر تقدّمًا ونموًا سريعًا عند التشخيص. أظهرت سرطاناتهم معدلات انقسام خلوية عالية وغزوًا مبكرًا للأوعية الدموية واللمفاوية. وحتى عندما لم يكن لدى بعض هؤلاء المرضى انتشار مرئي إلى أعضاء بعيدة، كان بقاؤهم العام والفترة الخالية من المرض أسوأ من المرضى دون إصابة جلدية، ما يبرز أن النقائل الجلدية تشير إلى شكل خاص وعدواني من سرطان الثدي.
الأوعية الدموية والدهون تشكّل البيئة الجلدية
لفهم ما يجعل الجلد أرضًا خصبة، تابعت الفريق مريضًا واحدًا لعدة سنوات، جامعًا عينات من الورم الثديي الأصلي ولاحقًا من العقيدات الجلدية. تحت المجهر، كانت كل من آفات الثدي والجلد مليئة بأوعية دموية ولمفاوية متشكلة جديدة—طرق دقيقة تساعد خلايا السرطان على الانتقال والاستقرار. أظهر تحليل نشاط الجينات أنه مع تقدّم المرض، شغّلت الأورام شبكات كاملة مرتبطة بنمو الأوعية الدموية والالتهاب والتعامل مع الدهون والأحماض الدهنية. على وجه الخصوص، أصبحت المسارات التي تكسر الدهون الغذائية الشائعة، مثل حمض الأراكيدونيك وحمض اللينوليك، أكثر نشاطًا، مما يشير إلى أن وقود الدهون وطبقات الجلد الدهنية تساهم في تطور الورم.
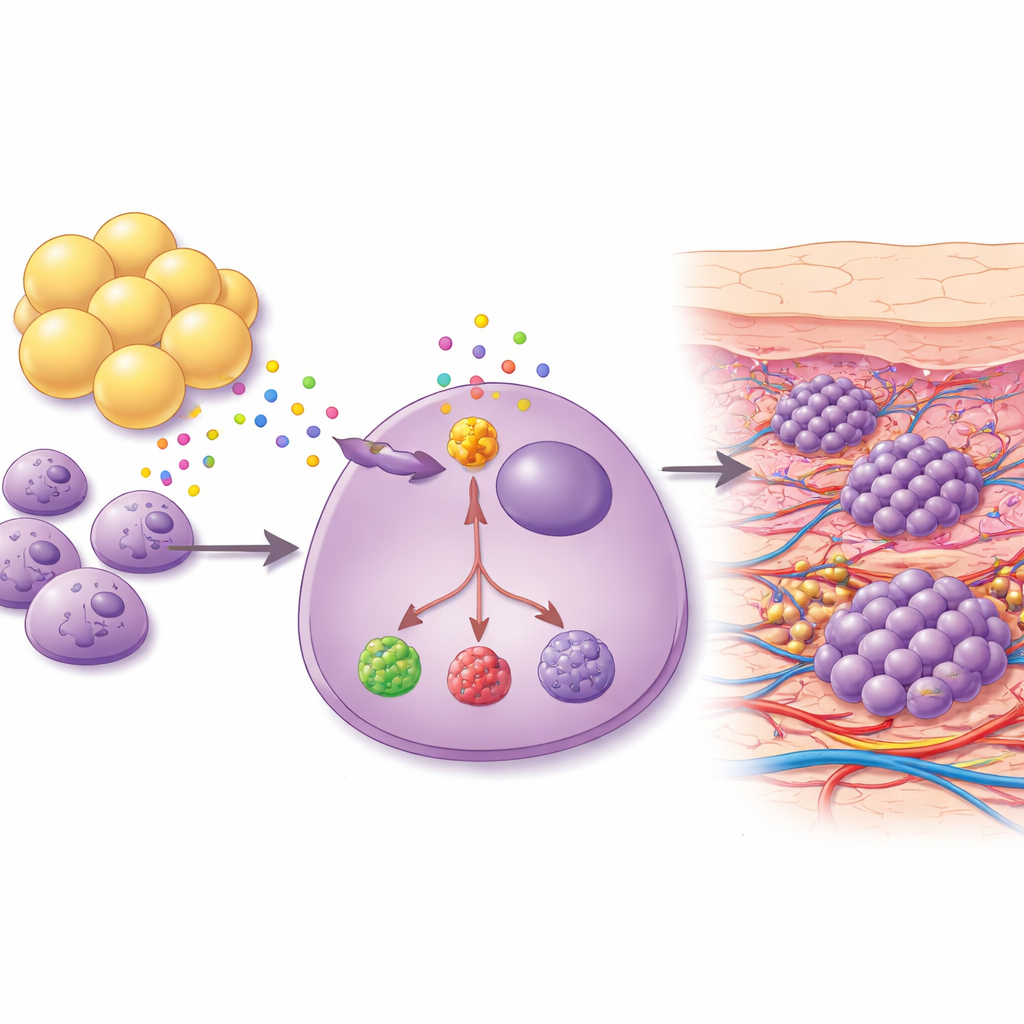
الخلايا الدهنية ترسل إشارات نمو قوية
نظرًا لأن الثدي وجدار الصدر السفلي غنيان بالدهون، تساءل العلماء عما إذا كانت الخلايا الدهنية نفسها قد تغري خلايا السرطان نحو الجلد. زرعوا خلايا سرطان ثدي مع الخلايا الدهنية—الخلايا الدهنية الناضجة—من نفس المريض وجمعوا خليط الجزيئات التي أفرزتها الخلايا الدهنية. هذا الخليط عزز بقوة قدرة خلايا الأوعية الدموية على تشكيل هياكل أنبوبية في المختبر، وهو علامة مميزة لتكوّن الأوعية. في نماذج الفئران، أدى تعرّض الأورام لسائل مشتق من الخلايا الدهنية إلى نمو سرطاني جديد في مناطق غنية بالجلد والدهون مثل الرقبة والظهر. كانت الخلايا السرطانية المأخوذة من هذه الآفات الجلدية أكثر شبهاً بالخلايا الجذعية، وأكثر مقاومة لموت الخلايا، وأنتجت مستويات أعلى من عوامل محفزة للنمو والالتهاب، بما في ذلك بروتين يُدعى ANGPT2 وإنزيم أيضي اسمه PTGIS.
مفتاح إشاري يمكن إيقافه
بتعمق أكبر، قارن الفريق الخلايا الورمية العادية بنظيراتها الميالة للجلد فوجد أن مسار تواصل شائع داخل الخلايا—مسار JAK–STAT—كان مفعلًا بقوة، وخصوصًا البروتين STAT3. عند تنشيطه، عمل STAT3 كقائد رئيسي، رافعًا مستويات ANGPT2 وVEGFC (المحفز لنمو الأوعية اللمفاوية) وPTGIS، وكلها تشجع تكوّن الأوعية وإعادة تشكيل بيئة الورم. أدى حجب STAT3 بواسطة دواء يُدعى Stattic إلى تقليل نمو أورام الجلد في الفئران وخفض مستويات هذه العوامل اللاحقة. في عينات مرضى، ارتبط نشاط عالي لـSTAT3 وANGPT2 وPTGIS بتدهور فترة الخلو من التقدّم والفترة الخالية من المرض، وكانت هذه العلامات مرتفعة بشكل خاص لدى المرضى الذين اقتصرت نقائلهم على الجلد.
ماذا يعني هذا للمرضى
تجدر الإشارة إلى أن العمل يجسد نقائل الثدي الجلدية كنوع فرعي مميز وخطير تغذيه تفاعل ثلاثي بين خلايا السرطان والدهون المحيطة والأوعية التي تغذي الأورام. تنشّط إشارات الخلايا الدهنية STAT3 داخل خلايا السرطان، والتي بدورها تزيد ANGPT2 وPTGIS وتعيد تشكيل أيض الأحماض الدهنية، مما يجعل الجلد بيئة مضيافة يمكن للأورام الاستقرار فيها والتوسع. بالنسبة للمرضى، يعني هذا أن النقائل الجلدية ليست مجرد عودة "محلية" بل علامة على بيولوجيا عدوانية. والمشجع هو أن المسار نفسه الذي يقود هذه العملية قد يكون نقطة ضعفها: الأدوية التي تستهدف STAT3 أو إنزيمات أيضية رئيسية مثل PTGIS قد تساعد مستقبلاً في قطع خطوط الدعم التي تسمح لسرطان الثدي باستعمار الجلد.
الاستشهاد: Luo, CW., Ou-Yang, F., Chang, SJ. et al. Adipocyte-driven STAT3-ANGPT2-PTGIS axis promotes cutaneous metastasis in breast cancer and represents a targetable pathway. npj Precis. Onc. 10, 111 (2026). https://doi.org/10.1038/s41698-025-01184-1
الكلمات المفتاحية: نقائل الجلد في سرطان الثدي, بيئة الورم الدقيقة, إشارات الخلايا الدهنية, مسار STAT3, تكوّن الأوعية الدموية