Clear Sky Science · ar
النقل الجيني Mediated بواسطة PiggyBac والقص بواسطة CRISPR–Cas9 في فراشة الشمع الكبرى، Galleria mellonella
يرقة صغيرة ذات إمكانات طبية كبيرة
تخيل اختبار مضادات حيوية جديدة أو دراسة عدوى خطرة دون استخدام الفئران أو الثدييات الأخرى. تظهر يرقات فراشة الشمع الكبرى، Galleria mellonella، كنموذج بديل منخفض التكلفة وجذاب من الناحية الأخلاقية لمثل هذه التجارب. تُظهر هذه الدراسة كيف قطع العلماء خطوة كبيرة إلى الأمام عبر تزويد هذه اليرقات بالأدوات الوراثية نفسها التي جعلت ذباب الفاكهة وأسماك الزرد أدوات قوية في أبحاث الطب الحيوي.
لماذا يهم هذا الحشر لن الصحة البشرية
تُحاكي يرقات Galleria mellonella استجابة الأجسام البشرية للجراثيم بشكل مدهش. يمكن حفظها عند 37 °م—درجة حرارة جسمنا—ويمكن إصابتها بمجموعة واسعة من البكتيريا والفطريات ذات الأهمية الطبية. عندما تمرض، يتغشى جسدها بعملية تُسمى التّصبّغ الميلانيني، ما يوفر للباحثين مؤشرًا مرئيًا على الحالة الصحية. وبما أنها لافقاريات، فهي تتفادى العديد من العقبات القانونية والأخلاقية المرتبطة بتجارب الفقاريات، كما أنها رخيصة التكاثر بكميات كبيرة. وُجد أيضًا أن اليرقات قادرة على تفكيك بعض أنواع البلاستيك الشائعة، مما يلمح إلى استخدامات في البحوث البيئية أيضًا.
الأدوات الجينية المفقودة
بالرغم من هذه المزايا، افتقرت يرقات فراشة الشمع إلى الحيل الجينية المتقدمة المتاحة في الحيوانات المخبرية التقليدية. على مدى العقد الماضي، فككت عدة فرق تسلسلاً لجينوم الفراشة وفهرست جيناتها وبروتيناتها النشطة، لكن الباحثين لم يتمكنوا بسهولة من تشغيل أو إيقاف الجينات أو إضافة علامات مفيدة. حد هذا الفراغ مما يمكن تحقيقه بالنموذج—مثل بناء حيوانات تتوهج عند العدوى أو حذف جينات محددة لاختبار تأثيرها على المناعة. تتصدى الورقة الحالية لهذا التحدي مباشرة عبر تكييف نظامين قويين للهندسة الجينية، يعرفان باسم PiggyBac وCRISPR–Cas9، لاستخدامهما في Galleria mellonella.
بناء يرقات مرصدة تتوهج في الظلام
درس الفريق أولاً توقيت تطور جنين الفراشة المبكر ووجدوا نافذة تقريبية مدتها ست ساعات بعد وضع البيض عندما لا تزال كل النوى المنقسمة تشترك في داخل مشترك. يسمح حقن الحمض النووي خلال هذه الفترة للدنا الجديد أن يدخل جميع الأنسجة اللاحقة، بما في ذلك الخلايا التناسلية المستقبلية. باستخدام هذه النافذة، أدخل الباحثون تراكيب DNA مبنية على ناقل PiggyBac الناقل، وهو عنصر "قص‑ولصق" يُدرِج قطعًا كبيرة من الحمض النووي في الجينوم. بعد اختبار بلزميدات مساعد مختلفة، حددوا نسخة تحمل إنزيم PiggyBac فائق النشاط نجح في إنتاج خطوط متحولة وراثيًا. عبرت هذه اليرقات عن بروتينات فلورية خضراء وحمراء في أنسجة جسدية مميزة، وأظهر تحليل الحمض النووي أن الكاسيت الجيني استقر في منطقة غير ضارة بين جينات أصلية.
مراقبة الخلايا واستئصال الجينات
بعد ذلك، أنشأ المؤلفون خطوط مراسلة أكثر تخصصًا. علّق تركيب واحد بروتينًا بنيويًّا يُدعى التوبولين بفلورية خضراء لتسليط الضوء على الهيكل الخلوي الداخلي، بينما دمج تركيب آخر علامة حمراء ببروتين هستون يلتف حول الحمض النووي في النواة. توهجت هذه الخطوط بأنماط مميزة عبر الأمعاء، وجسم الدهن، وغدد الحرير وأنسجة أخرى، مما أتاح للباحثين تصور هياكل الخلايا في يرقات حية أو مثبتة. للانتقال من مجرد إضافة جينات إلى تعطيلها فعليًا، لجأ الفريق إلى CRISPR–Cas9. حقنوا مجمعات بروتين‑RNA مُجمَّعة مسبقًا مستهدفة للعلامة الفلورية الخضراء في الأجنة التي كانت تحمل بالفعل كاسيت المراسلة. أظهر كثير من النسل فقدانًا جزئيًا أو كليًا للإشارة الخضراء مع بقاء الوميض الأحمر في العين، وأكدت تسلسلات الحمض النووي وجود إدخالات وحذف صغيرة في موقع القطع المستهدف بواسطة CRISPR.
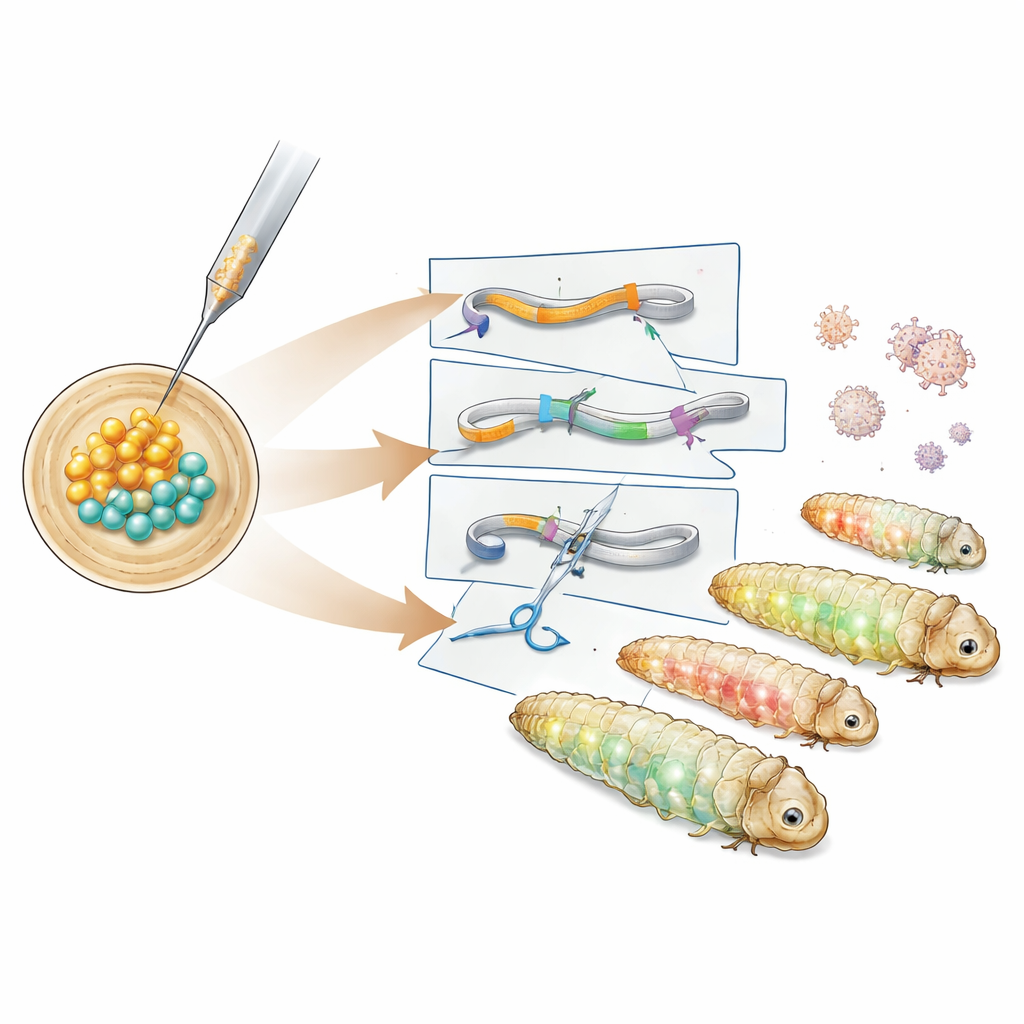
من التقدم التقني إلى الأثر العملي
رغم أن كفاءة كل من PiggyBac وCRISPR في هذه الفراشات لا تزال متواضعة مقارنة ببعض الحشرات الأخرى، يحدد المؤلفون مسارات واضحة للتحسين عبر ضبط المحفزات، وأنماط الإنزيم، واستراتيجيات الحقن. حتى في شكلها الحالي، فإن مجموعة الأدوات قوية بما يكفي لإنتاج خطوط مستقرة تصور مكونات خلوية رئيسية أو تحمل استئصالات جينية مستهدفة. للمختصين غير المتخصصين، الصورة الكبرى هي أن Galleria mellonella يمكن الآن تعديلها تقريبًا بنفس مرونة الحيوانات المخبرية المعروفة أفضل. وهذا يعني أن الباحثين يمكنهم بناء يرقات تُبلّغ عن العدوى، أو تمثل جوانب من المرض البشري، أو تختبر أدوية جديدة بطرق أسرع وأرخص وأكثر إنسانية، مما قد يقلل الاعتماد على نماذج ثديية في بيولوجيا العدوى والمجالات ذات الصلة.
الاستشهاد: Pearce, J.C., Campbell, J.S., Prior, J.L. et al. PiggyBac-mediated transgenesis and CRISPR–Cas9 knockout in the greater wax moth, Galleria mellonella. Lab Anim 55, 95–102 (2026). https://doi.org/10.1038/s41684-025-01665-7
الكلمات المفتاحية: Galleria mellonella, نموذج عدوى لافقاري, الهندسة الوراثية, نقل جيني بواسطة PiggyBac, استئصال بواسطة CRISPR