Clear Sky Science · ar
استهداف EGFR المعبر عنه في السرطان بواسطة جسم مضاد وحيد النسيلة مؤنسن
اكتشاف أعلام السرطان الخفية
غالبًا ما تواجه علاجات السرطان صعوبة في تحقيق توازن بين مهاجمة الخلايا الورمية والحفاظ على الأنسجة السليمة. تصف هذه الورقة جسمًا مضادًا مهندَسًا مخبريًا جديدًا، اسمه A10، قادرًا على تمييز الخلايا السرطانية التي تحمل شكلاً معينًا من مستقبل عامل النمو عن الخلايا الطبيعية. من خلال استهداف شكل يظهر أساسًا عندما يتغير هذا المستقبل أو يزداد تركيزه على الخلايا الورمية، يفتح A10 الباب أمام علاجات تكون في آن واحد فعّالة وأكثر انتقائية من العديد من الخيارات الحالية.
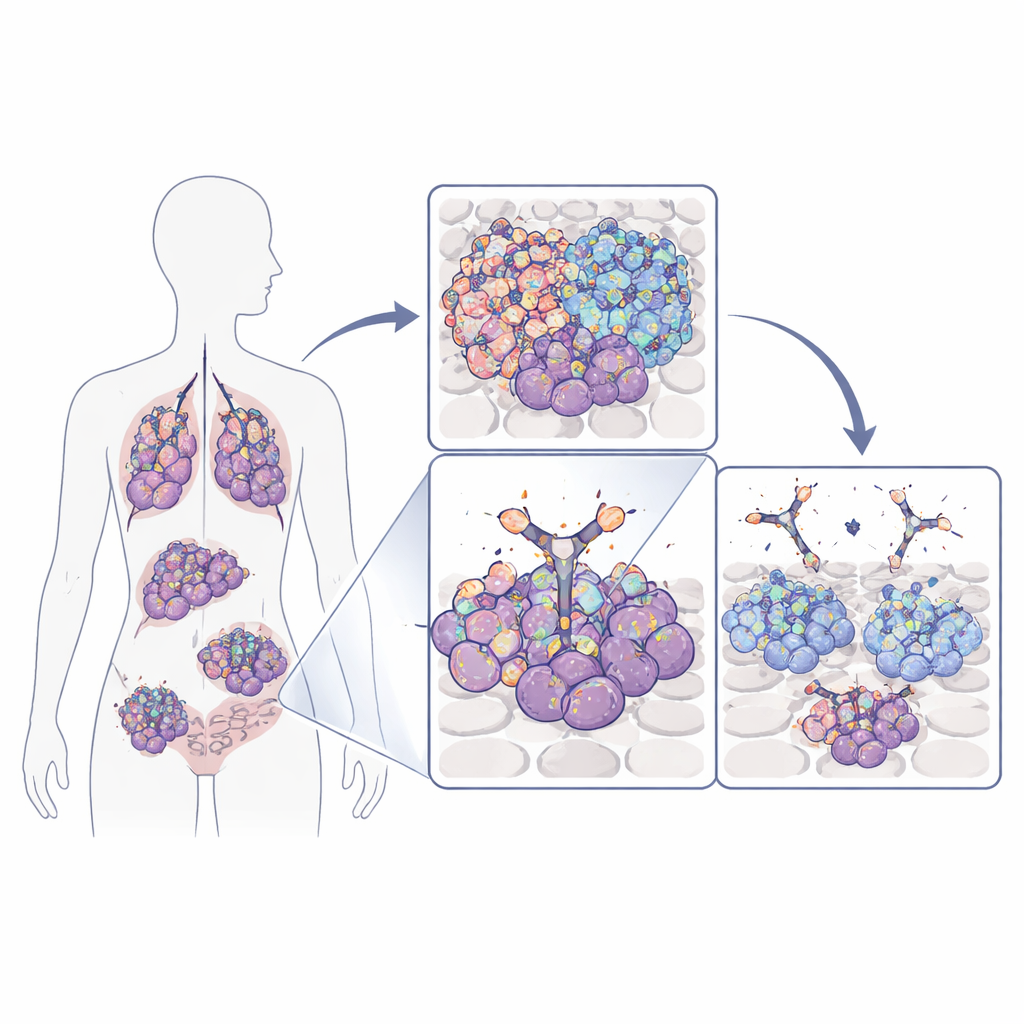
لماذا يهم هذا المفتاح النموّي
تعتمد العديد من الأورام، بما في ذلك سرطانات الدماغ والرئة والثدي والقولون العدوانية، على بروتين سطحي يسمى مستقبل عامل نمو البشرة (EGFR) للنمو والبقاء. يمكن للخلايا الورمية أن تزيِد من هذا المستقبل إما بتضخيم جينه أو بتحويره أو بإنتاج نسخة مختصرة تعمل دائمًا تُعرف باسم EGFRvIII. غالبًا ما تصيب الأدوية التقليدية التي تحجب EGFR كلًا من خلايا السرطان والأنسجة الطبيعية، لأنها تتعرف على أجزاء من المستقبل موجودة في كل مكان. بدلًا من ذلك، ركز فريق هذه الدراسة على حلقة صغيرة من EGFR تصبح ظاهرة بوضوح بشكل رئيسي على الخلايا السرطانية — إما لأن EGFR موجود بأعداد غير طبيعية أو لأن المستقبل مختصر في EGFRvIII. تعمل تلك الحلقة كـ«علم» خاص بالسرطان يمكن، من الناحية العملية، استهدافه بأمان أكبر.
تحويل جسم مضاد فأري إلى دواء بشري
كان الباحثون قد اكتشفوا سابقًا جسمًا مضادًا فأريًا باسم 40H3 يتعرف على هذه الحلقة المكشوفة في EGFR المعبر عنه في السرطان. ومع ذلك، يمكن للأجسام المضادة الفأرية أن تثير تفاعلات مناعية عند إعطائها مرارًا للمرضى. لتجاوز هذا، استخدم الفريق طرق هندسة البروتين لزرع المقاطع الرئيسية الممسكة للـ40H3 على أطر أجسام مضادة بشرية، مكوِّنين أربعة عشر مرشحًا «مؤنسنًا» بالإضافة إلى جزيء مرجعي كيمري. عندما اختبروا هذه المتغيرات على خلايا سرطانية تفرز EGFR بكثرة، ارتبطت ثلاث نسخ جيدًا بصورة خاصة، وبرزت إحداها — A10 — كالأقوى ارتباطًا مع الاستمرار في تجاهل الخلايا الطبيعية ذات مستويات EGFR المتواضعة. عبر مجموعة واسعة من خطوط الخلايا الورمية ذات طفرات أعداد نسخ مختلفة من EGFR، أظهرت A10 ارتباطًا أعلى باستمرار مقارنة بالجسم المضاد الفأري الأصلي وحافظت على تفضيل قوي للخلايا الخبيثة.
رؤية كيف يمسك الجسم المضاد هدفه
لفهم سبب انتقائية A10، حلل الفريق بنية ثلاثية الأبعاد عالية الدقة لجزء الفاعل من الجسم المضاد مربوطًا بحلقة EGFR. تطوى الحلقة إلى «مشبك» ضيق مثبت بجسر ثنائي الكبريتيد، وتحتضن A10 هذا الشكل في أخدود يتشكل بين ذراعيها، مع العديد من التلامسات المشحونة التي تثبته في مكانه. أدى مقارنة هذه البنية مع الأشكال المعروفة لجزيء EGFR الكامل إلى رؤية رئيسية: في كلٍّ من الشكل غير النشط «المقيد» والشكل الثنائي النشط للمستقبل العادي، تكون الحلقة مدفونة إلى حد كبير أو محمية جزئيًا بواسطة المجالات المجاورة. هذا يعني أن A10 لا يمكنه الوصول بسهولة إلى موقع ارتباطه على المستقبلات المعبر عنها بمستويات معتدلة. بالمقابل، في متغير EGFRvIII الخاص بالسرطان، الجزء الأمامي من المستقبل مفقود، ما يترك الحلقة مكشوفة وقابلة للوصول للغاية. تشير البيانات إلى أن A10 يتعرف أساسًا على EGFR خلال أشكال انتقالية معينة وفي الأشكال المزدحمة أو المختصرة التي تظهر بشكل مفضّل على الخلايا الورمية.
تسليح الجسم المضاد لقتل الخلايا الورمية
إدراك علم خاص بالورم مفيد في حد ذاته، لكن الباحثين ذهبوا أبعد من ذلك بتحويل A10 إلى مركب دوائي — جسم مضاد مرتبط بمخدر (ADC). ربطوا كيميائيًا مركبًا قاتلًا للخلايا قويًا، مونو ميثيل أورستاتين E (MMAE)، بـA10 باستخدام رابط يمكن قطعه داخل الخلايا. ارتبط هذا الـA10‑MMAE ADC بالخلايا السرطانية بنفس جودة الجسم المضاد غير المرتبط. في اختبارات مخبرية عبر خطوط خلوية عديدة، كان المركب الأكثر فعالية ضد الأورام ذات مستويات EGFR العالية جدًّا أو EGFRvIII، حيث كانت مواقع ارتباط A10 وفيرة. في هذه الخلايا، كانت كميات صغيرة للغاية من المركب كافية لإطلاق موت الخلايا. كانت خطوط الأورام ذات أهداف A10 القليلة أو المقاومة الطبيعية لـMMAE أقل تأثرًا، وظلت الخلايا الليفية الطبيعية الحاملة EGFR البريّة دون ضرر على الرغم من حساسيتها لـMMAE الحر. تظهر النتائج أن الجمع بين ارتباط انتقائي وإطلاق الدواء داخليًا يمكن أن يركّز السمية بشكل حاد على الخلايا السرطانية.
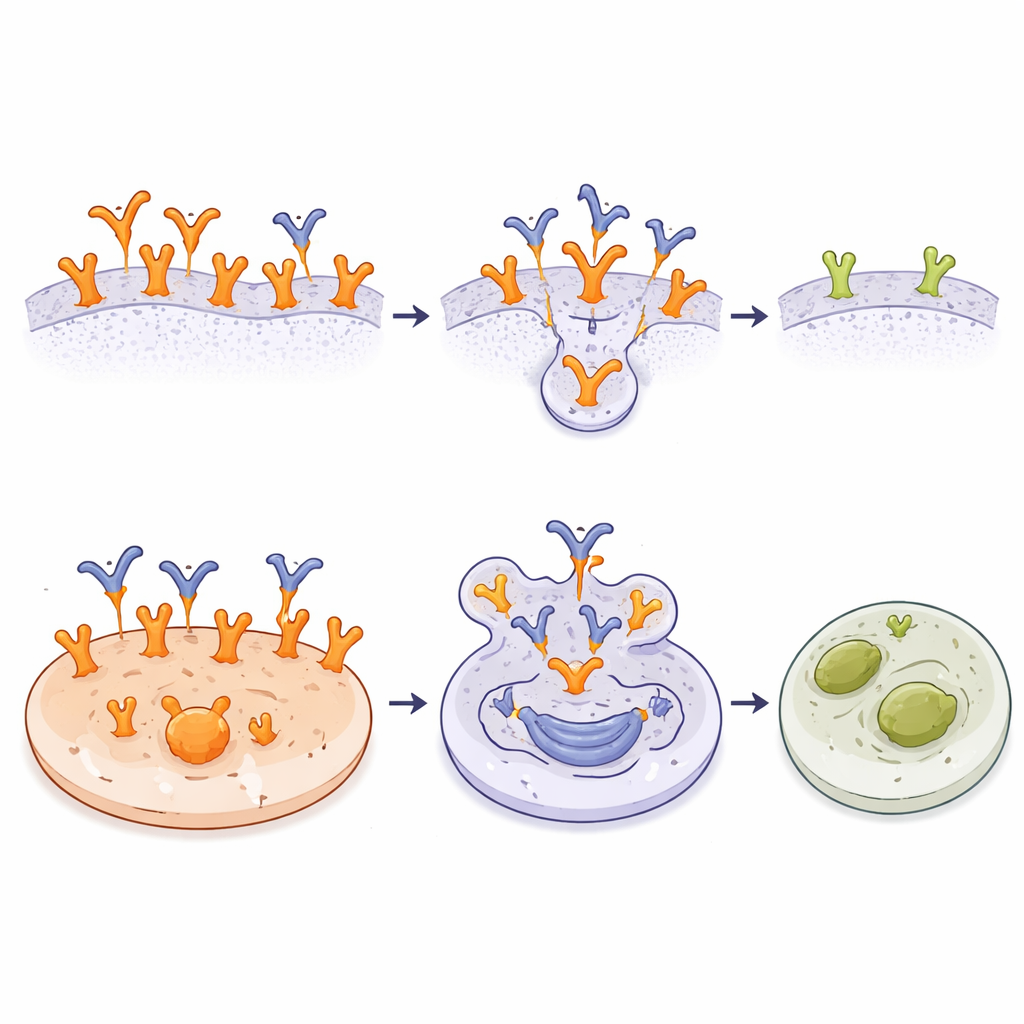
ماذا قد يعني هذا لرعاية السرطان المستقبلية
بعبارة بسيطة، تُظهر هذه الدراسة أنه من الممكن بناء جسم مضاد «يرى» EGFR فقط عندما يبدو ويتصرف كمستقبل محرِّك للسرطان، بينما يتجاهل في الغالب شكله اليومي على الأنسجة السليمة. من خلال رسم خريطة دقيقة لكيفية إمساك A10 بحلقة مخفية على EGFR وإثبات أن مركبًا دوائيًا قائمًا على A10 يمكنه قتل خلايا الورم الغنية بالمستقبل بكفاءة مع إبقاء الخلايا السليمة سالمة، توفِّر الدراسة أساسًا قويًا لتطوير علاجات أكثر أمانًا وذات استهداف عالٍ. إذا ترجمت هذه النتائج إلى المرضى، فقد تقدم العلاجات المستقبلية المبنية على A10 أدوية قوية مباشرة إلى سرطانات معتمدة على EGFR مع الحفاظ إلى حد كبير على باقي جسد المريض دون مساس.
الاستشهاد: Costa, T.G.F., Sarnovsky, R., Zhan, J. et al. Targeting cancer expressed EGFR with a humanized monoclonal antibody. Sci Rep 16, 10814 (2026). https://doi.org/10.1038/s41598-026-46245-y
الكلمات المفتاحية: EGFR, مركب دوائي جسم مضاد, علاج سرطاني مستهدف, ذبحة دماغيّة متعدّدة البؤر (غليوبلاستوما), EGFRvIII