Clear Sky Science · ar
المركب الفلوروكينوليني يظهر تأثيرات مضادة للاريثروليوكيميا عبر استهداف مزدوج لـ GLUT1 ومسار الإشارة PI3K/AKT
زاوية جديدة تجاه سرطان دم خطير
الاريثروليوكيميا هي شكل نادر لكنه عدواني للغاية من سرطانات الدم مع خيارات علاجية قليلة تتجاوز زرع الخلايا الجذعية. بالنسبة للعديد من المرضى، وغالبيتهم من كبار السن، يعني هذا علاجات قاسية، تكاليف مرتفعة، واحتمالات قاتمة. تستكشف هذه الدراسة مركباً مصمماً مخبرياً يسمى FKL-137 يتعامل مع خلايا الاريثروليوكيميا بطريقة غير متوقعة: عن طريق قطع مصدر وقودها المفضل، السكر، وتحفيز موتها الذاتي. تشير النتائج إلى فئة محتملة جديدة من الأدوية الموجهة التي تستغل اعتماد خلايا السرطان على استخدام الطاقة المعاد برمجته مع الحفاظ على مزيد من أنسجة الجسم السليمة.
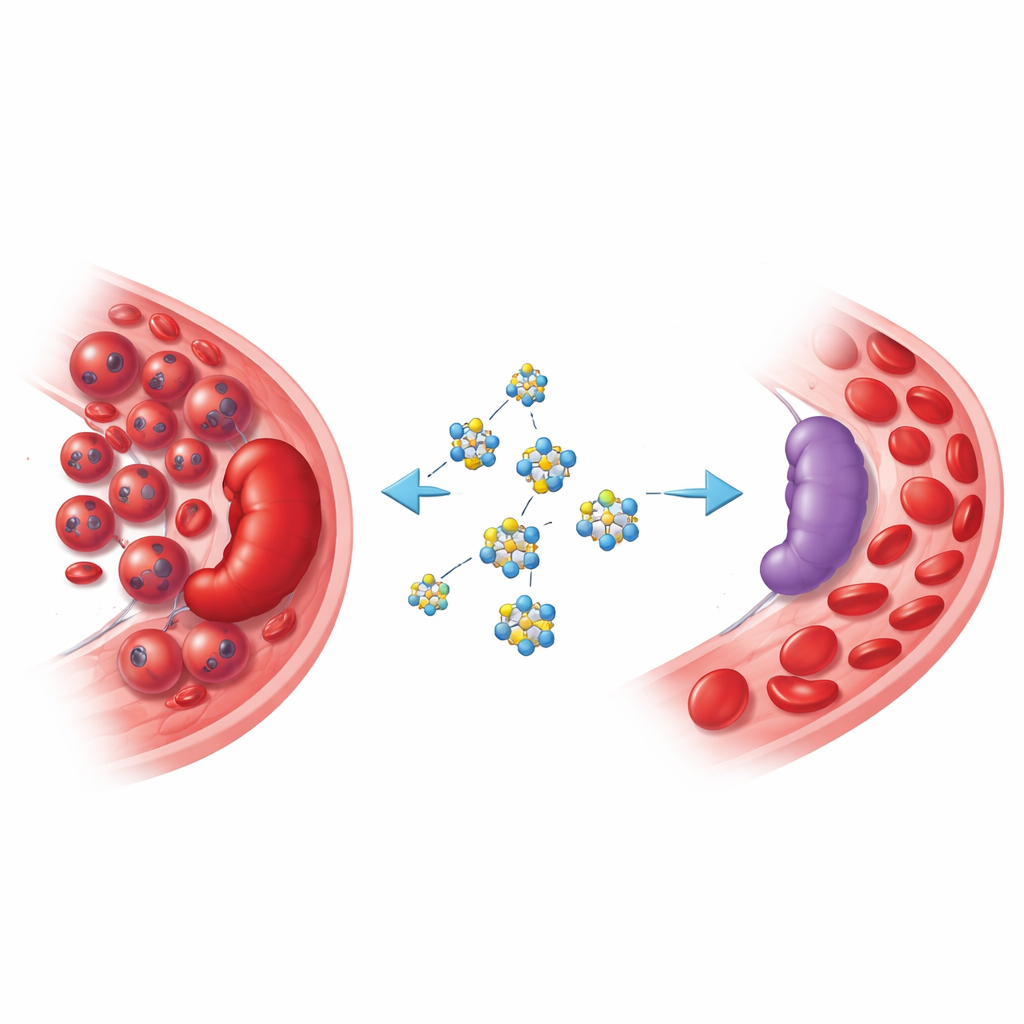
عندما تنحرف خلايا الدم
في الاريثروليوكيميا، تتكاثر خلايا سلفية حمراء غير ناضجة بشكل غير منضبط في نخاع العظم والطحال. قد يعاني المرضى من فقر دم شديد، وتورم في الطحال يعرّضه لخطر التمزق، وتدهور سريع في الحالة الصحية. العلاجات الحالية محدودة، والعديد من المرضى ضعفاء جداً لتحمّل علاجات مكثفة. في الوقت نفسه، تعلّم العلماء أن العديد من سرطانات الدم تعتمد على إعادة برمجة استخدام السكر: فهي تستوعب الجلوكوز بمعدلات عالية وتحوله بسرعة إلى طاقة وركائز بنائية، مما يساعدها على التكاثر وتجنب الجهاز المناعي. أصبح استهداف هذا "الإدمان" الأيضي استراتيجية جاذبة للأدوية الجديدة.
جوع خلايا السرطان عن السكر
ركز الباحثون على جزيء صناعي صغير، FKL-137، مشتق من عائلة كيميائية معروفة بالفعل بنشاطها المضاد للسرطان. في تجارب مخبرية، عرّضوا سلسلتين خلويتين بشريتين من الاريثروليوكيميا لجرعات متزايدة من FKL-137. أبطأ المركب نمو الخلايا بشكل حاد مع مرور الوقت ودفع الخلايا نحو الموت المبرمج، كما ظهر ذلك من خلال تغيّرات شكل الخلية الكلاسيكية وتنشيط آليات الموت الداخلية. ومن المهم أن FKL-137 كان أكثر فعالية بكثير ضد خلايا اللوكيميا مقارنة بخلايا الكبد الطبيعية، وأشارت مقاييس سلامة الدواء إلى سمّية منخفضة نسبياً عند الجرعات الفعالة.
استهداف بوابات السكر في السرطان
غصت المجموعة أعمق لسؤال كيف يتداخل FKL-137 مع استقلاب السرطان. وجدوا أن الخلايا المعالجة امتصت كمية أقل من الجلوكوز وأفرجت عن لاكتات أقل، وهو ناتج ثانوي لحرق السكر المكثف. تم خفض مستويات بروتينات رئيسية تساعد عادةً على تحويل الجلوكوز إلى طاقة وركائز بنائية. باستخدام النمذجة الحاسوبية، واختبارات الاستقرار الحراري، والتصوير، أظهر الباحثون أن FKL-137 يرتبط بـ GLUT1، وهي "بوابة" كبيرة على سطح الخلية تسمح بدخول الجلوكوز إلى الداخل. عندما تم تقليل مستويات GLUT1 بالحيلة الجينية، نمت خلايا اللوكيميا ببطء أكبر واستهلكت سكرًا أقل، وأصبحت أكثر حساسية لـ FKL-137. هذا أكد أن GLUT1 هو محرك لنمو خلايا الاريثروليوكيميا وهدف مهم لهذا الدواء.
تعطيل حلقة إشارة النمو
كشفت الدراسة أيضاً عن تأثيرات تتجاوز بوابة الجلوكوز بحد ذاتها. تستخدم خلايا الاريثروليوكيميا عادةً مسار إشاري يعرف باسم PI3K/AKT لتعزيز البقاء والنمو والاستهلاك العالي للسكر، جزئياً عن طريق دعم GLUT1. خفض علاج FKL-137 الأشكال النشطة لبروتينات رئيسية في هذا المسار، مكسرًا حلقة تعزيز متبادلة بين نقل السكر وإشارات النمو. في فئران مصابة بفيروس يسبب الاريثروليوكيميا بشكل موثوق، حسّن علاج FKL-137 مستويات خلايا الدم الحمراء، وقلّص الطحال المتضخم، وقلّل غزو خلايا السرطان للأعضاء، وصحّح الاستقلاب السكري الشاذ في نسيج الطحال — كل ذلك من دون أضرار واضحة في القلب أو الكبد أو الرئتين أو الكليتين.
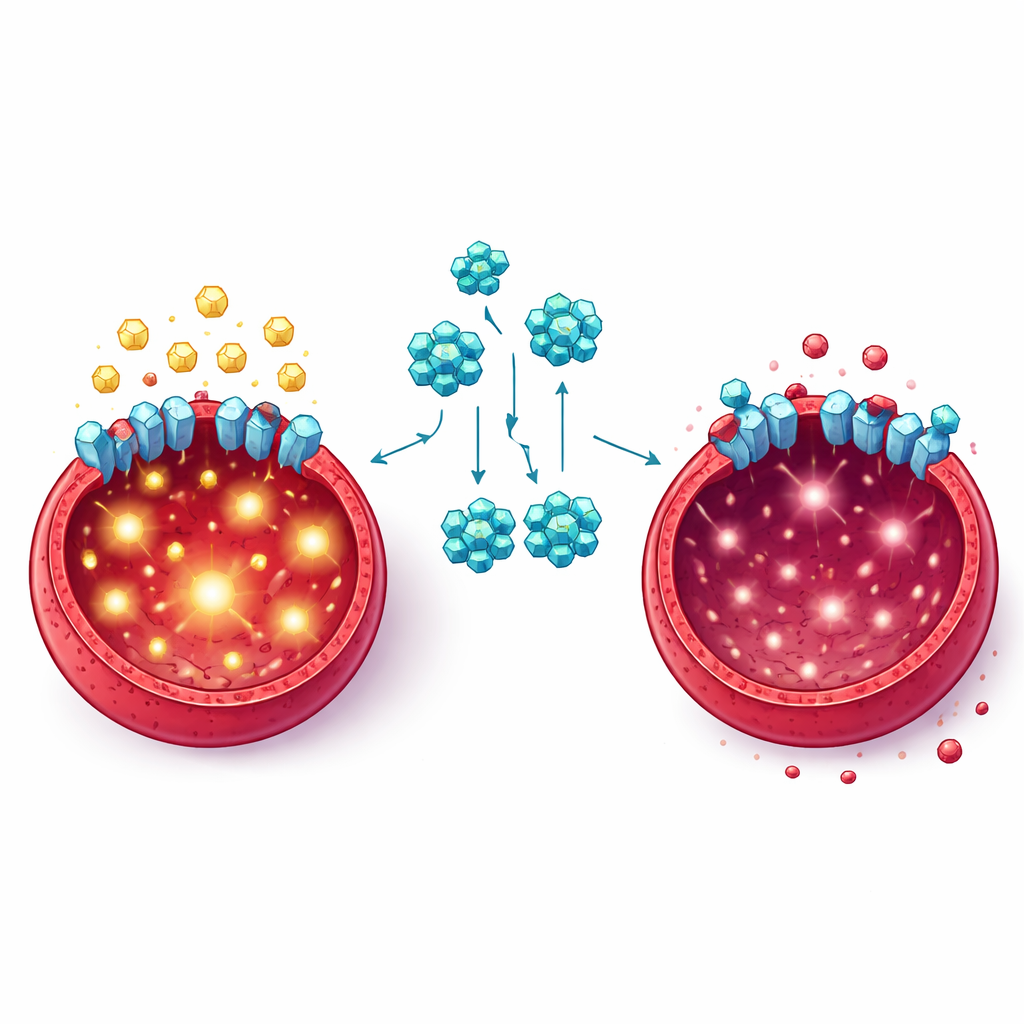
وعد وحدود وخطوات لاحقة
بشكل إجمالي، تعرض هذه الأعمال FKL-137 كمرشح دوائي ذو فعل مزدوج يعيق بوابة السكر الرئيسية في خلايا الاريثروليوكيميا ويخفّض في الوقت نفسه مسار نمو قوي يعتمد على ذلك الوقود. من خلال تجويع خلايا السرطان أولاً ثم دفعها نحو الموت، يقدم المركب نهجًا أنيقًا مفهوماً لاستغلال ضعف لا تشاركه الخلايا الطبيعية بنفس الدرجة. يحذر المؤلفون مع ذلك من أن FKL-137 ما يزال يحتاج إلى تحسين: لديه نافذة جرعة ضيقة نسبياً، قد تجد خلايا السرطان طرقًا لتعويض ذلك بإعادة توجيه استقلابها، ويجب تأكيد النتائج المستخلصة من خطوط الخلايا ونماذج الفئران في أنسجة بشرية. ومع ذلك، تعزّز الدراسة الفكرة القائلة إن استهداف كيفية تغذية ونمو خلايا السرطان بدقة قد يفتح جبهة جديدة لعلاج هذا السرطان الدموي الذي يصعب إدارته بخلاف ذلك.
الاستشهاد: Cheng, S., Zhao, W., Yu, J. et al. The fluoroquinoline compound exerts anti-erythroleukemic effects by dual-targeting GLUT1 and the PI3K/AKT signaling pathway. Sci Rep 16, 10916 (2026). https://doi.org/10.1038/s41598-026-45597-9
الكلمات المفتاحية: الاريثروليوكيميا, تمثيل غذائي للسرطان, مثبط GLUT1, مسار PI3K AKT, العلاج الموجه