Clear Sky Science · ar
الإنترفيرون-β وFTY720 يخففان الالتهاب التقدمي في الجهاز العصبي المركزي عبر إشارة الخلايا النجمية المرتبطة بـ SOCS1
لماذا يهم هذا البحث الأشخاص المصابين بالتصلب المتعدد
بالنسبة لكثير من المصابين بالتصلب المتعدد، الخوف الأكبر ليس النوبات المبكرة بل الفقدان البطيء والمستمر للوظائف الذي قد يتبعها. في هذه المرحلة اللاحقة والتقدمية، يستمر الضرر داخل الدماغ والحبل الشوكي حتى عندما تقوم الأدوية التقليدية المستهدفة للجهاز المناعي في الدم بدورها. تستكشف هذه الدراسة طريقة للوصول إلى ذلك الالتهاب «المخفي» عبر الجمع بين قرص متوافر لعلاج التصلب المتعدد وشكل من دواء مستخدم منذ زمن يُعطى مباشرة ليصل إلى الدماغ.
مرض دماغي طويل الأمد مع خيارات محدودة
التصلب المتعدد هو مرض مناعي ذاتي تهاجم فيه خلايا الجهاز المناعي في الجسم غلاف العزل للألياف العصبية، ما يؤدي إلى مشاكل في الرؤية وضعف وأعراض عصبية أخرى. في المراحل المبكرة، تميل الأعراض إلى التواتر والاختفاء. مع مرور الوقت يدخل العديد من المرضى مرحلة تقدمية تتسم بالإعاقة التدريجية وغالباً غير القابلة للعكس. خلال هذه المرحلة، يصبح من الأصعب على الأدوية عبور الحاجز الدم–دماغ، وتلعب الأنشطة الضارة لخلايا مقيمة في الدماغ تسمى الدبق—وخاصة الخلايا النجمية والميكروغليا—دورًا متزايدًا. العلاجات الحالية، التي تعمل في معظمها بحجب خلايا المناعة في الدم، تقدم مساعدة محدودة بمجرد ترسيخ هذه المرحلة.
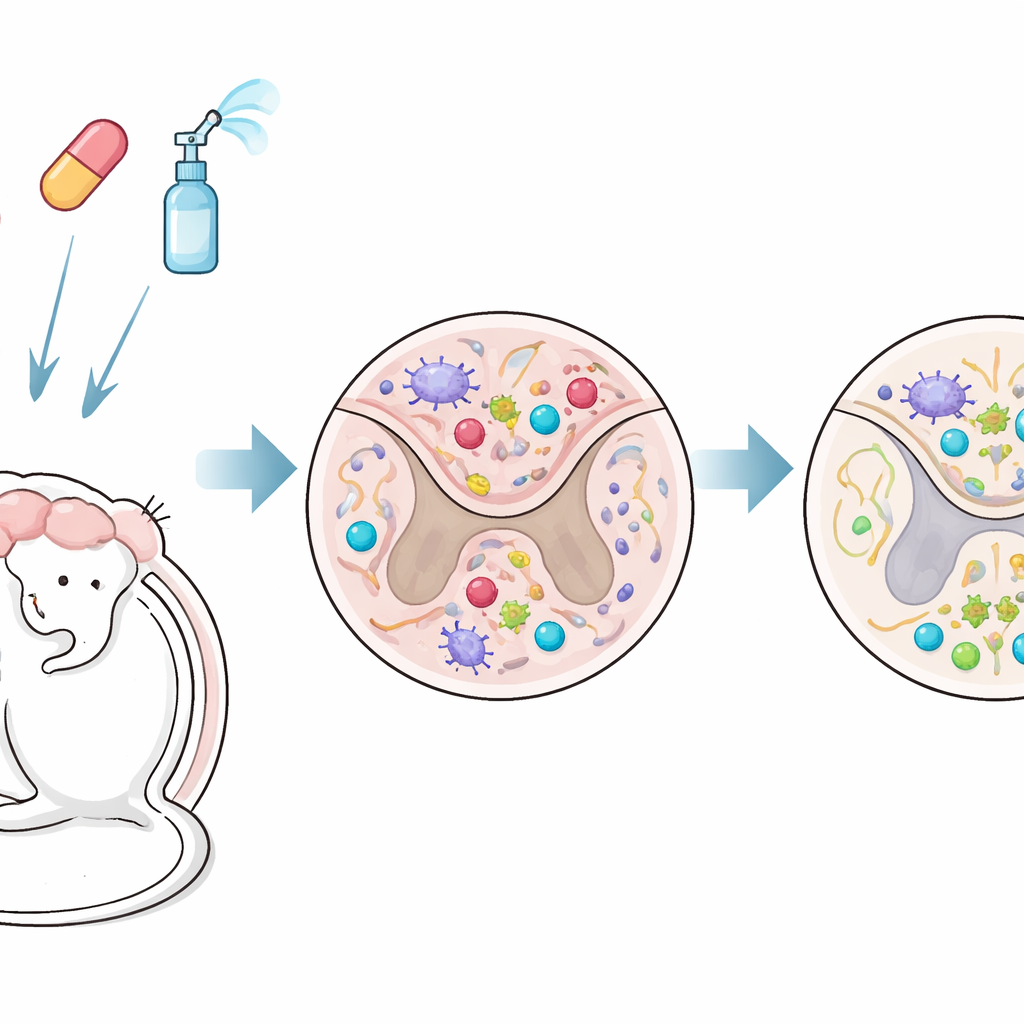
مزاوجة عقارين للوصول إلى الدم والدماغ معًا
اختبر الباحثون علاجًا مركبًا في نموذج فأري يحاكي عن قرب التصلب المتعدد التقدمي. أحد العقارين، فينجوليمود (FTY720)، هو قرص يحجز خلايا المناعة في العقد الليمفاوية ويمكنه أيضًا دخول الدماغ. والعقار الآخر، الإنترفيرون‑بيتا، علاج طويل الأمد للتصلب المتعدد يعمل عادة خارج الدماغ لأنه لا يعبر الحاجز الدم–دماغ بسهولة. في هذه الدراسة، أُعطي الإنترفيرون‑بيتا عبر الأنف—من خلال القناة الأنفية—حتى يتجاوز هذا الحاجز ويصل إلى الجهاز العصبي المركزي بصورة أكثر مباشرة. بدأ العلاج بعد أن تطورت لدى الفئران بالفعل مشاكل عصبية مزمنة، ما يعكس مرحلة يكون فيها الضرر أصعب عادة على العكس.
أضرار أقل ونشاط مناعي أهدأ
الفئران التي تلقت علاج الفينجوليمود بالإضافة إلى الإنترفيرون‑بيتا عبر الأنف أظهرت نتائج أفضل من تلك التي أعطيت الفينجوليمود وحده. تحسنت درجات المرض لديها أكثر، وتراجعت بعض العجزات العصبية القائمة. عند فحص العلماء للحبال الشوكية، وجدوا مزيدًا من الحفاظ على الميالين، وقلة علامات إصابة المحاور العصبية، وانخفاضًا في الخلايا المناعية المتسللة. انخفضت الخلايا التائية والوحيدات المسببة للالتهاب، وأنتجت الخلايا التائية المتبقية كميات أقل من الجزيئات المرسلة الضارة مثل الإنترفيرون‑غاما وIL‑17. والأهم أن العلاج المركب خفف أيضًا الإشارات الضارة الصادرة من الخلايا النجمية والميكروغليا، الخلايا الدبقية التي تُشكل البيئة المحلية داخل الدماغ والحبل الشوكي.
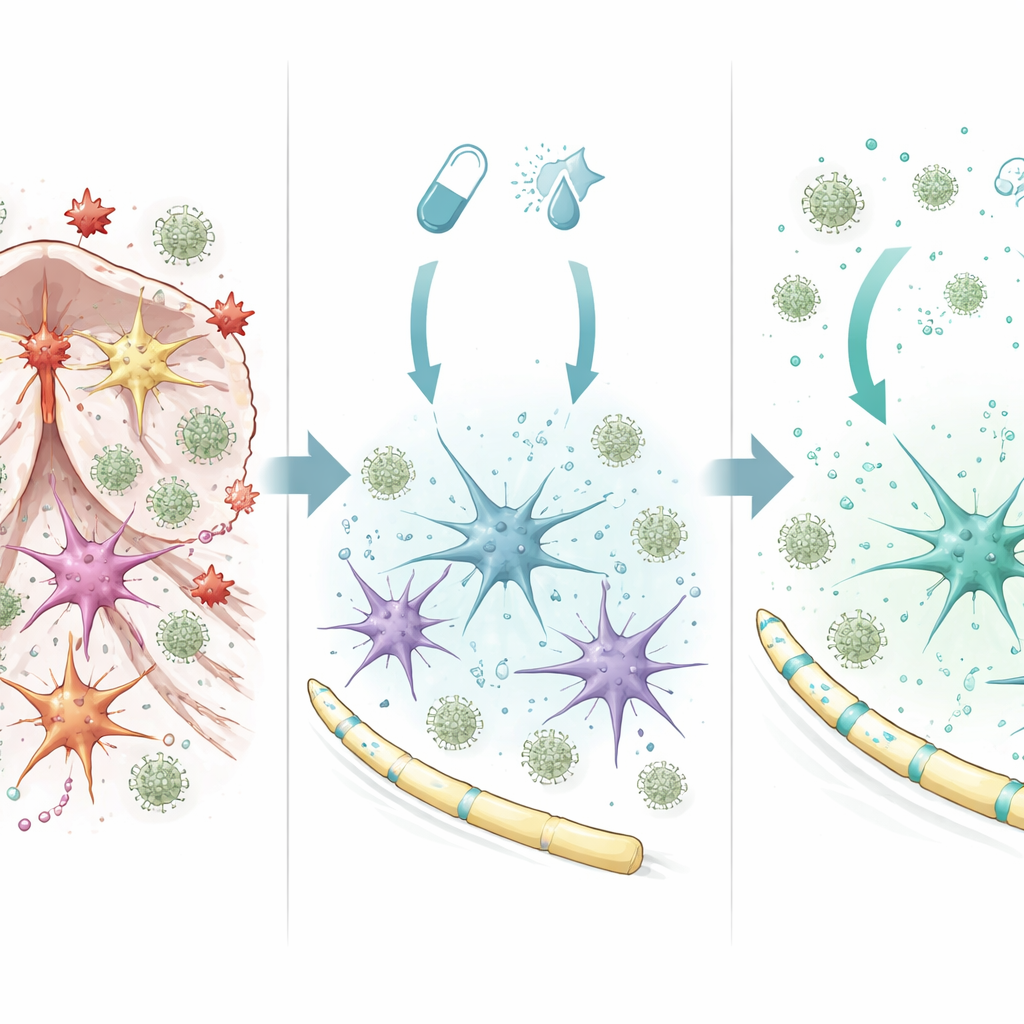
الخلايا النجمية تنقلب من سلوك ضار إلى وقائي
لفهم كيفية عمل العلاج المركب داخل الدماغ، درس الفريق خلايا نجمية منظفة في الزرع الخلوي. عندما تعرضت الخلايا النجمية للفينجوليمود مع الإنترفيرون‑بيتا، شغَّلت مجموعة واسعة من الجينات المرتبطة ببقاء الخلايا، وتقليل الالتهاب، وصحة عزل الأعصاب. كان لاعب أساسي هو منظم يُدعى SOCS1، الذي يعمل كمكبح لإشارات الالتهاب. حجب SOCS1 في الخلايا النجمية أزال جزءًا كبيرًا من نمط الجينات الوقائي وتسبب في إفراز هذه الخلايا لمزيد من العوامل الالتهابية التي جذبت خلايا مناعية. على النقيض، عندما كان SOCS1 نشطًا، أنتجت الخلايا النجمية مزيدًا من إشارات النمو والإصلاح وأفرجت مزيجًا من الجزيئات الذي قلل هجرة الوحيدات الالتهابية. شوهدت تحولات وقائية مماثلة في خطوط خلايا بشرية من الخلايا النجمية والميكروغليا المعالجة بالمزيج الدوائي، مما يوحي بأن الآلية ذات صلة تتجاوز الفئران.
ما الذي قد يعنيه هذا لعلاجات التصلب المتعدد المستقبلية
تُظهر هذه الدراسة أن مزاوجة فينجوليمود مع إنترفيرون‑بيتا الممنوح عبر الأنف يمكن أن تفعل أكثر من مجرد حجب خلايا المناعة في الدم. يمكنها أيضًا إعادة برمجة الخلايا النجمية داخل الجهاز العصبي المركزي نحو حالة أكثر هدوءًا وحماية، مع عمل SOCS1 كعقدة تحكم مركزية. وبينما أُجري العمل في فئران وزرعات خلوية، ولم يُختبر الإنترفيرون‑بيتا وحده جانبًا إلى جانب في جميع التجارب، تشير النتائج إلى استراتيجية واعدة: استهداف كل من الجهاز المناعي المحيطي وخلايا الدعم داخل الدماغ في آن واحد. إذا أمكن تحقيق آثار مماثلة وإثبات سلامتها في البشر، فقد تساعد مثل هذه النهج المركبة الموجهة إلى الدماغ في إبطاء أو جزئيًا عكس الضرر الصامت الذي يدفع التصلب المتعدد التقدمي.
الاستشهاد: Tsaktanis, T., Beyer, T., Nirschl, L. et al. Interferon-β and FTY720 ameliorate progressive CNS inflammation via SOCS1-associated astrocyte signaling. Sci Rep 16, 9851 (2026). https://doi.org/10.1038/s41598-026-45303-9
الكلمات المفتاحية: التصلّب المتعدد التقدّمي, فينجوليمود, الإنترفيرون بيتا, الخلايا النجمية, الالتهاب العصبي