Clear Sky Science · ar
التحقيق في تفاعلات بروتين المناعة كوليسين E9 من Escherichia coli مع gyrase الحمض النووي لبكتيريا Pseudomonas aeruginosa: نهج حوسبي متقدّم لتطوير استراتيجيات مضادة للميكروبات مبتكرة
تحويل أسلحة البكتيريا إلى أدوية جديدة
مع انتشار مقاومة المضادات الحيوية، تقل الوسائل المتاحة للأطباء لوقف العدوى الخطيرة. بعض المسببات الأكثر إصراراً، مثل Pseudomonas aeruginosa، قادرة على التحلل أمام العديد من الأدوية. تبحث هذه الدراسة في عالم البكتيريا نفسه عن أفكار جديدة، مستكشفة إمكانية إعادة توظيف بروتين وقائي طبيعي لدى ميكروب واحد لتعطيل إنزيم حيوي لدى آخر. باستخدام محاكاة حاسوبية متقدّمة، يبيّن الباحثون كيف أن بروتين «المناعة» الصغير يمكن أن يلتصق بإحكام بإنزيم بكتيري رئيسي، ما يشير إلى مسار جديد محتمل لمضادات الميكروبات المستقبلية.
درع صغير ضد سم قاتل
بعض سلالات Escherichia coli تُنتج سموم بروتينية قوية تُسمى الكوليسينات (colicins) التي يمكن أن تقتل البكتيريا المجاورة. ولتفادي تسميم نفسها، تنتج هذه البكتيريا أيضاً بروتينات مناعة مطابقة. أحد هذه الحمايات، المعروف ببروتين مناعة الكوليسين E9 (الذي يُشار إليه غالباً باسم Im9)، يرتبط بمجال القطع في السم ويمنعه من إتلاف حمض نووي الخلية. ونظراً لدقة وقوة هذه الشراكة، فقد شكّ العلماء منذ زمن أن فهمها تفصيلياً قد يكشف طرقاً جديدة للتحكم بالبكتيريا الضارة. في هذا العمل، يسأل المؤلفون ما إذا كان Im9 قد يلتصق أيضاً بجيراز الحمض النووي (DNA gyrase)، الإنزيم الحيوي في Pseudomonas aeruginosa الذي يدير كيفية لف ونسخ حمضه النووي.
استهداف إنزيم ضعيف في جرثومة يصعب علاجها
تُعد Pseudomonas aeruginosa ممرضاً مستشفوياً رئيسياً، قادراً على البقاء في بيئات قاسية ومقاوماً للعديد من الأدوية. يُعتبر gyrase الحمض النووي من بين أهم إنزيماتها، فهو مسؤول عن المحافظة على لفّ خيوط الحمض النووي الطويلة بطريقة مناسبة لتتمكن من النسخ. وبما أن تعطيل هذا الإنزيم يمكن أن يوقف نمو البكتيريا، فهو هدف مثبت لبعض المضادات الحيوية. استخدم المؤلفون أداة تعلّم عميق لمسح البنية ثلاثية الأبعاد لـ gyrase في Pseudomonas وتحديد «نقاط ساخنة» محتملة — تجمعات من الأحماض الأمينية على سطحه الأهم في الارتباط بشركاء آخرين. تشكل هذه المناطق جيب الإنزيم الفعّال، حيث تجري عمليات معالجة الحمض النووي الطبيعية وحيث من المثالي أن يرتبط مثبط محتمل.
محاكاة مصافحة جزيئية
للاطّلاع على ما إذا كان Im9 قد يقبض على هذه النقاط الساخنة، لجأ الباحثون إلى برامج تركيب جزيئي (docking) تصوّر «ملائمة» البروتينات مع بعضها كقطع أحجية ثلاثية الأبعاد. أولاً، قاموا بتنقية وإكمال الهياكل المتاحة لكل من Im9 وgyrase، فأصلحوا حلقة مفقودة في الإنزيم وأجروا محاكاة قصيرة للاسترخاء وإزالة أي مناطق متوترة. ثم استخدموا أداتين تكميليتين للتراص، ClusPro وLightDock، لتوليد العديد من المجمعات المرشحة. من بينها اختاروا الترتيبات الأكثر وعداً وخضعّت لمحاكاة ديناميكا جزيئية طويلة امتدت لمئات النانوسواندات. سمحت لهم هذه «الأفلام» الزمنية بمراقبة كيفية تكيّف البروتينين ومرونتهما واستقراهما إلى أشكال أكثر ثباتاً عند الارتباط.
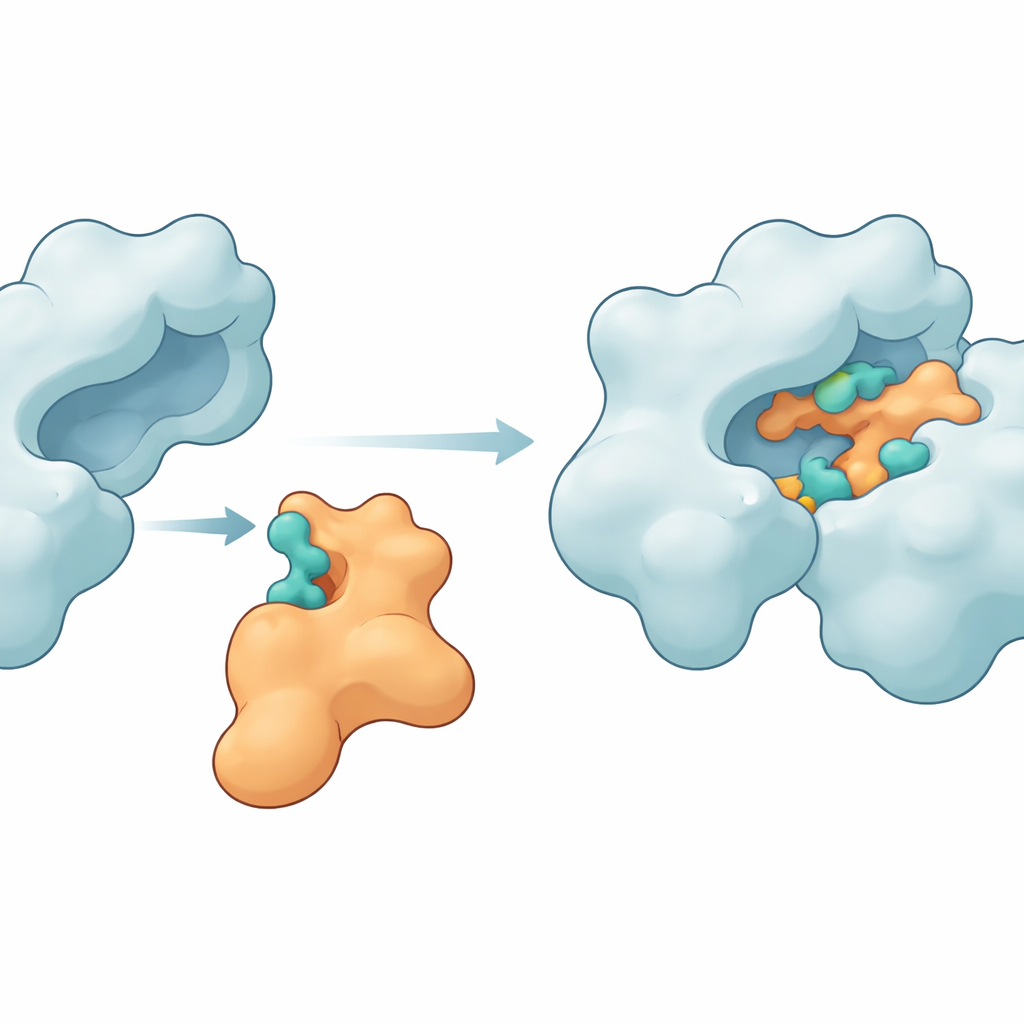
نقاط اتصال رئيسية تُمسك البروتينين معاً
أظهرت المحاكاة أن Im9 يمكن بالفعل أن يشكل مركباً مدمجاً ومستمراً مع gyrase الحمض النووي. عدة أحماض أمينية على الإنزيم — مثل MET27 وASP47 وLYS105 وLEU198 وASN199 وARG191 وGLU194 — شكلت مراراً روابط هيدروجينية وقوى جاذبة أخرى مع مواقع مطابقة على Im9. في نموذج رائد واحد، حافظ الشريكان على بين ست و10 روابط هيدروجينية خلال معظم المحاكاة، وهو علامة على واجهة قوية ومنظمة جيداً. مقاييس بنيوية أخرى، بما في ذلك مدى تماسك البروتينين وكم تقلبت أشكالهما، أظهرت أن الإنزيم بقي سليم البنية بينما تموّج بروتين المناعة بما يكفي ليتشكل حول سطح الجيراز. دعمت حسابات الطاقة باستخدام طريقة MM-GBSA أيضاً فكرة أن هذه التلامسات تخلق طاقة ارتباط حرة مواتية، وإن كانت متواضعة، تغلب عليها مساهمات كهرستاتيكية وفان دير فال.
من النماذج الحاسوبية إلى مضادات ميكروبات مستقبلية
بشكل مجمّع، تشير النتائج إلى أن بروتين مناعة الكوليسين E9 قادر على الارتباط بثبات بمنطقة الفعالية في gyrase الحمض النووي لدى Pseudomonas، مكوناً مركباً طويل العمر قد يعيق من حيث المبدأ الدور الطبيعي للإنزيم في معالجة الحمض النووي. وعلى الرغم من أن هذه النتائج مبنية كلياً على نماذج حاسوبية وتحتاج بعد ذلك إلى اختبارات تجريبية، فإنها توفر مخططاً تفصيلياً لمكان وكيفية ارتباط مثبط مرتكز على البروتين. للقراء غير المتخصصين، الرسالة الأساسية هي أن أسلحة ودروع البكتيريا الطبيعية يمكن أن تلهم استراتيجيات جديدة ضد العدوى الصعبة العلاج. ومن خلال فهم هذه المصافحة المجهرية على المستوى الذري، يقترب العلماء خطوة نحو تصميم مضادات ميكروبات مبتكرة تغلق إنزيمات بكتيرية حاسمة من دون الإضرار بخلايا الإنسان.
الاستشهاد: Alfaraj, R., Alkathiri, F. & Chikhale, R. Investigating Escherichia coli Colicin E9 immunity protein interactions with DNA gyrase of Pseudomonas aeruginosa: advanced computational approach for developing novel antimicrobial strategies. Sci Rep 16, 10786 (2026). https://doi.org/10.1038/s41598-026-44427-2
الكلمات المفتاحية: مقاومة المضادات الحيوية, gyrase الحمض النووي, تفاعلات بروتين–بروتين, تصميم أدوية حوسبي, Pseudomonas aeruginosa